Ghid pentru tratamentul pacientilor cu aritmii ventriculare si
prevenirea mortii subite cardiace
Preambul
Este
important ca medicii au un rol semnificativ in evaluarea critica a
folosirii mijloacelor diagnostice si terapeutice pe parcurs ce sunt
introduse si testate in detectarea, managementul sau preventia
bolilor. Analizele riguroase ale datelor disponibile asupra beneficiilor
si riscurilor absolute si relative ale acelor proceduri si terapii
pot produce ghiduri utile care sa imbunatateasca eficienta
ingrijirii, optimizarea beneficiilor pacientilor, si care sa
afecteze favorabil costurile globale prin concentrarea cercetarii asupra
strategiilor cu eficienta maxima.
Fundatia
American College of Cardiology (ACCF) si American Heart
Association (AHA) s-au angajat in producerea unor asemenea ghiduri in
domeniul bolilor cardiovasculare incepand cu anul 1980. Grupul de Lucru al
Ghidurilor de Practica ACC/AHA, a carui sarcina este sa
dezvolte, sa actualizeze sau sa revizuiasca ghidurile de
practica pentru bolile si procedurile cardiovasculare importante
conduce acest proces. Grupul de Lucru este multumit ca a dezvoltat
acest ghid impreuna cu Societatea Europeana de Cardiologie (ESC).
Comitetele de redactare sunt insarcinate sa evalueze dovezile
si sa actioneze independent in formularea recomandarilor
de practica.
Expertii
in subiectele tratate au fost selectati din cele trei organizatii
pentru a evalua subiecte specifice si a scrie ghidul. Procesul include
si reprezentanti ai altor specialitati, in situatiile
adecvate. Comitetele de redactare sunt insarcinate specific sa
studieze publicatiile aparute, sa cantareasca
dovezile pentru sau impotriva unui anumit tratament sau procedura, si
sa faca estimari atunci cand exista informatii.
Factorii individuali, comorbiditatile si preferinta
pacientului care pot influenta alegerea unui test sau mijloc terapeutic,
sunt de asemenea luate in considerare, ca si fracventa urmaririi
si eficacitatea costului. Cand sunt disponibile, informatiile din
studii asupra costurilor vor fi luate in considerare; Totusi, datele
despre eficacitatea si beneficiile clinice constituie baza
recomandarilor din acest ghid.
Grupul
de Lucru ACC/AHA al Ghidurilor de Practica si Comitetul ESC pentru
Ghiduri de Practica fac toate eforturile pentru a preveni orice conflict
de interese, actual, potential, sau perceput ca existent, care pot apare
ca urmare a legaturilor membrilor lor cu industria medicala sau a intereselor
personale. Toti membrii Comitetului de Redactare, ca si evaluatorii
documentului prezent, au declarat relatiile care ar putea fi percepute
drept conflicte de interese, reale sau potentiale. Membrii Comitetului au
fost incurajati sa declare legaturile anterioare cu industria
medicala, potential relevante pentru dezvoltarea ghidului. Daca
a aparut o asemenea relatie in timpul redactarii ghidului, a
fost anuntata in scris. Participarea fiecarui membru va fi
revizuita. Aceste declaratii sunt analizate de Grupul de Lucru
respectiv, raportate oral membrilor la fiecare intalnire, si actualizate
pe parcurs. Pentru informatii asupra metodologiei folosite la producerea
ghidului, inclusiv privind relatiile cu industria medicala, se pot
consulta siteurile ACC, AHA si ESC (https://www.acc. org/clinical/manual/manual_introltr.htm,
https://circ.aha
journals.org/manual, https://www.escardio.org/knowle dge/guidelines/Rules,
respectiv) si Anexele 1 si 2.
Acest
ghid de practica au scopul de a ajuta personalul medical in luarea
deciziilor clinice prin descrierea spectrului de abordari general
acceptabile a diagnosticului si managementului bolilor. Se incearca
definirea practicilor adecvate celor mai multi pacienti, in majoritatea
circumstantelor. Reflecta consensul opiniilor expertilor
dupa parcurgerea dovezilor stiintifice actuale si
urmaresc imbunatatirea ingrijirii bolnavilor. Daca
acest ghid este folosit ca baza pentru decizii economice, scopul final
este calitatea ingrijirii si satisfacerea intereselor pacientului.
Decizia ultima privind un anumit pacient trebuie luata de medicul
curant si de pacient, in contextul situatiei particulare a acelui
pacient. Exista situatii cand o deviere de la prezentele
recomandari poate fi corecta.
Acest
ghid va fi reanalizat anual de catre Grupul de Lucru ACC/AHA al Ghidurilor
de Practica si Comitetul ESC pentru Ghiduri de
Practica, si este considerat actual pana la updatare, revizuire
sau retragere. Rezumatul si recomandarile sunt publicate in
numarul din 5 septembrie 2006 in Journal of the American College of
Cardiology, 5 septembrie 2006 in Circulation si 17 septembrie 2006 in
European Heart Journal. Textul complet este publicat electronic in
aceleasi numere din Journal of the American College of Cardiology si
Circulation si in septembrie 2006 in Europace, ca si postat pe
siteurile ACC (www.acc.org), AHA (www.americanheart.org) si ESC (www.escardio.org Copii ale rezumatului si textului
complet sunt disponibile la cele trei organizatii.
Sidney C. Smith, Jr., MD, FACC,
FAHA, FESC,
Presedinte, Grupul de Lucru
ACC/AHA al Ghidurilor de Practica
Silvia G. Priori, MD, PhD, FESC,
Presedinte, Comitetul ESC
pentru Ghiduri de Practica
1.
Introducere
Exista
deja cateva ghiduri excelente despre tratamentul pacientilor cu aritmii
ventriculare (Tabel 1). Scopul acestui document este de a actualiza si
combina precedentele recomandari intr-o forma unica,
acceptata de marile societati de cardiologie din Statele Unite
si Europa. Am incercat sa producem un document usor de
urmarit, nu un manual, care sa fie folositor specific pentru localizarea
recomandarilor de evaluare si tratament al pacientilor cu risc
sau cu aritmii ventriculare. Astfel, sectiunile despre epidemiologie,
mecanisme si substraturi, tablou clinic sunt scurte, pentru acestea
neexistand recomandari. Pentru celelalte sectiuni informatiile
suplimentare sunt minimale, restranse la aspectele relevante din punct de
vedere al recomandarilor.
1.1. Organizarea comitetului
si
analiza dovezilor
Membrii
Comitetului de Redactare au fost selectati in functie de
subspecialitatile cardiovasculare, reprezentarea geografica,
implicarea in lumea academica si practica clinica. Comitetul de
Redactare pentru Managementul Pacientilor cu Aritmii Ventriculare si
Prevenirea Mortii Subite Cardiace a mai inclus membrii ai Grupului de Lucru ACC/AHA pentru
Ghiduri de Practica, Comitetul ESC pentru Ghiduri de
Practica, Board-ului ACC, ESC, ai European Heart Rhythm Association (EHRA)
si Heart Rhythm Society (HRS).
Comitetul a fost condus de A. John Camm, MD, FACC, FAHA,
FESC, si Douglas P. Zipes, MD, MACC, FAHA, FESC. Acest document a fost
reexaminat de catre 2 experti numiti de ACC, 2 numiti de
AHA, 2 reprezentanti ESC, 1 numit de ACC/AHA Task Force on Practice
Guidelines, experti ai EHRA si HRS, si 18 revieweri,
cuprinzand membri ai ACCF Clinical Electrophysiology Committee, AHA
Council on Clinical Cardiology, Electrocardiography, and Arrhythmias, si
AHA Advanced Cardiac Life Support Subcommittee.
Comitetul a studiat exhaustiv publicatiile despre
aritmii ventriculare si moarte subita cardiaca (MSC). Ne-am
limitat la publicatiile in limba engleza, referitoare la
populatia umana, din perioada 1990-2006. Parametrii de cautare
au fost extinsi cand a fost nevoie de citarea datelor mai vechi, sau
daca au existat putine studii in limba engleza. In plus, s-au
cautat informatii tintite despre: mecanisme, substraturi, tablou
clinic, ECG, test de efort, ecocardiografie, imagistica, studiu
electrofiziologic, terapia medicamentoasa (antiaritmica si
non-antiaritmica), dispozitive implantabile sau externe, ablatie,
tehnici chirurgicale, aritmii acute specifice (ex, sindroamecoronariene
acute, insuficienta cardiaca, tahicardie ventriculara
monomorfa sustinuta stabila, torsada varfurilor), patologie
specifica (ex, cardiopatii congenitale, miocardita, disfunctii
endocrine, insuficienta renala), cardiomiopatii, aritmii genetice,
cord structural normal, atleti, varstnici, copii, sex, aritmii iatrogene.
Prezentarea listei complete de cuvinte cheie nu este un scop al acestei sectiuni.
Comitetul a analizat rezultatele cautarii computerizate si a
efectuat cautari manuale suplimentare. Citarile au fost
restranse la lucrarile publicate in jurnale din Idex Medicus.
Datorita importantei studiilor in desfasurare, au fost
citate si abstracte, atunci cand acestea au fost singura informatie
publicata disponibila. Recomandarile finale de indicatie a
unei proceduri diagnostice, tratament sau interventie, referitoare la
pacientii cu aritmii ventriculare si preventia MSC sunt
rezultatul dovezilor si opiniei expertilor. Odata finalizate
recomandarile, au fost stabilite pentru fiecare o Clasa de Recomandare
si un Nivel de dovezi.
Tabelul 1.
Ghiduri de practica si declaratii care se suprapun cu Ghidul
ACC/AHA/ESC
pentru managementul pacientilor cu aritmii ventriculare si
preventia mortii subite cardiace
|
Document
|
Sponsor
|
Citare
|
|
Ghiduri
|
|
|
|
MSC
|
ESC
|
Eur
Heart J 2001;22:1374450
|
|
Sincopa
|
ESC
|
Eur
Heart J 2004;25:205472
|
|
Test de
efort
|
ACC/AHA
|
Circulation 2002;106:188392
|
|
Pace-makeri
si dispozitive antiaritmice
|
ACC/AHA/NASPE
|
Circulation 2002;106:214561
|
|
Ecocardiografie
|
ACC/AHA
|
J Am Coll Cardiol 2003;42:95470
|
|
Tahicardii supraventriculare
|
ACC/AHA/ESC
|
Eur Heart J 2003;24:185797 J Am
Coll Cardiol 2003;42:1493531
|
|
MSC Update
|
ESC
|
Eur Heart J 2003;24:135
|
|
Boli cardiace congenitale
|
ESC
|
Eur Heart J 2003;24:103584
|
|
Ghidul European de preventie
a bolilor cardiovasculare
|
ESC
|
Eur J Cardiovasc Prev Rehab
2003;10 Suppl 1:S178
|
|
Endocardita
infectioasa
|
ESC
|
Eur Heart J 2004;25:26776
|
|
Boli ale pericardului
|
ESC
|
Eur Heart J 2004;25:587610
|
|
Hipertensiune arterial pulmonara
|
ESC
|
Eur Heart J 2004;25:224378
|
|
Folosirea DAE in Europa
|
ESC/ERC
|
Eur Heart J 2004;25:43745
|
|
Infarct miocardic cu
supradenivelare de ST
|
ACC/AHA
|
J Am Coll Cardiol 2004;44:e1211
|
|
Insuficienta cardiac
cronica
|
ACC/AHA
|
J Am Coll Cardiol 2005;46:e182
|
|
Insuficienta cardiac
cronica
|
ESC
|
Eur Heart J 2005;26:111540
|
|
RCP si ingrijirea cardiac de
urgenta
|
AHA/ILCOR
|
Circulation 2005;112:IV-1203
|
|
Resuscitare
|
ERC
|
Resuscitation 2005;67 Suppl:53986
|
|
Valvulopatii
|
ACC/AHA
|
J Am Coll Cardiol 2006;48:e1e148
|
|
Declaratii
|
|
|
|
Studii electrofiziologice,
ablatie, cardioversie
|
ACC/AHA
|
J Am Coll Cardiol 2000;36:172536
|
|
Cardiomiopatie hipertrofica
|
ACC/ESC
|
Eur Heart J 2003;24:196591 J Am
Coll Cardiol 2003;42:1687713
|
|
Boli
cardiovasculare in timpul sarcinii
|
ESC
|
Eur Heart J 2003;24:76181
|
|
Activitate
fizica si sporturi recreationale pentru pacientii tineri
cu boli cardiovasculare genetice
|
AHA
|
Circulation 2004;109:280716
|
|
Conferinta
36 Bethesda: Recomandari pentru sportivii de performanta cu
boli cardiovasculare
|
ACC
|
J Am Coll Cardiol 2005;45:131875
|
|
Ghidurile
ACC, AHA si ESC sunt disponibile la www.acc.org, www.americanheart.org,
si www.escardio.org,
respectiv.
ACC, American College of Cardiology; AHA, American Heart Association; RCP, resuscitare
cardiopulmonara; ERC, European
Resuscitation Council; ESC, European
Society of Cardiology; ILCOR, International
Liaison Committee on Resuscitation; NASPE, Heart Rhythm Society (cunoscuta anterior ca North American Society for Pacing and
Electrophysiology); MSC, moarte subita cardiaca.
|
Clasa de Recomandare si Nivelul de
Dovezi sunt exprimate in formatul ACC/AHA/ESC, dupa cum urmeaza:
Clasificarea
recomandarilor
Clasa I
Conditii
pentru care exista dovezi si/sau acord general ca o anumita
procedura sau un tratament sunt benefice, utile si eficiente.
Clasa II
Conditii pentru care exista dovezi
contradictorii si/sau opinii divergente despre utilitatea/eficienta
unei proceduri sau tratament.
Clasa IIa
Dovezile/opiniile sunt in favoarea utilitatii/
eficacitatii.
Clasa IIb
Utilitatea/eficacitatea
este mai putin sustinuta prin dovezi/opinii.
Clasa III
Conditii
pentru care exista dovezi si/sau acord general ca o anumita
procedura/tratament nu este utila/eficienta si in unele
cazuri poate fi chiar daunatoare.
Nivelul de dovezi
Nivel
de dovezi A: Date care deriva din multiple trialuri clinice randomizate
sau meta-analize.
Nivel
de dovezi B: Date care rezulta dintr-un singur trial randomizat sau studii
nerandomizate.
Nivel
de dovezi C: Consensul expertilor, studii de cazuri clinice sau standardul
de sanatate.
Schema
de clasificare a recomandarilor si nivelului de dovezi sunt
prezentate in Tabelul 2, care ilustreaza si cum sistemul de gradare
ofera o estimare a marimii si gradului de certitudine al
efectului terapeutic.
Recomandarile care privesc terapia au
luat in considerare:
Tipul
terapiei aplicate (cardioverter-defibrilator implantabil [ICD], medicamente antiaritmice, metode
chirurgicale, alte masuri terapeutice).
Momentul
aplicarii terapiei (preventie primara pentru cei care sunt la
risc dar care nu au avut inca aritmii ventriculare amenintatoare
de viata sau un episod de moarte subita, sau preventie
secundara pentru cei care au avut deja un asemenea eveniment aritmic).
Scopul
terapiei (sustinerea vietii sau ameliorarea
simptomelor/imbunatatirea calitatii vietii).
Etiologia
substratului aritmiei (boala coronariana, cardiomiopatie sau
altele).
Statusul
functional al pacientului (clasa functionala NYHA)
Functia
ventriculului stang (fractia de ejectie [FEVS]).
Tipul
aritmiei (ex: tahicardie ventriculara monomorfa, tahicardie
ventriculara polimorfa, fibrilatie ventriculara [FV]).
Nu toate
combinatiile terapeutice sunt relevante clinic, multe nu au o baza
de dovezi si probabil nu vor avea nici in viitor datorita lipsei
relevantei clinice sau raritatii relative a conditiilor
implicate. In multe cazuri valoarea probabila a terapiei poate fi
rezonabil dedusa din raspunsul grupurilor similare de pacienti
la terapii specifice.
Tabelul 2.
Aplicarea Claselor de Recomandari si a Nivelului de Dovezi
|
Marimea efectului terapeutic
|
|
Estimarea certitudinii (preciziei) efectulului terapeutic
|
|
Clasa I
Beneficiu >>> Risc
Procedura tratamentul
TREBUIE aplicata/ administrat
|
Clasa IIa
Beneficiu >> Risc
Sunt necesare studii aditionale
cu obiective tintite
ESTE REZONABIL ca
procedura sa fie facuta tratamentul sa fie administrat
|
Clasa IIb
Beneficiu > Risc
Sunt necesare studii aditionale cu obiective mai largi; Datele din
Registre pot fi utile
Procedura tratamentul
poate fi LUAT IN CONSIDERARE
|
Clasa III
Beneficiu < Risc
Nu sunt necesare studii aditionale
Procedura tratamentul
NU trebuie aplicata administrat, NU SUNT UTILE SAU POT FI
DAUNATOARE
|
Nivel A
Au fost evaluate multiple
grupuri populationale cu risc (3-5)a
Efect cosistent ca sens
si magnitudine
|
Procedura tratamentul sunt utile eficiente
Exista suficiente dovezi din trialuri randomizate multiple sau
metaanalize
|
Recomandari in favoarea eficientei/utilitatii procedurii/tratamentului
Unele dovezi divergente din trialuri randomizate multiple sau metaanalize
|
Eficacitate/utilitate mai
putin clare
Dovezi puternic divergente din trialuri randomizate multiple sau metaanalize
|
Procedura/tratamentul nu sunt utile eficiente si pot fi daunatoare
Exista suficiente dovezi din trialuri randomizate multiple sau
metaanalize
|
Nivel B
Au fost evaluate putine grupuri populationale cu risc (2-3)
a
|
Procedura tratamentul sunt utile eficiente
Dovezi limitate,
dintr-un studiu randomizat sau studii nerandomizate
|
Recomandari in favoarea eficientei/utilitatii procedurii/tratamentului
Unele dovezi divergente dintr-un studiu randomizat sau studii nerandomizate
|
Eficacitate/utilitate mai
putin clare
Dovezi puternic divergente dintr-un studiu randomizat sau studii nerandomizate
|
Procedura/tratamentul nu sunt utile eficiente si pot fi daunatoare
Dovezi limitate,
dintr-un studiu randomizat sau studii nerandomizate
|
|
Nivel C
Au fost evaluate foarte putine grupuri populationale cu risc
(1-2) a
|
Procedura tratamentul sunt utile eficiente
Opinia expertilor, studii de caz sau standarde de sanatate
|
Recomandari in favoarea eficientei/utilitatii procedurii/tratamentului
Opinii divergente ale expertilor, studii
de caz sau standarde de sanatate
|
Eficacitate/utilitate mai
putin clare
Opinii divergente ale expertilor, studii de caz sau standarde de
sanatate
|
Procedura/tratamentul nu sunt utile eficiente si pot fi daunatoare
Opinii divergente ale expertilor, studii de caz sau standarde de
sanatate
|
|
a Date din trialuri sau registre asupra
utilitatii/eficacitatii
la diferite subpopulatii, in functie de sex, varsta,
prezenta diabetului zaharat, antecedentele de IM, insuficienta
cardiaca, tratamentul cu aspirina. O recomandare cu nivel de dovezi B sau C nu implica faptul
ca recomandarea ar fi mai slaba. Multe probleme clinice discutate in
ghid nu fac obiectul trialurilor. Chiar daca nu exista trialuri
randomizate, poate exista un consens clar asupra utilitatii sau
eficacitatii unui tratament.
1.2. Recomandarile din
ghidurile actuale privind implantarea profilactica a ICD
Update-ul Ghidului ACC/AHA/NASPE din 2002 referitor la implantarea de
pace-makere si dispozitive antiaritmice,1 Ghidul ACC AHA 2004 de management al
pacientilor cu infarct miocardic cu supradenivelare de ST, 2 ghidurile
ESC de preventie a mortii subite cardiace din 2001 si 2003,3,4
ghidul ESC 2005 de diagnostic si tratament al insuficientei
cardiace cronice5a si
update-ul ghidului ACC/AHA
2005 pentru diagnosticul si managementul insuficientei cardiace
cronice la adulti6 includ un numar mare de recomandari
privind terapia cu defibrilator implantabil care merita atentie.
Recomandarile pentru implantarea profilactica a
ICD bazata pe fractia de ejectie au fost inconsecvente
datorita faptului ca investigatorii au ales valori diferite ale FE la
inrolarea in trialuri, valorile medii ale FE in aceste trialuri au fost
substantial mai mici decat valoarea limita pentru inrolare iar
analiza subgrupurilor pe baza fractiei de ejectie nu a fost
consecventa din punct de vedere al implicatiilor clinice. De aceea au
rezultat diferente semnificative intre ghiduri. Cu toate acestea nu
exista nici un trial care sa fi randomizat pacienti cu valori
intermediare ale FE. De exemplu, nu exista nici un trial care sa fi
studiat specific pacienti cu FEVS intre 31 si 35%, si
totusi au fost facute recomandari pentru acesti
pacienti pe baza datelor din trialuri care au inclus pacienti cu FEVS
<30%, din alte studii pe pacienti cu FEVS <35% si
dintr-un trial care a cuprins pacienti cu FEVS <40%. Recunoscand
aceste inconsecvente, Comitetul de Redactare a decis sa formuleze
recomandarile astfel incat sa poata fi aplicate la pacienti
cu fractia de ejectie mai mica sau egala cu un set de
valori. Clasa de recomandari cea mai inalta a fost apoi
obtinuta din toate trialurile care au inclus pacienti cu FE
intre aceste limite. Astfel, se reduc conflictele intre ghiduri si se
minimizeaza erorile rezultate din tragerea de concluzii false legat de
grupurile de pacienti nestudiate (Tabel 3).
Este important de mentionat ca expertii
pot da diferite interpretari acelorasi date. Incercarea de omogenizare
a unor trialuri heterogene duce invariabil la obtinerea unor
interpretari diferite. Mai mult, diferentele dintre Statele Unite
si Europa pot modula modul de implementare a recomandarilor.
Ghidurile cuprind recomandari rezultate din dovezile
stiintifice disponibile actual; implementarea acestor
recomandari depinde totusi de diferentele sociale, financiare
si culturale dintre tari.
Tabelul 3.
Inconsecvente intre Ghidul ACC/AHA/ESC pentru managementul pacientilor
cu aritmii ventriculare si preventia mortii subite cardiace
si alte ghiduri ACC/AHA si ESC referitoare la terapia cu ICD privind
preventia primara pentru reducerea mortalitatii totale prin
reducerea MSC
|
|
Ghidul si Clasa de Recomandare cu Nivelul
de Dovezi* pentru fiecare grup
| |
|
2005 ACC/AHA
HF
|
ESC HF
|
2004 ACC/AHA STEMI
|
2002 ACC/AHA/
NASPE PM si ICD
|
Comentariu din Ghidul ACC/AHA/ESC pentru AV si MSC
| |
|
Grupul cuprins in recomandare
| |
|
LVD d/t MI, LVEF <30% NYHA II, III
|
Clasa I;
ND: B
|
Clasa I;
ND: A
|
Clasa IIa;
ND: B
|
Clasa IIa;
ND: B
|
AV-MSC a combinat toate trialurile care au cuprins
pacienti cu LVD d/t MI intr-o singura recomandare, Clasa I; ND: A
| |
|
LVD d/t MI, LVEF 30%-35%, NYHA II, III
|
Clasa IIa;
ND: B
|
Clasa I;
ND: A
|
N/A
|
N/A
| |
|
LVD d/t
MI, LVEF 30%-40%, NSVT, SEFpozitiv
|
N/A
|
N/A
|
Clasa I;
ND: B
|
Clasa IIb;
ND: B
| |
|
LVD d/t MI, LVEF <30%, NYHA I
|
Clasa IIa;
ND: B
|
N/A
|
N/A
|
N/A
|
AV-MSC a marit limita LVEF
la 30%-35% sau mai puti pentru pacientii cu
LVD
d/t MI si NYHA I intr-o singura recomandare,
Clasa IIa; ND: B
| |
|
LVD d/t MI, LVEF 31%-35% sau mai putin, NYHA I
|
N/A
|
N/A
|
N/A
|
N/A
| |
|
NICM, LVEF
<30%, NYHA II, III
|
Clasa I;
ND: B
|
Clasa I;
ND: A
|
N/A
|
N/A
|
AV-MSC a combinat toate trialurile cu NICM, NYHA II,
III intr-o singura recomandare,
Clasa I;
ND: B
| |
|
NICM, LVEF
30%-35%, NYHA II, III
|
Clasa IIa;
ND: B
|
Clasa I;
ND: A
|
N/A
|
N/A
| |
|
NICM, LVEF
<
NYHA I
|
Clasa IIb;
ND: C
|
N/A
|
N/A
|
N/A
|
AV-MSC a marit limita LVEF
la 30%-35% sau mai putin pentru pacientii cu
NICM si NYHA I intr-o singura recomandare,
Clasa IIb; ND: B
| |
|
NICM, LVEF 31%-35% sau mai putin, NYHA I
|
N/A
|
N/A
|
N/A
|
N/A
| |
|
*Pentru
explicarea claselor de recomandari si a nivelului de dovezi vezi
Tabel 2. Pentru discutii suplimentare vezi Introducerea.
ACC/AHA HF, ACC/AHA 2005 Guideline Update for the Diagnosis and
Management of Chronic Heart Failure in the Adult6;
ACC/AHA/NASPE PM si ICD, ACC/AHA/NASPE 2002 Guidelines Update for Implantation of Cardiac Pacemakers and
Antiarrhythmia Devices1; ACC/AHA STEMI, ACC/AHA 2004 Guidelines for the Management of Patients
With ST-Elevation Myocardial Infarction2; SEF, studio
electrofiziologicl; ESC HF, ESC 2005 Guidelines
for the Diagnosis and Treatment of Chronic Heart Failure5; ND,
nivel de dovezi; LVD d/t MI, disfuntie ventriculara stanga
dupa infarct miocardic; LVEF, fractia de ejectie a
ventriculului stang; N/A, populatii neincluse; NICM, cardiomiopatie
nonischemica; NSVT, tahicardie ventriculara nesustinuta;
NYHA, clasa functionala New
York Heart Association; MSC, moarte subita cardiac; AV, aritmii
ventriculare.
| |
1.3.
Clasificarea aritmiilor ventriculare si a mortii subite cardiace
Tabelul
cu clasificari are rol de orientare si introducere in ghid (Tabel
4).
Tabelul 4.
Clasificarea aritmiilor ventriculare
|
Clasificarea
dupa tabloul clinic
|
Bibliografie
|
|
Stabile hemodinamic
|
Asimptomatice
|
Absenta
simptomelor care ar putea fi produse de o aritmie.
|
|
|
Simptome minime, ex,
palpitatii
|
Pacientul
descrie palpitatii in piet, gat, astfel:
Batai
cardiace rapide
Perceperea
neplacuta a batailor
Simtirea
pauzelor
|
|
|
Instabile
hemodinamic
|
Presincopa
|
Pacientul
descrie presincopa ca:
Ameteala
Senzatie
de cap gol
Senzatie
de lesin
Pierdere
|
|
|
Sincopa
|
Pierdere
brusca a constientei si a tonusului postural,
nelegata de anestezie, cu recuperare spontana, relatata de
pacient sau martori. Poate apare in decubit.
|
|
|
Moarte subita
|
Moarte
prin stop circulator neasteptat, datorat de obicei unei aritmii,
aparuta in prima ora de la debutul simptomelor.
|
(7a)
|
|
Stop cardiac subit
|
Moarte
prin stop circulator neasteptat, datorat de obicei unei aritmii,
aparuta in prima ora de la debutul simptomelor, la care
interventia medicala (ex, defibrilare) este eficienta.
|
|
|
Clasificare
electrocardiografica
|
|
|
TV nesustinuta
|
|
Trei
sau mai multe batai successive, oprite spontan in maximum 30 s.
TV
este o aritmie cu trei sau mai multe batai successive, cu originea
in ventricul, cu frecventa mai mare de 100 bpm (lungime a ciclului mai
mica de 600 ms)
|
|
|
Monomorfa
|
TV
nesustinuta cu o singura morfologie QRS.
|
|
|
Polimorfa
|
TV nesustinuta cu
morfologie QRS variabila, cu lungimi de ciclu intre 600 si 180 ms.
|
|
|
TV
sustinuta
|
|
TV cu
durata mai mare de 30 s si/sau care trebuie oprita datorita
compromiterii circulatiei chiar <30 s.
|
|
|
Monomorfa
|
TV
sustinuta cu o morfologie QRS stabila.
|
|
|
Polimorfa
|
TV sustinuta cu
morfologie QRS variabila sau multiforma cu lungime a ciclului intre
600 si 180 ms.
|
|
|
Tahicardie prin reintrare in ramura
|
|
TV
datorata reintrarii care implica sistemul His-Purkinje, de
obicei cu morfologie de BRS; apare de obicei in contextual cardiomiopatiei.
|
|
|
TV
bidirectionala
|
|
TV cu alternanta
bataie-cu-bataie a axului QRS in plan frontal, asociata
frecvent cu toxicitatea digitalica.
|
|
|
Torsada
varfurilor
|
|
TV asociata cu interval
QT/QTc lung, caracterizata electrocardiografic prin rasucirea
varfului complexului QRS in jurul liniei izoelectrice in timpul aritmiei
Tipic,
initiata dupa o secventa de cicluri
scurt-lung-scurt.
Varianta cu
cuplaj scurt, aparuta dupa o secventa de cuplare
normal-scurt.
|
|
|
Flutter
ventricular
|
|
Aritmie ventriculara
regulata (variabilitate a ciclului de 30 ms sau mai putin), cu
frecventa de aproximativ 300 bpm (lungime a ciclului-200 ms), cu aspect
monomorf; fara linie izoelectrica intre complexe QRS
succesive.
|
|
|
Fibrilatia
ventriculara
|
|
Ritm
ventricular rapid, de obicei peste 300 bpm/200 ms (lungime a ciclului de 180
ms sau mai putin), cu variabilitate mare a duratei ciclului, morfologiei
si amplitudinii QRS.
|
|
|
Clasificarea dupa entitatea
patologica
|
|
|
Boala coronariana cronica
Insuficienta cardiaca
Cardiopatii congenitale
Tulburari neurologice
Cord structural normal
Sindromul de moarte subita a nou-nascutului
|
|
|
|
Cardiomiopatii
|
Cardiomiopatia
dilatativa
Cardiomiopatia
hipertrofica
Cardiomiopatia
aritmogena de ventricul drept
|
|
|
BRS,
bloc de ramura stanga; TV, tahicardie ventriculara.
|
|
2.
Epidemiologie
Epidemiologia
aritmiilor ventriculare acopera o plaja larga de descriptori de
risc si aplicatii clinice, de la bataile premature
ventriculare (BPV) si tahicardia ventriculara nesustinuta
(TVNS) la subiecti normali pana la MSC datorata tahiaritmiilor
ventriculare la pacienti cu sau fara boala cardiaca
structurala.9
Pattern-urile
epidemiologice au implicatii care ajuta la
imbunatatirea profilarii riscului in functie de caracteristicile
individuale ale subiectilor si a designului trialurilor clinice.10
Tehnicile epidemiologice includ identificarea factorilor de risc clinici
si a stilului de viata care predispun la dezvoltarea bolii,
masurarea riscului in subgrupuri de pacienti cu boala
instalata si domeniul nou aparut ale epidemiologiei genetice.9,11
2.1. Aritmiile ventriculare
2.1.1.
Bataile premature ventriculare si tahicardia ventriculara
nesustinuta
Formele
izolate sau repetitive de BPV au fost studiate pentru rolul lor in
predictia riscului in cateva circumstante clinice diverse, inclusiv
la subiecti aparent sanatosi comparativ cu cei cu
boala diagnosticata, in evenimente cronice comparativ cu cele
tranzitorii, la subiecti inactivi versus cei supusi stresului fizic.
Implicatiile epidemiologice variaza in fiecare din aceste circumstante.
2.1.1.1. Bataile premature ventriculare in
absenta bolii cardiace
La
indivizii presupusi normali, prevalenta estimata a BPV si
TVNS variaza in functie de tehnica de inregistrare folosita
si sursa de date. BPV au fost inregistrate pe ECG standard la 0,8% din
subiectii dintr-o populatie de militari sanatosi, cu
limite de la 0,5% sub 20 ani si pana la 2,2% la cei peste 50 ani.12
Intr-un
studiu cu barbati de varsta medie cu sau fara
boala cardiaca diagnosticata, monitorizarea timp de 6 ore a
identificat o incidenta de 62% a aritmiilor ventriculare
asimptomatice, mai mult de jumatate fiind BPV izolate.13
Incidenta, frecventa si complexitatea aritmiilor ventriculare au
fost mai mari in prezenta unei boli cardiace cunoscute sau
suspectate ; nu s-a asociat risc de mortalitate la cei fara
boala cardiaca structurala.13,14
In
contrast cu BPV si episoadele de TVNS monomorfa, tahiaritmiile
ventriculare polimorfe in absenta bolii cardiace structurale sunt markeri
de risc.15 Multe episoade de TVNS polimorfa care apar la
indivizi fara anomalii cardiace structurale evidente se
datoreaza anomaliilor la nivel molecular, apar ca urmare a
tulburarilor electrolitice sau sunt efecte adverse ale administrarii
de medicamente.
In
studiul epidemiologic din Tecumseh, Michigan, bataile premature
ventriculare la subiecti cu cord normal nu au avut semnificatie prognostica
sub varsta de 30 ani, dar la cei peste 30 ani, prezenta BPV si a
paselor scurte de TVNS au influentat riscul.16 Studii mai
recente dau informatii contradictorii privind riscul la indivizii asimptomatici.
Intr-un studiu,17 aritmiile ventriculare asimptomatice in
absenta unei boli cardiace identificabile au asociat o crestere
mica a riscului, in timp ce in alt studiu18 nu au modificat
riscul.
In
contrast cu implicarea aparent neutra a BPV aparute in repaus, ca
risc vital, cele care apar la testul de efort, chiar la indivizi aparent
normali, par sa implice un anumit risc in timp. Intr-un studiu,19
BPV si TVNS induse de efort s-au corelat cu cresterea riscului de
mortalitate totala, in timp ce in alt studiu,20 atat BPV
aparute la efort cat si cele din faza de recuperare s-au corelat cu
riscul, semnificatie mai mare avand aritmiile aparute in faza de
recuperare.
Criteriile
de selectie, bazate pe indicatiile testului de efort, se poate
sa fi influentat aceste observatii.21
2.1.1.2. Bataile
premature ventriculare in prezenta bolii cardiace
Prezenta
BPV si a paselor de TVNS la pacienti cu boala cardiaca
structurala contribuie la cresterea riscului de mortalitate,
magnitudinea riscului variind cu natura si gradul bolii subiacente. La
supravietuitorii unui infarct miocardic (IM), activitatea
ventriculara ectopica frecventa si repetitiva,
asociata cu scaderea FE, este predictor de risc crescut de MSC in
urmarirea pe termen lung.21-23 Cele mai multe studii
citeaza un prag al frecventei de 10 BPV/ora si prezenta
formelor repetitive de ectopie ventriculara ca markeri de risc crescut.
Cativa investigatori au considerat ca cel mai puternic predictor,
dintre variatele forme de BPV, ar fi pasele de TVNS.21,22
Specificitatea acestei asocieri este acum pusa la indoiala. Puterea
predictiva a BPV si TVNS pare a fi direct legata de extinderea
bolii cardiace structurale, estimata prin FE si de limitarea
cardiovasculara estimata prin capacitatea functionala.24
Aritmiile
ventriculare in timpul monitorizarii ambulatorii la pacientii cu
insuficienta cardica nu sunt predictori specifici pentru riscul
de MSC.25 Acestia au deja un risc mare datorita bolii de
fond. Supresia aritmiilor ventriculare nu mai este considerata
tinta terapeutica pentru prevenirea mortalitatii la pacientii
postinfarct miocardic sau la cei cu cardiomiopatie non-ischemica.
2.1.2. Tahicardia
ventriculara si fibrilatia ventriculara din sindroamele
coronariene acute
Observatii
asupra pacientilor post-IM26 si supravietuitorilor
stopului cardiac din timpul fazei acute a unui IM transmural27
sugereaza ca tahiaritmiile ventriculare amenintatoare de
viata aparute in primele 24-48 ore post-IM nu asociaza o
crestere a riscului pe termen lung. Un studiu de urmarire la
pacientii cu FV intraspitaliceasca a sugerat un prognostic negativ
pe o perioada de 6 luni de la eveniment,28 dar pacientii
nu au fost selectati specific. FV tardiva in timpul spitalizarii
a fost asociata anterior cu un risc pe termen lung.29 In
contrast, pacientii cu IM fara supradenivelare de segment ST au
un risc crescut de MSC pe termen lung,30 fapt datorat probabil in
parte unei predispozitii persistente pentru tahiaritmii ventriculare.31
Asemenea pacienti au fost in general exclusi din trialurile clinice
cu interventii care aveu drept tinta riscul de moarte
aritmica pe termen lung, datorita riscului absolut mic, dar
ramane neclar daca magnitudinea riscului este modulata de
extinderea afectarii miocardice care apare in timpul evenimentului acut.
Implicatiile
TV si FV aparute in faza acuta a IM asupra riscului pe termen
lung se pot aplica de asemenea si in cazul BPV frecvente si paselor
de TVNS.32 Este important de precizat faptul ca abilitatea
clinicianului de a recunoaste indivizii cu cauze reversibile sau
tranzitorii de tahiaritmii ventriculare este limitata.33
2.2.
Moartea subita cardiaca
2.2.1. Incidenta MSC
Incidenta
geografica a MSC variaza in functie de prevalenta bolii
cardiace ischemice in diferitele regiuni.3 Estimarile pentru
SUA34-38 variaza de la mai putin de 200.000 pana la mai
mult de 450.000 MSC anual, estimarea cea mai des citata fiind de
300.000 350.000 MSC/an. Variatiile rezulta in parte din criteriile de includere
utilizate in studii. In Europa, datele sunt similare,3 cu
variatii geografice semnificative.
Definitiile
date MSC influenteaza puternic datele epidemiologice.40
Proportia de morti naturale datorate MSC este de 13% cand este
folosita limita de o ora de la debutul simptomelor. In contrast, un
studiu populational in Maastrich, Olanda, a raportat ca 18,5% din
toate mortile sunt MSC utilizand limita de 24 ore in definitie.41
Aplicarea acestui de al doilea criteriu creste proportia de
morti naturale incluse in categoria subite dar reduce proportia de
morti naturale subite care se datoreza unei cauze cardiace.40
Aproximativ
50% din decesele din boala coronariana sunt subite si
neasteptate, aparand brusc (instantaneu sau pana la o ora)
dupa o modificare a statusului clinic, cu cateva variatii geografice
in procentul de morti cu substrat coronarian care sunt subite.42
Scaderea mortalitatii prin boala coronariana,
ajustata in functie de varsta, nu implica o scadere a
numarului absolut de morti cardiace sau subite43,44
datorita imbatranirii populatiei si cresterii
prevalentei bolilor cardiace cronice.45
2.2.2.
Subgrupuri populationale si predictia riscului
Trei
factori influenteaza abilitatea de a identifica subiecti si
subgrupuri populationale la risc si evaluarea strategiilor pentru
prevenirea MSC:
numarul absolut si rata
evenimentelor (incidenta) in subgrupurile populationale (Figura 1)
subgrupurile
clinice in care apare MSC
dependenta
de timp a riscului
Incidenta
MSC in SUA este intre 1 si 2 la 1000 locuitori (0,1-0,2%) anual, cu
cateva variatii in functie de sursa de date.
Acest
grup mare populational include subiecti la care MSC apare ca prim
eveniment cat si pe cei la care MSC poate fi prezisa cu o mare
acuratete pentru ca ei sunt inclusi in categoria de risc crescut
(Figura 1). Niveluri mai mari de rezolutie a riscului pot fi
obtinute prin identificarea unor subgrupuri mai specifice. Cu toate
acestea, numarul absolut de morti corespunzatoare devine
progresiv mai mic pe masura ce subgrupurile devin mai centrate,
limitand impactul potential al interventiilor la o fractiune
mult mai mica din populatia totala.10 Cel putin
50% din MSC datorate bolii coronariene apar ca prim eveniment sau in subgrupuri
de pacienti considerate a fi la risc relativ scazut de MSC.43
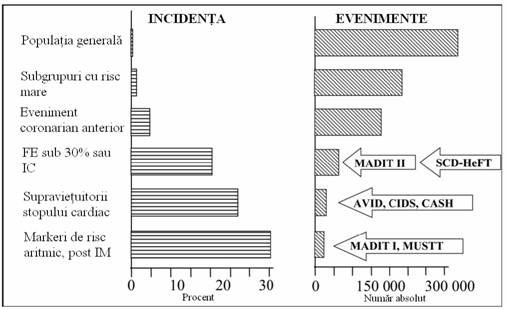
Figura 1. Numarul absolut de evenimente
si rata MSC la un an in populatia generala si in subgrupuri
specifice. Populatia generala se refera al o populatie
neselectata cu varsta <de 35 ani, subgrupul cu risc mare se
refera la cei cu multipli factori de risc pentru un prim eveniment
coronarian.Trialurile care includ subpopulatii specifice sunt aratate
in dreapta figurii. AVID, Antiarrhythmics Versus Implantable Defibrillators;
CASH, Cardiac Arrest Study Hamburg; CIDS, Canadian Implantable Defibrillator
Study; FE, fractia de ejectie; IC, insuficienta cardiaca;
MADIT, Multicenter Automatic Defibrillator Implantation Trial; IM, infarct
miocardic; MUSTT, Multicenter UnSustained Tachycardia Trial; SCD-HeFT, Sudden
Cardiac Death in Heart Failure Trial. Modificat cu acord, dupa Myerburg
RJ, Kessler KM, Castellanos A. SCD. Structure, function, and time-dependence of
risk. Circulation 1992;85:I210.
2.2.3. Riscul dependent de
timp
Riscul
de MSC dupa un eveniment clinic nu este liniar ca functie de timp.39,46
Curbele de supravietuire dupa evenimente cardiovasculare majore, care
identifica atat riscul de mortalitate cardiaca subita si
totala, demonstreaza ca cea mai rapida rata de
actualizare a riscului apare in primele 6-18 luni dupa evenimentul originar.
Curbele cu aceste caracteristici s-au obtinut din date de la
supravietuitorii stopului cardiac din afara spitalului, de la cei
insuficienta cardiaca nou aparuta, angina
instabila si subgrupurile cu risc crescut din pacientii cu IM
recent. In contrast cu patternul cu riscului inerent, curbele de beneficiu din
trialurile controlate pot arata divergente precoce (terapia cu beta
blocante post-IM, clopidogrel in SCA) sau tardive (IEC si statine). Mortalitatea
este maxima in prima luna post-IM la pacienti cu FE <30%.47
2.2.4. Varsta, ereditatea,
sexul si rasa
Incidenta
MSC creste cu varsta,48 paralel cu cresterea legata
de varsta a incidentei totale a deceselor de cauza
coronariana, dar poate avea o relativa scadere in a opta
decada si peste datorita interventiei altor cauze de
moarte. Incidenta este de 100 ori mai mica la adolescenti
si adulti tineri sub 30 ani (1 la 100.000/an) decat la adultii
peste 35 ani.49-51 Proportia deceselor subite cu substrat
coronarian si a celor de orice cauza cardiaca este cea mai mare
in grupele de varsta mai tinere.
S-a
considerat ca factorii ereditari care contribuie la boala cardiaca
ischemica actioneaza nespecific in aparitia MSC.
Totusi, cateva studii au identificat mutatii si polimorfisme
relevante de-a lungul multiplelor trepte ale evolutiei de la
ateroscleroza la destabilizarea placii, tromboza si
aritmogeneza, fiecare din acestia fiind asociati cu risc de
evenimente coronariene.52-55 Integrarea acestor markeri poate
furniza in viitor o putere predictiva mai mare pentru riscul individual.56
In plus, doua studii populationale sugereaza ca MSC, ca expresie
a bolii coronariene, prezinta o aglomerare familiala.57,58
Exista o larga preponderenta a MSC la barbati
comparativ cu femeile la populatia tanara si cea de varsta
medie, datorita protectiei hormonale impotriva aterosclerozei
coronariene la femei pre-menopauza. Deoarece riscul de evenimente
coronariene creste post-menopauza, riscul de MSC creste
proportional. Chiar daca riscul total este mult mai scazut la
femeile tinere, factorii clasici de risc coronarian raman predictori
pentru un eveniment ischemic.59,61-63
Studii
care au comparat existenta unor diferente rasiale privind riscul de
MSC din cardiopatia ischemica la populatia alba si cea
african-americana au avut rezultate contradictorii si neconcludente.
Cu toate acestea, unele studii au demonstrat cresterea riscului de stop
cardiac si MSC la african-americani comparativ cu cei albi.61,64
Rata de MSC la populatia hispanica a fost mai mica. 61
2.2.5. Profiluri de risc
si moartea subita cardiaca
Conturarea
profilului biologic si de comportament cu risc pentru boala
coronariana folosind factorii conventionali de risc ai
aterogenezei,65 este utila pentru identificarea nivelurilor de
risc populational, dar are valoare limitata in identificarea
individuala a pacientilor cu risc de MSC. Analizele multivariate ale
unor factori selectati de risc aterogen au determinat ca aproximativ
jumatate din MSC au loc in 10% din populatie, in grupul cu risc
maxim. Astfel, riscul cumulativ asociat factorilor conventionali
implicati in ateroscleroza coronariana depaseste
suma aritmetica a riscurilor individuale.65 Comparand factorii
de risc la victimele MSC si la populatia cu boala
coronariana aparenta clinic nu se obtin informatii utile.
In plus, unele patternuri angiografice si hemodinamice discrimineaza
intre riscul de moarte subita de cel de moarte non-subita numai in
anumite conditii.66
Markeri
de risc care depasesc conceptia clasica a aterogenezei ca
depunere de lipide, spre o pato-biologie mai complexa, sunt acum
identificati, concentrandu-se primar pe mecanismele destabilizarii
placii. Markeri ai inflamatiei, ca proteina C-reactiva si
alti indicatori de inflamatie si destabilizare,67 au
intrat in uz, oferind informatii potential utile, pe langa
markerii conventionali.68,69 Agregarea familiala a MSC ca
manifestare specifica a bolii ischemice57,58 poate duce la
identificarea unor anomalii genetice specifice care predispun la MSC.52-54,70
Hipertensiunea
este un factor consacrat de risc coronarian, si mai nou factor de risc
pentru MSC.71 Semnele de hipertrofie ventriculara stanga
pe ECG si dovezile ecocardiografice de HVS se asociaza cu moartea
cardiaca subita si neasteptata. Tulburarile de
conducere intraventriculara ca Blocul de Ramura Stanga (BRS)
asociaza de asemenea un numar disproportionat de MSC.72,73
Exista
de asemenea asocieri semnificative ale fumatului, obezitatii,
diabetului si stilului de viata cu moartea subita
cardiaca. Studiul Framingham demonstreaza ca fumatorii au
un risc de MSC de 2-3 ori mai mare; fumatul este unul din putinii factori
de risc la care proportia de morti subite la pacientii cu
boala coronariana creste in relatie cu factorul de risc.72
In plus, intr-un studiu care a cuprins 310 supravietuitori ai
stopului cardiac extra-spitalicesc, rata de recurenta la 3 ani a
fost de 27% la cei care au continuat sa fumeze si 19% la cei care au
oprit fumatul.74 Obezitatea este un al doilea factor care pare
sa influenteze proportia de decese subite cu substrat ischemic.72
Relatia
intre nivelul de activitate fizica si MSC a fost studiata, cu
rezultate variabile.75 O frecventa cardiaca de repaus
mare, si putin modificata la efort si in perioada de
recuperare, este un factor de risc pentru MSC. Date epidemiologice au sugerat o
relatie intre sedentarism si riscul de deces prin boala coronariana.
Studiul Framingham a indicat totusi o relatie nesemnificativa
intre nivelul redus de activitate fizica si incidenta MSC, dar
cu o proportie mai mare de morti subite aparute la efort.
72 Asocierea MSC cu efortul acut are un risc relativ de 17 ori mai mare
la toata populatia (activa sau inactiva). Pentru cei
inactivi riscul relativ a fost 74.76 Exercitiul fizic regulat
atenueaza riscul.76,77 Aceste date arata ca in timp
ce riscul de stop cardiac este mai mare in timpul efortului intens (mai ales la
indivizii sedentari), exercitiul fizic regulat scade riscul de stop
cardiac, atat la efort cat si in repaus.78
Magnitudinea
recentelor modificari ale stilului de viata in ce priveste
sanatatea, locul de munca, locuinta, familia, factorii
individuali si sociali, au fost legate de IM si MSC.79-82
Exista
o relatie intre cresterile semnificative ale scorului de modificare
a vietii in perioada de 6 luni inaintea unui eveniment coronarian,
aceasta este mai evidenta la victimele MSC. Dupa ajustarea in
functie de alti factori prognostici majori, MSC si mortalitatea
totala cresc cu stresul social si economic,83 si
influenta asupra stilului de viata a fost propusa ca o
parte a strategiei de reducere a riscului de MSC in boala coronariana.84
Stresul psihosocial acut se asociaza cu evenimentele
cardiovasculare, inclusiv cu MSC.85,86 Riscul pare sa se
aglomereze la momentul stresului, la indivizi cu risc preexistent, stresorul
grabind evenimentul.85
A fost
sugerata si posibilitatea rupturii placii coronariene
indusa de stresul fizic.87
3. Mecanisme
si substraturi
3.1. Substratul aritmiilor
ventriculare
Substratul
MSC depinde de boala cardiaca de baza, daca exista, si
variaza de la cardiomiopatii avansate pana la lipsa unor
modificari structurale evidente. Majoritatea studiilor sugereaza
ca trei sferturi din pacientii care decedeaza prin MSC au
boala coronariana. Ateroscleroza coronariana extinsa este
in general prezenta, o mare parte din pacienti avand trei sau patru
vase interesate. La examenul anatomo-patologic au fost gasite
modificari morfologice ale placii coronariene, ca tromboza sau
ruptura placii, sau amandoua, la mai mult de 50% din cazurile de
moarte subita ischemica. Pacientii care au cicartrice
miocardica, dar nu au IM acut, au leziuni coronariene active in 50% din
cazuri.88 Eroziunea placilor bogate in proteoglicani si
celule musculare netede, lipsite de un miez superficial de lipide, sau ruptura
placii aterosclerotice, este frecvent intalnita.89 Ruptura
placii aterosclerotice pare mai frecventa la femeile in varsta.90
Totusi, aceste modificari anatomice nu sunt reprezentate de factori
clinici specifici de risc diferiti de cei care identifica
pacientii cu boala coronariana in general.
In mod
evident substratul este diferit in functie de natura bolii cardiace de
baza. Alte boli care predispun la MSC sunt reprezentate de: cardiomiopatia
hipertrofica, cardiomiopatia dilatativa, cardiomiopatia de ventricul
drept, anomaliile congenitale (in special anomaliile arterelor coronare),
spasmul coronarian si altele mai putin frecvente (vezi si
Sectiunea 2).44,46,91 Obezitatea, hipertensiunea,
dislipidemia, diabetul zaharat sunt factori de risc importanti.92-95 Anomaliile
mostenite intalnite in cardiomiopatia de ventricul drept si CMH
reprezinta substratul major la cei cu moarte subita la varste tinere
(pre-coronarieni).96-98 Riscul cumulativ de MSC a fost estimat intre
15-20% la adultii cu stenoza aortica, cu un risc mai mare la
pacientii simptomatici si un risc egal sau mai mic de 5% la
asimptomatici.99 Prolapsul de valva mitrala este de obicei
benign si legatura sa cu MSC nu a fost niciodata
demonstrata.3 Rata MSC la pacientii cu sindrom
Wolff-Parkinson-White (WPW) a fost de 0,15% in special la cei care au dezvoltat
fibrilatie atriala (FA) cu raspuns ventricular rapid care poate
degenera in fibrilatie ventriculara.100,101
Factori
genetici influenteaza riscul de MSC in contextul bolii coronariene,
si probabil si in altele.3,55,102 Studiul prospectiv Paris
I, analizand mai mult de 7000 de barbati urmariti in medie
timp de 23 ani, a aratat ca istoricul familial de MSC a crescut
riscul relativ la descendenti la 1,8, fara sa creasca
riscul pentru infarct miocardic. Cand amandoi parintii au avut MSC riscul
relativ la descendenti a fost 9,4.58 Un studiu retrospectiv al
supravietuitorilor stopului cardiac, din King County, Washington, a
raportat deasemenea ca istoricul familial este un factor de risc
semnificativ, independent, cu un risc relativ de 1,57.57
Influentele genetice pot interveni prin multiple mecanisme, care nu sunt
neaparat exclusive: prin modularea substratului fix, aterotrombozei, propagarea
impulsului electric, reglarea si controlul neural.
In 5-10%
din cazuri, MSC apare in absenta bolii coronariene sau a
cardiomiopatiilor. Exista un grup de anomalii mostenite, precum
sindromul de QT lung (LQTS), sindromul de QT scurt (SQTS), sindromul Brugada
si TV catecolaminergica, care pot precipita MSC in absenta unor
modificari structurale evidente.103-105 Anomaliile canalelor de
sodiu si potasiu, ankyrinei B si receptorului ryanodinic de la
nivelul reticulului sarcoplasmic care este responsabil pentru eliberarea
calciului necesar contractiei miocardice, pot afecta procesele electrice
normale cu aparitia aritmiilor venticulare grave. Este important sa
subliniem ca anumiti indivizi cu anomalii mostenite pot sa
nu aiba nici un fel de simptom pina la aparitia unui factor
declansator extern. De exemplu, modularea autonomica asociata cu
anumite tipuri de activitate, precum si medicamentele care afecteaza
repolarizarea cardiaca, pot sa transforme o anomalie genetica
subclinica in moarte subita cardiaca. Este foarte probabil ca
alte cauze genetice de MSC sa fie descoperite in viitor.56
Dintre
factorii genetici cele mai frecvente sunt polimorfismele ADN, care pot fi prezente in
proportie mare la nivelul populatiei si pot determina
susceptibilitate pentru MSC. Polimorfismele mononucleotid (SNP - single
nucleotide polymorphism) sunt variante de ADN care pot fi asociate cu
modificari functionale. De exemplu, un polimorfism identificat la
nivelul receptorilor adrenergici alfa
2b este asociat cu o crestere a riscului de infarct miocardic si MSC.106
Asemenea studii necesita insa validare inainte de a intra in
practica clinica. Totusi, pentru ca milioane de polimorfisme
mononucleotid sunt prezente la nivelul ADN-ului fiecarui individ, o
combinatie specifica de polimorfisme in gene diferite,
interactionand cu un trigger sau un substrat specific, poate fi
necesara pentru a determina un risc de moarte subita cardiaca.56
3.2. Mecanismele mortii
subite cardiace
Aritmia
cea mai frecvent inregistrata in timpul MSC este fibrilatia
ventriculara (FV). Studiile anterioare au aratat ca 75-80% din cazurile de MSC
se produc prin acest mecanism, iar 15-20% din cazuri sunt atribuite
bradiaritmiilor incluzand blocul atriventricular avansat si asistola.107
Bayes de Luna si colab.108 au aratat ca din 157 de
pacienti cu MSC in timpul monitorizarii Holter 62,4% au avut FV, 16,5% au avut bradiaritmii,
12,7% au avut torsada varfurilor si 8,3% au avut TV primara.
Incidenta reala a bradiaritmiilor nu este clara pentru ca
un ritm inceput ca FV poate sa apara ca asistola atunci cand
este inregistrat primul ECG. Cu toate acestea, un studiu raportat de Cobb
si colab.37 sugereaza ca FV explica o
proportie mult mai mica de evenimente decat se credea anterior.
Blocul atrioventricular avansat sau bradicardia severa pot cauza FV. Este
dificil de identificat precis mecanismul sau mecanismele electrofiziologice
responsabile de MSC. Motivul este acela ca mecanismele pot fi
multifactoriale si este destul de probabil sa fie diferite in
functie de patologia cardiaca, iar un ritm poate sa inceapa
printr-un mecanism si sa se perpetueze prin altul. Este de asemenea
important sa amintim ca in timp ce multe studii au investigat mecanismele
electrofiziologice responsabile pentru initierea si perpetuarea TV
si FV, nu s-a demonstrat clar ca un agent antiaritmic din clasa I sau
III109 ar reduce mortalitatea totala sau subita la
pacientii cu risc de MSC.7a,109 De fapt, tocmai medicamentele
fara efecte elctrofiziologice directe la nivelul fibrelor miocardice
si tesutului specializat de conducere s-au dovedit eficiente in preventia
MSC. Aceste medicamente includ beta blocantele, IECA, blocantii
receptorilor de angiotensina, hipolipemiantele, spironolactona si
agentii fibrinolitici si antitrombotici; anumite date sugereaza
un efect protector al acizilor grasi n-3,110 desi acest
lucru ramane sa fie confirmat111 (vezi Sectiunea
6.4).
Deoarece
MSC este in cea mai mare parte rezultatul tahiaritmiilor ventriculare, aceste
medicamente probabil ca actioneaza la nivelul proceselor
fundamentale biochimice, ischemice,
fibrotice sau altele care sunt la baza aparitiei si mentinerii
aritmiei. Astfel, FV poate fi considerata o cale comuna finala
evolutiei cordului instabil electric. Mecanismele fundamentale pentru
oprirea cardiaca includ disociatia electromecanica, asistola,
blocul atriventricular si FV (cea mai frecventa). Probabil ca
aceste medicamente actioneaza asupra triggerilor instabilitatii
electrice. In timp ce indiscutabil este necesar sa continuam
investigatiile electrofiziologice asupra tahiaritmiilor ventriculare,
sunt necesare mai multe studii cu medicamentele care influenteaza
acesti triggeri, deoarece, la momentul actual cel putin, par a fi
motivul care face ca un individ asimptomatic, aparent stabil, sa dezvolte
MSC la o anumita ora dintr-o anumita zi. Probabil ca unul
sau mai multi factori, posibil pasageri, interactioneaza cu un
substrat fix precipitand aritmia. Exista o lista lunga de
factori posibili care include efortul fizic, ischemia tranzitorie,
modificarile de pH si electrolitice, inflamatia, hipoxia, stretch-ul, modificarile la nivelul
canalelor ionice, factori neuroendocrini, medicamentele si altele, toate
fiind capabile sa moduleze conducerea la nivel cardiac intr-un mod pe
care nu il intelegem in totalitate. Deasemenea pot sa apara
si modificari permanente, ca de exemplu ruptura placii
mentionata anterior.112
4. Tabloul
clinic la pacientilor cu aritmii ventriculare si moarte subita
cardiaca
Aritmiile
ventriculare pot sa apara la indivizi cu sau fara o
tulburare cardiaca. Exista o mare legatura intre tabloul
clinic (Tabelul 5) si severitatea sau tipul de bola cardiaca de
baza. De exemplu, tahicardiile ventriculare bine tolerate pot sa
apara la pacientii cu infarct miocardic in antecedente si
disfunctie ventriculara. Prognosticul si managementul
pacientilor este individualizat in functie de simptomatologia si
severitatea bolii cardiace de baza, la care se aduga tabloul clinic.
Tabelul 5. Tabloul clinic al
pacientilor cu aritmii ventriculare si MSC
|
Pacienti asimptomatici cu sau
fara modificari electrocardiografice
Pacienti cu
simptome datorate probabil aritmiilor ventriculare
o palpitatii
o dispnee
o durere precordiala
o sincopa sau presincopa
Tahicardie
ventriculara stabila hemodinamic
Tahicardie
ventriculara instabila hemodinamic
Oprirea cardiaca
o asistola (oprire sinusala, bloc
atrioventricular)
o tahicardie ventriculara
o fibrilatie ventriculara
o activitate electrica fara puls
|
4.1. Pacienti
asimptomatici
Aritmiile
ventriculare pot fi detectate intamplator in timpul unei monitorizari
ECG sau la examenul clinic. Deasemenea aritmiile ventrticulare pot fi
identificate in timpul investigatiilor pentru stabilirea prognosticului la
pacientii cu bola cardaica cunoscuta. In general, tratamentul
este indicat pentru a preveni morbiditatea potentiala (de exemplu
tahicardiomiopatia), pentru a reduce simptomele si pentru a reduce riscul
de MSC. Nu exista nici un motiv pentru a trata aritmiile ventriculare
asimptomatice in absenta oricarui potential beneficiu. Riscul
de moarte subita cardiaca depinde mai mult de tipul si
severitatea bolii cardiace asociate si mai putin de frecventa
sau clasificarea aritmiilor ventriculare.44,113 Anumite aritmii
precum TV polimorfa trebuie tratate chiar si la pacientii
asimptomatici fara boala cardiaca evidenta. Cu toate
acestea, asemenea aritmii sunt rareori asimptomatice si sunt probabil
determinate de modificari la nivelul canalelor ionice inca incomplet
elucidate.114,115 TVNS la pacientii cu infarct miocardic in
antecedente si disfunctie ventriculara creste riscul de MSC
si necesita evaluare in vederea tratamentului.116
Contributia aritmiilor ventriculare asimptomatice la managementul
pacientilor nu este bine stabilita pentru alte boli cardiace precum
CMD117 si CMH.118
4.2. Simptome potential
legate de
aritmiile ventriculare
Palpitatiile
sau perceptia neregularitatii ritmului cardiac pot fi
determinate de majoritatea aritmiilor si sunt de asemenea frecvent
relatate de pacienti in absenta oricarei aritmii.119
Mai putin frecvent, pacientii cu TV pot sa prezinte simptome
precum dispnee paroxistica sau durere precordiala in absenta
senzatiei de batai rapide ale inimii. In asemenea situatii
dispneea sau durerea precordiala pot fi determinate de consecintele
hemodinamice ale tahicardiei. Presincopa este un termen nu foarte bine
definit, dar probabil este interpretata de majoritatea pacientilor ca
o senzatie de sincopa iminenta.120 Nu este un simptom
specific. TV poate fi o cauza de sincopa nediagnosticata, in
special la pacientii cu boala cardiaca structurala.121
Pacientii cu disfunctie ventriculara si TV sau FV inductibile
cu defibrilator implantat au o rata mare de socuri administrate adecvat.122-128
Asemenea pacienti cu disfunctie ventriculara severa pot
avea risc de MSC.129 Pacientii cu tahicardie ventriculara
foarte rapida, precum torsada varfurilor cu sindrom de repolarizare, de
obicei se prezinta cu sincopa sau convulsii, mai degraba decat
cu palpitatii.130
4.2.1. Tahicardia
ventriculara stabila hemodinamic
Pacientii
cu TV mai lenta, stabila pot fi asimptomatici, dar mai frecvent
prezinta o senzatie de batai rapide ale inimii posibil
insotite de dispnee sau disconfort toracic. Stabilitatea sau
toleranta TV depind de frecventa tahicardiei, prezenta
conducerii retrograde, functia ventriculara si de integritatea
mecanismelor compensatorii periferice. TV stabila hemodinamic, relativ
bine tolerata nu sugereza absenta unei boli cardiace si poate
fi observata la pacientii cu disfunctie VS foarte severa.
Chiar pacientii cu fuctie proasta a VS pot sa nu simta
palpitatii in timpul TV. Prezentarea cu TV stabila nu indica per
se un prognostic benign la pacientii cu boala cardiaca
semnificativa.131 TV incesanta, desi stabila
hemodinamic, poate fi o cauza de deteriorare hemodinamica ce duce
la insuficienta cardiaca.132 La pacientii cu
ICD, frecventa tahicardiei ventriculare poate scadea sub
frecventa minima de detectare, ducand la lipsa de detectare a TV,
ceea ce poate preveni oprirea aritmiei. Reinceperea imediata a TV
dupa un soc adecvat al ICD poate duce de asemenea la deteriorare
hemodinamica si la o consumare precoce a bateriei.132,133
Tahicardia ventriculara instabila
hemodinamic
Termenul de instabil hemodinamic nu a fost definit
strict dar este larg folosit. Se refera la o tahicardie asociata cu hipotensiune
si proasta irigare a tesuturilor, si care este
considerata cu potential iminent de stop cardiac sau soc
daca nu este tratata. TV instabila hemodinamic este de obicei,
dar nu in mod exclusiv, observata la pacientii cu functie
ventriculara proasta. Pacientii cu functie
ventriculara normala pot avea TV instabila sau FV daca
tahicardia e suficient de rapida, ca in LQTS si alte sindroame de
repolarizare anormala.103 Unii pacienti cu cord normal
si TV idiopatica monomorfa sau chiar tahicardii
supraventriculare (TSV) pot deveni hipotensivi in timpul aritmiei
datorita unei reactii vasovagale.
4.3
Stopul cardiac subit
TV
rapida sustinuta sau FV duc la alterarea severa a perfuziei
tisulare si pierderea constientei ca rezultat al debitului
cardiac inadecvat, ducand la MSC daca nu sunt rapid intrerupte. Stopul
cardiac subit poate fi simptomul de prezentare in orice boala
cardiaca sau chiar la indivizi fara boala cardiaca
aparenta.44 Mecanismul de initiere al stopului cardiac
subit poate sau nu sa fie legat de aritmie.
5. Evaluarea generala a pacientilor cu aritmii ventriculare
documentate sau suspectate
5.1. Istoricul si
examenul clinic
Palpitatiile,
presincopa si sincopa sunt cele mai importante simptome ce necesita
o caracterizare suplimentara in cazul pacientilor suspectati
de a avea aritmii ventriculare. Palpitatiile sunt de obicei cu
debut/final bruste si pot fi asociate cu presincopa si/sau
sincopa. Episoade bruste de colaps cu pierderea constientei
fara orice simptom premonitor, ce tin de regula cateva
secunde, trebuie sa ridice suspiciunea unor tulburari de conducere
sau aritmii ventriculare. Alte simptome legate de boala structurala
cardiaca pot fi de asemenea prezente, in special disconfortul toracic,
dispneea sau fatigabilitatea. Un istoric minutios al mediamentelor luate
inclusiv dozajele trebuie inclus in evaluarea pacientilor suspectati
de aritmii ventriculare. Doua studii57,58 importante
au confirmat ca un istoric familial de MSC este un predictor independent
de susceptibilitate pentru aritmii ventriculare si MSC, cum a fost
mentionat mai inainte. Examenul clinic adesea nu relava nimic la
pacientii suspectati de aritmii ventriculare decat daca aritmia
apare in timp ce pacientul este examinat sau are alte elemente ce indica
boala structurala cardiaca.
5.2. Evaluarea neinvaziva
5.2.1. Electrocardiograma de
repaus
Recomandari
Clasa I
ECG
de repaus pe 12 derivatii este indicata la toti pacientii
care sunt evaluati pentru aritmii ventriculare. (Nivel de dovezi : A)
ECG
standard pe 12 derivatii permite nu numai identificarea diverselor
anomalii congenitale asociate cu aritmii ventriculare si MSC (LQTS, SQTS,
sindrom Brugada, CAVD) dar si identificarea altor parametrii ECG, ca aceia
datorati diselectrolitemiilor, sau dovada unei suferinte structurale
ca blocul de ramura, bloc AV, hipertrofia ventriculara, unde Q ce
indica boala ischemica cardiaca sau cardiomiopatie
infiltrativa. Durata QRS si anomaliile de repolarizare sunt
predictori independenti de MSC. O durata a QRS mai mare de 120130
ms a fost intr-un numar de studii asociata cu cresterea
mortalitatii la pacientii cu FEVS redusa (egala sau
mai mica de 30%). Studii prospective au raportat o asociere intre
subdenivelarea segmentului ST sau anomalii ale undei T si riscul crescut
de moarte cardiovasculara si MSC in particular. Aceste studii au
demonstrat un raport de risc pentru moartea de cauza cardiovasculara
de la 2,16 (intervalul de incredere [CI] de 95%: 1,30-3,58) la 2,4 (95% CI:
1,70- 3,53) in prezenta unui ECG ischemic134 si 4,4 (95%
CI: 2,6-7,4) pentru MSC in prezenta unei axe a undei T anormale.135,136
Un interval QTc prelungit este de asemenea predictor independent de MSC. QTc
mai mare de 420ms a fost dovedit ca avand un risc mai mare de deces
cardiovascular decat un QTc mai scurt. Un QTc mai mare de 440ms prezice semnificativ
mortalitatea cardiovasculara cu risc relativ ajustat de 2,1.137
Desi un QTc mai lung prezice MSC, trebuie retinut ca anumite
date sugereaza ca relatia intre QTc si supravietuire
poate avea aspectul de J. Cu alte cuvinte intervale QTc relativ scurte s-au
asociat de asemenea cu risc crescut. De exemplu, s-a mentionat ca
pacientii cu QTc mediu mai scurt de 400ms in timpul unei monitorizari
ECG de 24 ore au un risc de 2 ori mai mare de moarte subita decat
pacientii cu QTc mediu intre 400 si 440ms dupa 2 ani de
urmarire.138 Un QTc mai mic de 300ms este adesea folosit pentru
a defini SQTS, care este un predictor independent de MSC.139,140
5.2.2.
Testul de efort
Recomandari
Clasa I
Testul
de efort este recomandat pacientilor adulti cu aritmii ventriculare
care au o probabilitate intermediara sau mare de BCI prin varsta,
sex, simptome,* pentru a produce modificari ischemice sau aritmii
ventriculare. (Nivel de Dovezi: B) *vezi Tabelul 4
in completarea Ghidului ACC/AHA 2002 pentru Testarea de Efort141
pentru explicarea suplimentara a probabilitatii de BCI.
Testul de efort, indiferent de varsta, este util la
pacientii cu aritmii ventriculare cunoscute sau suspectate ca fiind induse
de efort, incluzand TV catecolaminergica, pentru a provoca aritmia, a obtine
un diagnostic si pentru a determina raspunsul pacientului la
tahicardie. (Nivel de Dovezi: B)
Clasa IIa
Testul
de efort poate fi util in evaluarea raspunsului la terapia medicala
sau ablatie la pacientii cu aritmii ventriculare cunoscute ca fiind
induse de efort . (Nivel de Dovezi: B)
Clasa IIb
Testul
de efort poate fi util la pacientii cu aritmii ventriculare si o
probabilitate mica de BCI prin varsta, sex, simptome.* (Nivel
de Dovezi: C) *vezi Tabelul 4 in completarea Ghidului ACC/AHA 2002 pentru
Testarea de Efort141 pentru explicarea suplimentara a
probabilitatii de BCI.
Testul
de efort poate fi util in investigarea extrasistolelor ventriculare izolate
(BPV) la pacientii de varsta mijlocie sau mai batrani
fara vreo alta dovada de BCI. (Nivel de Dovezi: C)
Clasa III
Vezi Tabelul 1 in completarea Ghidul ACC/ AHA 2002 pentru
Testarea de Efort141 pentru contraindicatii. (Nivel
de Dovezi: B)
Testul
EKG de efort este folosit usual in evaluarea pacientilor cu aritmii
ventriculare. Cea mai frecventa utilizare este pentru detectarea ischemiei
silentioase la pacientii suspectati ca avand BCI141
subjacenta. La pacientii cu BCI cunoscuta sau
silentioasa sau cardiomiopatii, prezenta BPV frecvente in
timpul sau dupa efort se asociaza cu risc mai mare de evenimente
cardiovasculare semnificative dar nu in mod special de MSC.19,20,24
BPV induse in timpul efortului la indivizi aparent normali nu trebuie folosite
pentru a stabili terapia decat daca se asociaza cu ischemie
documentata sau TV sustinuta. Cu exceptia beta blocantelor,
la momentul actual folosirea antiaritmicelor pentru abolirea BPVV induse in
timpul efortului nu s-a dovedit eficienta in reducerea MSC.
Testul
de efort in cazul tulburarilor de ritm adrenergic-dependente, incluzand
TV monomorfa si polimorfa, poate fi util in evaluarea
subiectilor simptomatici si evaluarea raspunsului la terapie.
ECG ambulatorie sau monitorizarea evenimentelor poate sa esueze in
inregistrarea aritmiei, mai ales daca pacientul este relativ sedentar.
Mai mult, testul de efort poate oferi informatii prognostice la
acesti pacienti avand in vedere ca prezenta aritmiei
ventriculare induse de efort creste mortalitatea la 12 luni de 3 ori,
comparativ cu pacientii cu aritmie numai in repaus.142
Pacientii cu dublete de BPV sau TV au o supravietuire mai mica
decat aceia cu ectopie ventriculara simpla la efort.143
Desi
siguranta testului de efort supravegheat este bine stabilita, mai
putine date sunt accesibile la pacientii cu risc pentru aritmii
ventriculare severe. Intr-un studiu, testul de efort la pacientii cu
aritmii ventriculare ce pun in primejdie viata a fost asociat cu o
incidenta de 2,3% a aritmiilor ce necesita cardioversie,
administrarea de medicamente intravenos sau resuscitare.144 Un
astfel de test de efort poate fi justificat intrucat e mai bine sa
demasti aritmiile si riscul intr-un mediu controlat. Testul de efort
trebuie facut acolo unde echipamentul de resuscitate si personalul
antrenat sunt imediat accesibile.
5.2.3. Electrocardiografia
ambulatorie
Recomadari
Clasa I
ECG
ambulatorie este indicata cand este
nevoie de clarificarea diagnosticului prin detectia aritmiilor,
modificarilor intervalului QT, alternantei undei T (TWA) sau
modificarilor ST, pentru evaluarea riscului si a terapiei (Nivel de Dovezi: A)
Monitoarele
event-triggered sunt indicate cand
simptomele sunt sporadice pentru a stabili daca sau nu sunt cauzate de
aritmii tranzitorii. (Nivel de Dovezi: B)
Dispozitive
de inregistare implantabile sunt utile la pacientii cu simptome sporadice
suspectate ca fiind legate de aritmie, ca sincopa, cand o corelatie
simptom-ritm nu poate fi stabilita prin tehnici conventionale de
diagnostic. (Nivel de Dovezi: B)
Folosirea
de tehnici de inregistare ambulatorie continua sau intermitenta
poate fi foarte utila in diagnosticarea unei artimii suspectate,
stabilirea frecventei ei si raportarea simptomelor la prezenta
aritmiei. Episoade de ischemie miocardica silentioasa pot fi
detectate. O inregistare continua Holter pe 24-48 ore este adecvata
cand se stie sau se suspecteaza ca aritmia apare cel putin
o data pe zi. Pentru episoade sporadice ce produc palpitatii,
ameteli sau sincopa, dispozitive conventionale de monitorizare a
evenimentelor sunt mai adecvate intrucat ele pot inregistra pe perioade mai
lungi de timp.145
Noi
dispozitive implantabile de inregistrare sunt capabile de monitorizare a
ritmului si pot fi activate de catre paceint sau automatic pentru
criterii prestabilite.
Desi
aceste dispozitive necesita implantare chirurgicala ele sunt extrem
de utile pentru diagnosticarea tahiaritmiilor severe si bradiaritmiilor
la pacientii cu simptome amenintatoare de viata ca
sincopa.120,146
5.2.4. Tehnici si
masuratori electrocardiografice
Recomandari
Clasa IIa
Este
rezonabil de a folosi TWA pentru imbunatatirea diagnosticului
si stratificarea riscului pacientilor cu aritmii ventriculare sau
care au risc de a dezvolta aritmii ventriculare amenintatoare de
viata. (Nivel de Dovezi: A)
Clasa IIb
Tehnicile
ECG ca ECG de inalta rezolutie (SAECG), variabilitatea ritmului
cardiac (HRV), sensibilitatea baroreflexa si turbulenta
frecventei cardiace pot fi utile pentru imbunatatirea
diagnosticului si stratificarea riscului pacientilor cu aritmii
ventriculare sau care au risc de a dezvolta aritmii ventriculare
amenintatoare de viata.
(Nivel de
Dovezi: B)
Trialurile
cu ICD, in special Multicenter Automatic Defibrillator Implantation Trial
(MADIT) II, au subliniat nevoia de a dezvolta noi metode pentru a identifica
pacientii cu cel mai inalt risc de aritmii ventriculare si MSC.
Numeroase modalitati exista in prezent pentru aprecierea acestui
risc dar numai doua sunt in prezent acceptate de U.S. Food and Drug
Administration (FDA): SAECG si TWA. Totusi, HRV si
sensibilitatea baroreflexa sunt de asemenea promitatoare. SAECG
imbunatateste raportul semnal-zgomot al ECG de suprafata,
permitand identificarea semnalelor de amplitudine mica (nivel de
microvolti) de la sfarsitul QRS care sunt numite potentiale
tardive. Potentialele tardive indica regiuni de miocard anormal ce
prezinta conducere lenta, o anomalie de substrat ce permite aritmii
ventriculare prin reintrare, si se crede ca servesc ca marker al prezentei
unui substrat EF pentru tahiaritmii ventriculare prin reintrare. Prezenta
unei SAECG anormale creste riscul de evenimente aritimice de 6-8 ori
post-IM.147 Cu toate acestea, restabilirea patentei arterei
coronare interesata de infarct prin fibrinoliza sau angioplastie
si folosirea pe scara larga a revascularizarii chirurgicale
au modificat substratul aritmogen, ducand la o scadere notabila in
puterea predictiva a acestei metode. De aceea SAECG izolata nu mai
este utila pentru identificarea pacientior post-IM cu risc de
aritmii ventriculare. Oricum valoarea predictiva negativa mare, de
89-99%, a facut din SAECG o metoda utila cu care sa se
excluda o tahicardie cu QRS larg drept cauza a unei sincope inexplicabile.148,149
TWA, care este o fluctuatie a
amplitudinii sau morfologiei undei T ce alterneaza bataie cu
bataie, determinata in timpul efortului sau pacingului atrial, a
fost dovedita ca o metoda utila pentru identificarea pacientilor
cu risc mare post-IM150si in prezenta cardiomiopatiei
ischemice sau non-ischemice. Acesta asociere pare independenta de FE
si la fel de puternica la pacientii cu cardiomiopatie
ischemica sau non-ischemica. TWA pare sa aiba o putere
predictiva negativa foarte mare.151-153 TWA poate fi
folosita de asemenea pentru identificarea riscului de mortalitate
aritmica la pacientii cu disfunctie de VS datorita unui
IM.154 Intr-un studiu mic cu pacienti cu caracteristicile
pacientilor din MADIT-II (post-IM, cu FE mai mica sau egala cu
30%) un test MTWA a fost mai bun decat durata QRS pentru identificarea unui
grup cu risc foarte mare si de asemenea unui grup cu risc mic ce nu
beneficiaza de terapie prin ICD.155
HRV,
care este o variatie bataie cu bataie a lungimii ciclului
cardiac ce rezulta din influenta sistemului nervos autonom la nivelul
nodului sinusal, la pacientii in ritm sinusal, prezice independent riscul
de MSC si mortalitate totala la pacientii post IM156
cu si fara disfunctie de VS.157-159 Studii
observationale sugereaza de asemenea utilitatea ei in prezenta
cardiomiopatiei nonischemice, dar acest fapt trebuie confrmat in trialuri
clinice mari. Exista multe moduri diferite de analiza a frecventei
cardiace, unele dintre ele, cum este turbulenta frecventei cardiace
pot fi mai productive decat celelalte. Scaderea sensibilitatii
baroreflexe, o apreciere cantitativa a capacitatii sistemului
nervos autonom de a reactiona la stimularea acuta ce implica in
primul rand reflexe vagale, comparat cu o apreciere continua a
informatiei simpatovagale bazale oferita de HRV, s-a dovedit de
asemenea de succes in aprecierea riscului de MSC atat izolat (cresterea inductibilitatii
evenimentelor aritmice incluzand TV in timpul testarii EF160,161)
si cand se foloseste in combinatie cu HRV (cresterea riscului
de mortalitate cardiaca post IM157) sau imeeeeeee TWA (cresterea riscului de
evenimente aritmice daca ambii parametri sunt anormali intr-o cohorta
de pacienti cu ICD162). Studii aditionale prospective
sunt necesare pentru a clarifica rolul acestor parametri ECG in aprecierea
riscului in diferite circumstante clinice.
5.2.5. Functia si
imagistica ventricului stang
Recomandari
Clasa I
Ecocardiografia
este recomandata la pacientii cu aritmii ventriculare care sunt
suspectati de boala structurala cardiaca (Nivel de Dovezi: B)
Ecocardiografia
este recomandata la subsetul de pacienti cu risc mare de a dezvolta aritmii
ventriculare grave sau MSC, ca aceia cu cardiomiopatie dilatativa,
hipertrofica, sau de ventricul drept, supravietuitorii IMA sau rudele
pacientilor cu boli mostenite asociate cu MSC (Nivel de Dovezi: B)
Testul
de efort impreuna cu o modalitate imagistica (ecocardiografia sau
SPECT) este recomandata pentru a detecta ischemia silentioasa
la pacientii cu aritmii ventriculare care au o probabilitate
intermediara de BCI prin varsta, simptome, sex si la care
aprecierea ECG nu este de incredere datorita utilizarii digoxinului,
HVS, subdenivelarii ST in repaus mai mari de 1mm, sindromului WPW sau
BRS. (Nivel de Dovezi: B)
Testul
de stres farmacologic combinat cu o modalitate imagistica
(ecocardiografie sau SPECT de perfuzie miocardica) este recomandat pentru
detectarea ischemiei silentioase la pacientii cu aritmii
ventriculare care au o probabilitate intermediara de BCI prin
varsta, simptome, sex si sunt incapabili fizic de a face un test de
efort limitat de simptome. (Nivel de
Dovezi: B)
Clasa IIa
RMN,
CT cardiac sau angiografia cu radionuclizi pot fi utile la pacientii cu
aritmii ventriculare cand ecocardiografia nu ofera o masurare
adecvata a functiei VS si VD si/sau o evaluare a
modificarilor structurale (Nivel de
Dovezi:B)
Coronarografia
poate fi utila in stabilirea sau excluderea prezentei stenozelor
coronariene semnificative la pacientii cu aritmii amenintatoare
de viata sau la supravietuitorii MSC, care au o probabilitate
intermediara sau mai mare de BCI prin varsta, simptome, sex (Nivel de Dovezi:C)
Imagistica VS poate fi utila la pacientii ce
sunt supusi unui pacing biventricular (Nivel
de Dovezi:C)
5.2.5.1. Ecocardiografia
Ecocardiografia
este tehnica imagistica cel mai frecvent folosita intrucat este
ieftina comparativ cu alte tehnici ca RMN si CT cardiac, este rapid
accesibila, si ofera un diagnostic corect al suferintelor
miocardice, valvulare sau congenitale asociate cu aritmii ventriculare
si MSC.163,164 (Tabel 6). In plus, functia
sistolica a VS si kinetica regionala pot fi evaluate, si la
majoritatea pacientilor poate fi determinata FE.165
Ecocardiografia poate fi de aceea indicata la pacientii cu aritmii
ventriculare suspectati ca avand boala structurala cardiaca
si la subsetul de pacienti cu risc mare de a dezvolta aritmii
ventriculare grave sau MSC, cum sunt aceia cu cardiomiopatii dilatative,
hipertrofice sau de VD, supravietuitorii IMA sau rude ale
pacientilor cu boli mostenite asociate cu MSC. Combinarea ecocardiografiei
cu testul de efort sau stresul farmacologic (denumita uzual eco de
stres) se foloseste la un grup selectionat de pacienti
suspectati de a avea aritmii ventriculare declansate de ischemie
si aceia care nu sunt capabili de a face efort sau au anomalii ECG de
repaus ce limiteaza acuratetea ECG pentru detectarea ischemiei.164
Originea anormala a arterelor coronare poate fi detectata prin ecocardiografie
sau alte tehnici imagistice.
Tabelul 6. Conditii asociate cu
aritmii ventriculare, ce pot fi diagnosticate prin ecocardiografie
|
Entitate
|
Acuratete
diagnostica
|
|
Cardiomiopatia
dilatativa
Cardiomiopatia
ischemica
HTA cu HVS moderata si severa Cardiomiopatia
hipertrofica Boala valvulara cardiaca CAVD Sindromul
Brugada
|
Mare
Mare
Mare
Mare
Mare
Medie
Mica
|
|
CAVD, cardiomiopatia aritmogena a
ventriculului drept; HVS, hipertrofie ventriculara stanga
|
5.2.5.2. Imagistica prin
rezonanta magnetica nucleara
Progresele
in RMN cardiaca au facut posibila folosirea acestei tehnici
imagistice pentru a evalua atat structura cat si functia cordului in
miscare. Rezolutia excelenta a imaginii obtinute prin
tehnicile actuale permite cuantificarea exacta a volumelor camerelor,
masei VS si functiei ventriculare.166-168 Are o importanta particulara la
pacientii suspectati de cardiomiopatie aritmogena de VD (CAVD)
la care RMN ofera o evaluare excelenta a dimensiunilor VD,
functiei si kineticii regionale si, important, permite
detectarea infiltrarii grase in miocardul VD.169,170
Angiografia VD poate fi de asemenea utila. RMN cardiaca este
utilizata din ce in ce mai des si este validata pentru
detectarea ischemiei (studii de kinetica la perfuzia de stress cu
adenozina si dobutamina) si detectarea si
cuantificarea infarctizarii/fibrozei, ca substrat pentru TV. Costul
si accesibilitatea RMN cardiace devin mai competitive. RMN cardiaca
poate oferi o evaluare cardiaca comprehensiva intr-un singur studiu.
Este important de subliniat ca, asa cum se intampla la toate
modalitatile imagistice, interpretarea corecta ii
influenteaza utilitatea.171
5.2.5.3. Tomografia
computerizata cardiaca
La fel
ca RMN, domeniul CT a avansat mult cu dezvoltarea de scannere rapide cu mai
buna rezolutie ce permite vizualizatrea tomografica a inimii
si arterelor coronare. Aceste sisteme permit cuantificarea
precisa a volumelor VS, FE si masei VS, cu rezultate comparabile cu
RMN, dar in plus ofera imagini segmentare ale arterelor coronare din care
poate fi cuantificat gradul calcificarii.172-176 Majoritatea
bolilor cardiace associate cu aritmii ventriculare severe sau MSC sunt evaluate
bine prin ecocardiografie. CT cardiaca poate fi folosita la
pacienti selectionati la care evaluarea structurilor cardiace
nu este accesibila prin ecocardiografie si RMN nu este
accesibila. Actulal nu exista nici un beneficiu suplimentar provenit
din vizualizarrea arterelor coronare prin CT cardiaca la pacientii cu
aritmii ventriculare.
5.2.5.4. Tehnicile cu
radionuclizi
SPECT de
perfuzie miocardica la efort sau folosind agenti farmacologici este
aplicabila la un grup selectionat de paceinti care sunt
suspectati de a avea aritmii ventriculare declansate de ischemie
si care sunt incapabili de efort sau au anomalii pe ECG de repaus ce
limiteaza acuratetea acesteia pentru detectarea ischemiei. SPECT de
perfuzie miocardica poate fi de asemenea folosita pentru a aprecia
viabilitatea miocardului la pacientii cu disfunctie de VS
datorita unui IM in antecedente.177 Cuantificarea precisa
a FEVS este posibila prin angiografie cu radionuclizi (scanare cu multiple
planuri/porti de achizitie) si astfel aceasta tehnica
poate fi utila la pacientii la care aceasta
masuratoare nu este accesibila prin ecocardiografie.
5.2.5.5. Coronarografia
La
pacientii cu aritmii amenintatoare de viata sau la
supravietuitorii MSC, coronarografia are un important rol diagnostic in
stabilirea sau excluderea prezentei unor stenoze coronariene
semnificative. Este obisnuit la acesti pacienti sa
faca aceasta procedura ca parte a evaluarii lor
diagnostice, mai ales daca au o probabilitate intermediara sau mai
mare de BCI. Recomandari detaliate privind imagistica si testarea de
efort pot fi gasite in ghidurile respective.141,164,177
5.3.
Studiul electrofiziologic
Studiul
EF cu inregistrari intracardiace si stimulare electrica, bazal
si cu medicamente a fost folosit pentru evaluarea aritmiei si
stratificarea riscului pentru MSC. Testarea EF pentru evaluarea TV a fost
introdusa in 1972 de catre Wellens si colab.178
Sensibilitatea, specificitatea si valorile predictive ale SEF au fost pe
larg evaluate de diversi autori, de obicei pe grupuri mici de
pacienti. SEF este folosit pentru documentarea inductibilitatii
TV, ghidarea ablatiei, evaluarea efectelor medicamentelor, aprecierea
riscului de TV recurenta sau MSC, evaluarea pierderii
constientei la pacienti selectionati cu aritmii suspectate
drept cauza si aprecierea indicatiilor de terapie prin ICD.121,179-183
Scopul SEF variaza fundamental cu tipul si severitatea bolii cardiace,
prezenta sau absenta TV spontane, terapia concomitenta cu
medicamente, protocolul de stimulare, locul de stimulare. Cele mai mari rate de
inductie si reproductibilitate sunt observate la pacientii
pos-IM.184-186
Pentru evaluarea pacientilor cu aritmii
ventriculare, majoritatea centrelor folosesc 8 stimuli ventriculari la cicluri
intre 600 si 400ms la apexul VD, la dublul pragului diastolic si cu
durata pulsului intre 0,5 si 2ms, emitand 1 pana la 3 extrastimuli in
conditii bazale. Acest test poate fi repetat in timpul infuziei de isoproterenol.187-189
Prematuritatea extrastimulilor este crescuta pana cand apare
refractaritatea sau se obtine inductia unei tahiaritmii ventriculare
sustinute. Secvente de ciclu lung-scurt pot fi testate. Intrucat
stimularea ventriculara prematura cu un interval scurt de cuplare e
mai probabil sa induca FV decat TV monomorfa, este rezonbil
sa se limiteze prematuritatea extrastimulilor la un minimum de 180ms cand
sunt studiati pacienti la care numai TV monomorfa
sustinuta inductibila este considerata ca endpoint dorit.190
Testarea EF poate fi repetata in tractul de
iesire al VD sau in VS.189 La anumiti pacienti la
care inductia TV este dependenta de frecventa stimularea
atrila sau ventriculara rapida poate induce TV.191
Studiul electrofiziologic la pacientii cu boala coronariana
Recomandari
Clasa I
SEF
este recomandat pentru evaluarea diagnostica a pacentilor
cu IM vechi cu simptome sugestive de tahiaritmii ventriculare, incluzand
palpitatii, presincopa sau sincopa. (Nivel de Dovezi: B)
Testarea
EF este recomandata la pacientii cu BCI pentru a ghida si a
aprecia eficienta ablatiei TV.
(Nivel de Dovezi: B)
Testarea
EF este utila la pacentii cu BCI pentru evaluarea diagnostica a
tahicardiilor cu complex QRS larg cu mecanism neclar. (Nivel de Dovezi: C)
Clasa IIa
SEF
este rezonabil pentru stratificarea riscului la pacentii cu IM vechi,
TVNS si FEVS egala sau mai mica decat 40% (Nivel de Dovezi:B)
Testarea medicamentelor pentru aprecierea eficacitatii
lor antiaritmice a fost in mare parte abandonata. Testarea EF a fost o cerinta in
trialurile MADIT, Multicenter UnSustained Tachycardia Trial (MUSTT),
si Beta-Blocker Strategy Plus Implantable Cardioverter Defibrillator (BEST-ICD)
si altele, dar nu in trialurile MADIT II, Sudden Cardiac Death in Heart
Failure (SCD-HeFT), sau Antiarrhytmic Versus Implantable Defibrillators (AVID).
Inductibilitatea TV la pacientii cu TVNS pe monitorizarea Holter a
identificat o populatie cu risc mare de TV/FV si la care s-a folosit
ICD in trialul MADIT.192
Intr-un
substudiu al trialului MUSTT, caracteristicile ECG ale TVNS (frecventa,
durata, aparitia in spital versus in afara spitalului) nu s-au
corelat cu inductibilitatea. Supravietuirea a fost mai proasta
penntru TVNS survenita in spital comparativ cu TVNS in afara spitalului,193
sugerand ca pot fi necesare criterii diferite de stratificare a riscului
la pacientii asimptomatici din ambulator. Intr-un substudiu al trialului
MADIT II inductibilitatea a fost de 36%. O frecventa cardiaca
mai mica, o FE mai mica si un interval mai mare intre IM si
studiul EF se coreleaza cu o mai mare inductibilitate.196
La
pacientii cu BCI, TVNS asimptomatica si FE mai mica de 40%,
inductibilitatea TV sustinuta
variaza intre 20% si 40%.116 Inductibilitatea
identifica pacientii cu mare risc de TV ulterioare si lipsa
inductibilitatii indica un risc mic la pacientii
asemanatori celor din MADIT.197 Oricum, acesti
paceinti au beneficiat in procent mare de revascularizare
percutanata. La pacientii cu BCI cu FE joasa (mai putin de
30%), noninductibilitatea nu implica un prognostic bun. Inductibilitatea
persistenta in timp ce pacientul primeste antiaritmice prezice un
prognostic prost.199 Pacientii la care amiodarona suprima
inductibilitatea TV sau scade frecventa TVpana la un ciclu mediu mai
mare de 400ms au avut mortalitate mai mare cu 30% comparativ cu pacientii
care nu raspund la amiodarona si li se implanteaza un ICD.200
Administarea medicatiei antiaritmice ghidata prin SEF la
pacientii cu TVNS la care s-a indus TV sustinuta nu confera
nici un beneficiu.195
Valoarea
prognostica a flutterului ventricular inductibil si a FV este
inca controversata. Date limitate asupra valorii prognostice a
flutterului ventricular inductibil sugereaza ca poate fi un endpoint
important.201,202
Studiul electrofiziologic la pacientii cu cardiomiopatie dilatativa
In CMD
SEF joaca un rol minor in evaluarea si managementul TV. Aceasta este
legata de inductibilitatea si reproductibilitatea reduse ale
studiului EF, si valoarea predictiva a TV induse.203,204
(vezi Sectiunea 9.1)
5.3.3.
Studiul electrofiziologic in anomaliile de repolarizare datorate sindroamelor
aritmice genetice
5.3.3.1. Sindromul de QT lung
Testarea
EF nu s-a dovedit utila in LQTS103,205 (vezi Sectiunea
11.1.1 pentru discutii suplimentare).
5.3.3.2. Sindromul Brugada
Rolul
testarii electrofiziologice pentru stratificarea riscului in sindromul
Brugada este dezbatut,104,206-208 si va ramane
probabil nedefinit pana cand vor fi obtinute date prospective la
pacienti studiati cu un protocol uniform, intr-o populatie
mare, cu urmarire adecvata (vezi Sectiunea 11.1.3. pentru
discutii suplimentare).
5.3.3.3. Cardiomiopatia
hipertrofica
Valoarea
SEF in CMH este controversata (vezi Sectiunea 9.2. pentru
discutii suplimentare).
5.3.3.4. Cardiomiopatia
aritmogena de ventricul drept
Manufestarile
aritmice ale CAVD sunt variabile.96 Rolul prognostic al
testarii electrofiziologice la pacientii cu extrasistole ventriculare
izolate sau TVNS este necunoscut. Raspunsul la testarea EF poate fi
influentat de severitatea bolii. Progresia bolii trebuie luata in
considerare (vezi Sectiunea 9.3 pentru discutii suplimentare).
Studiul electrofiziologic la pacientii cu tahicardie cu origine in
tractul de iesire
Este
similar cu cel al altor forme de TV. Este motivat de nevoia de a stabili
diagnosticul precis pentru a ghida ablatia cu cateter curativa.209,210
(vezi Sectiunea 12.1. pentru discutii suplimentare)
Studiul electrofiziologic la pacientii cu sincopa
Recomandari
Clasa I
Studiul
EF este recomandat la pacientii cu sincopa de cauza
necunoscuta cu disfunctie de VS sau boala cardiaca
structurala. (Nivel de
Dovezi: B)
Clasa IIa
Studiul
EF pote fi util la pacientii cu sincopa cand bradiaritmii sau
tahiaritmii sunt suspectate si la care studiile diagnostice noninvazive
nu sunt concludente (Nivel de Dovezi: B)
Sincopa
este un simptom tranzitor ce poate fi cauzat de o tulburare de ritm cu sau
fara o boala cardiaca asociata. Testarea EF este
folosita pentru a documenta sau exclude cauza aritmica a sincopei.120,211
Este cea mai utila la pacientii cu BCI sau disfunctie de VS. SEF
nu este de obicei primul pas in evaluare
ci mai degraba este complementara pentru explorarea completa a
sincopei. Lipsa corelatiei intre simptome si o aritmie documentata
produsa in timpul SEF poate duce la suprainterpertarea sau
subinterptretarea valorii predictive a rezultatelor. Efecte tranzitorii ale
medicamentelor ce pot provoca sincopa pot ramane nedetectate. Alte
cauze ca etiologia neurologica trebuie luate in considerare la unii pacienti.
5.3.5.1.
Studiul electrofiziologic cand este suspectata bradicardia
Sincopa se poate datora bradiaritmiilor din disfunctia
de nod sinusal sau blocului atrioventricular. Antiaritmicele, beta-blocantele,
glicozizi cardiotonici si blocantii canalelor de calciu pot induce
bradicardie simptomatica. Studiul electrofiziologic poate fi utilzat
pentru a documenta sau provoca bradiaritmii sau blocul atrioventricular atunci
cand celelalte investigatii nu au adus informatii clare. Stabilirea
diagnosticului depinde de criteriile de selectie a pacientilor.212
Studiul electrofiziologic este mai util in prezenta bolii cardiace
organice.213 Profitul diagnostic in absenta bolii cardiace
organice si a ECG-ului anormal este mic. SEF fals pozitiv poate aparea
pana la 24% din pacienti. La pacientii cu sincopa, bloc de
ramura cronic si FE redusa (sub 45%), TV indusa la SEF
apare in pana la 42% din cazuri.184,214,215 La pacientii cu sincopa si
bloc de ramura SEF fals negative
sunt frecvente.216,217 SEF la pacientii cu bradicardie
sporadica si sincopa are sensibilitate limitata chiar
si atunci cand se asociaza stresul electrofarmacologic precum
administrarea intravenoasa de procainamida sau atropina.218
SEF poate determina aparitia unui raspuns tahiaritmic
nespecific la pacientii cu functie VS pastrata care nu au
boala cardiaca organica.219
5.3.5.2 Studiul
electrofiziologic in caz de suspiciune a tahiaritmiei supraventriculare
Rolul
SEF este de a documenta tipul tahiaritmiei si de a ghida tratamentul.
Intr-o populatie mixta, diagnosticul s-a obtinut la 5% din
cazuri.220 In tahiaritmiile supraventriculare, sincopa este rareori
unicul simptom si palpitatiile sunt de obicei prezente. Reactia
vasodepresoare ce apare la cativa dintre pacientii cu tahicardie
supraventriculara indusa, in principal prin reintrare in nodul
atrioventricular,221 poate fi cauza sincopei. Sincopa nu se
coreleaza cu frecventa sau durata intervalelor R-R preexcitate in
sindromul WPW din timpul fibrilatiei atriale.221
5.3.5.3 Studiul
electrofiziologic in caz de suspiciune a tahicardiei ventriculare
Sincopa
la pacientii cu boala cardiaca organica si, in special
disfunctie de VS semnificativa este de rau augur. TVNS la
monitorizarea Holter, sincopa si boala cardiaca organica sunt
inalt sugestive pentru prezicerea TV inductibile.184 Sincopa
asociata cu boala cardiaca organica si FE redusa are
recurenta si rata de deces crescute222,223 chiar
si atunci cand rezultatele SEF sunt negative. SEF este util la
pacientii cu disfunctie VS datorata unui IM vechi (FE<40%)
dar nu este sensibil la pacientii cu cardiomiopatie non-ischemica.184
Inducerea TV polimorfa sau FV, in special cu tehnici de stimulare
agresiva, nu este specifica. In boala cardiaca ischemica un
diagnostic se poate obtine in pana la 50% din cazuri.222
In cardiomiopatia hipertrofica, SEF nu este diagnostic la majoritatea
pacientilor.224 A fost observata inducerea TV
non-specifica la 23% dintre pacientii cu reducere usoara a
FE.225
6.
Tratamentul aritmiilor ventriculare
6.1.
Managementul general
Alegerea
unui tratament adecvat pentru managementul aritmiilor ventriculare
(extrasistole ventriculare, TVNS, TVSM si TVSP si flutter
ventricular/fibrilatie ventriculara) necesita intelegerea
etiologiei si mecanismului aritmiei, evaluarea conditiilor medicale
asociate care pot contribui/exacerba aritmia, riscurilor datorate aritmiei
si raportului beneficiu/risc privind selectia tratamentului.31,99,226-235
Tratamentul aritmiei manifeste poate implica oprirea drogurilor proaritmice,
tratament antiaritmic specific, implantare de dispozitive, ablatia si
interventia chirurgicala.
6.2. Tratamentul medicamentos
In
trialurile clinice randomizate, cu exceptia beta-blocantelor, toate
celelalte medicamente antiaritmice disponibile actual nu s-au dovedit a fi
eficiente in tratamentul primar al aritmiilor ventriculare
amenintatoare de viata sau in preventia mortii
subite cardiace. Ca regula generala, tratamentul antiaritmic poate fi
eficient ca terapie adjuvanta in managementul pacientilor predispusi
la aritmie in circumstante speciale. Datorita posibilelor efecte
secundare adverse ale antiaritmicelor disponibile, aceste medicamente trebuie
utilizate cu precautie. Aceasta sectiune furnizeaza
comentarii generale despre tratamentul medicamentos si interventional
pentru aritmiile amenintatoare de viata. Recomandarile
si nivelul de dovezi pentru tratamentul specific al aritmiilor
ventriculare care apar in diferite boli cardiace sunt furnizate in alte
sectiuni ale acestui ghid, cu exceptia recomandarilor privind
ablatia, care se gasesc in sectiunea 6.6.
Multe
medicamente cardiovasculare si non-cardiovasculare prelungesc
repolarizarea ventriculara si au capacitatea de a precipita
aparitia tahiaritmiilor ventriculare amenintatoare de
viata202, 236-239 (vezi sectiunea 13.6). Unii
pacienti sunt mai susceptibili decat altii la efectele de alungire a
intervalului QT chiar si la dozele obisnuite, posibil datorita
predispozitiei genetice sau sexului feminin. Mai frecvent, efectul
proaritmic al unui medicament este legat de cresterea concentratiei
sanguine, ca rezultat al dozelor excesive, bolii renale sau
interactiunilor medicamentoase. Odata ce s-a considerat ca
aritimia ventriculara a fost datorata prelungirii QT de catre
unul sau mai multe medicamente prescrise, tratamentul in cauza trebuie
oprit si urmat de monitorizarea atenta a repolarizarii
ventriculare si a ritmului cardiac.
6.3. Medicamentele
antiaritmice
6.3.1. Valoarea
medicamentelor antiaritmice
Utilizarea
antiarimicelor in situatii acute este descrisa in sectiunea 7.
Antiaritmicele
disponibile pot fi clasificate dupa Vaughan Williams in patru clase (tipul
I: blocante ale canalelor rapide de sodiu, tipul II: beta-blocante, tipul III:
blocante ale curentilor de potasiu repolarizanti, tipul IV:
antagonisti ai canalelor de calciu)240 sau dupa Gambitul
Sicilian, mult mai precis privind mecanismul si mult mai relevant clinic.241
Clasificarea Vaughan Williams este oarecum depasita pentru
ca antiaritmicele au actiuni complexe ceea ce nu face
usoara clasificarea in una din cele patru clase de efecte
antiaritmice specificate. Aceasta clasificare are utilitate
limitata cand se alege un antiaritmic pentru tratamentul unei aritmii
specifice. Gambitul
Sicilian, introdus in 1991, a fost o incercare de a clasifica antiaritmicele pe
baza mecanismelor lor de actiune si a mecanismelor antiaritmogene.
6.3.1.1. Beta-blocantele
Aceste
medicamente sunt eficiente in suprimarea batailor ventriculare
ectopice si a aritmiilor ca si in reducerea mortii subite
cardiace la pacienti cu o serie de boli cardiace cu sau fara
insuficienta cardiaca. Beta-blocantele sunt agenti
antiaritmici siguri si eficienti putand fi considerate piatra de
temelie a tratamentului antiaritmic.242,243 Mecanismul
eficacitatii antiaritmice a acestei clase de medicamente implica
blocarea competitiva la nivelul receptorilor adrenergici a mecanismelor
trigger simpatic-dependente, incetinirea frecventei sinusale si
posibil inhibitia eliberarii excesive de calciu prin receptorul de
ryanodina.244
6.3.1.2.
Amiodarona si sotalolul
Amiodarona
are un spectru de actiuni care include blocarea curentilor
repolarizanti de potasiu care pot inhiba sau opri aritmiile ventriculare
prin cresterea lungimii de unda a reintrarii. Beneficiul global
pe termen lung al amiodaronei este controversat, majoritatea studiilor
nearatand un avantaj clar fata de placebo. Cateva studii si
o metaanaliza a catorva studii mari au aratat reducerea mortii
subite cardiace cu amiodarona la pacientii cu disfunctie VS
datorata unui infarct miocardic sau unei cardiomiopatii dilatative
non-ischemice,245-247 dar trialul SCD-HeFT nu a aratat
beneficiu al tratamentului cu amiodarona privind supravietuirea
comparativ cu placebo.7a,248 Administrarea cronica de amiodarona
este asociata cu interactiuni medicamentoase complexe si o
serie de efecte adverse implicand plamanul, ficatul, tiroida si
pielea. Ca regula generala, cu cat este mai mare probabilitatea
aparitiei unui efect advers, cu atat este mai necesara oprirea
administrarii medicamentului. Sotalolul, ca si amiodarona, este
eficient in oprirea aritmiilor ventriculare, dar are efecte proaritmice mai
mari si nu a fost dovedita o crestere clara a supravietuirii;
agravarea aritmiilor ventriculare apare la 2-4% din pacientii
tratati.249
6.3.1.3. Eficacitatea
antiaritmicelor
Antiaritmicele
disponibile, altele decat beta-blocantele, nu trebuie utilzate ca terapie de
prima linie in tratamentul aritmiilor ventriculare si preventia
mortii subite cardiace. Eficacitatea antiaritmicelor non-beta-blocante
este echivoca, si fiecare antiaritmic are potential semnificativ
pentru efecte adverse, inclusiv proaritmia.
6.3.2. Situatii
speciale cand pot fi indicate antiaritmicele
Tratamentul
cu amiodarona poate fi considerat in situatii speciale;109
analize secundare indica posibil beneficiu in supravietuire cand
amiodarona este asociata cu beta-blocantele.250,251 Oricum,
studiul SCD-HeFT nu a aratat beneficiu al amiodaronei la pacientii cu
insuficienta cardiaca clasa functionala II NYHA
si a fost daunatoare la pacientii cu
insuficienta cardiaca clasa functionala III NYHA
si FE≤35%.8 S-a aratat ca azimilida scade
riscul de administrare a socurilor electrice adecvate sau neadecvate la
pacientii cu defibrilator automat implantat.252 S-a aratat
de asemenea ca atat sotalolul cat si amiodarona reduc frecventa
administrarii socurilor la pacientii cu defibrilator automat
implantat.253,254
6.3.2.1. Pacientii cu
tahiaritmii ventriculare care nu indeplinesc criteriile pentru implantarea unui
ICD
Beta-blocantele
sunt prima linie de tratament, dar daca aceasta terapie nu este
eficienta in doze maxime, atunci pot fi incercate amiodarona sau
sotalolul, cu monitorizarea efectelor adverse pe durata tratamentului.
6.3.2.2. Pacientii cu
ICD care prezinta tahicardie ventriculara
recurenta/fibrilatie ventriculara cu descarcari
frecvente adecvate ale defibrilatorului
Acest
scenariu extrem, a fost denumit furtuna defibrilatorului/tahicardiei si
necesita adaugarea unui antiaritmic si/sau ablatia pentru
controlul tahicardiei ventriculare recurente si a eliberarii de
socuri asociate. Sotalolul este eficient in oprirea
aritmiilor atriale si ventriculare;253 o alternativa de
ales este asocierea beta-blocantelor cu amiodarona. Deoarece multi astfel
de pacienti au FE mica si functie renala
scazuta, amiodarona si beta-blocantele, mai mult decat
sotalolul, pot fi terapie de prima linie pentru furtuna defibrilatorului.
Sotalolul trebuie evitat la pacientii cu functie VS sever
deteriorata sau insuficienta cardiaca semnificativa.
Studiile pe animale si un caz raportat au aratat beneficiile
modularii neurale via maduva spinarii.257Adminstrarea
intravenoasa a amiodaronei este utila.
6.3.2.3. Pacientii cu
ICD care au fibrilatie atriala paroxistica sau cronica cu
frecventa rapida si descarcare neadecvata a
defibrilatorului
Controlul
raspunsului ventricular rapid al tahiaritmiilor atriale este
esential si tratamentul combinat cu beta-blocante si/sau
antagonisti de calciu este util. Amiodarona a fost folosita pentru
controlul frecventei daca alte terapii au fost contraindicate,
netolerate sau ineficiente. Ablatia nodului atrioventricular poate fi
necesara cand tratamentul farmacologic nu este eficient.
6.4. Medicamente
non-antiaritmice
Folosirea
medicamentelor non-antiaritmice in situatii acute va fi discutata in
sectiunea 7.
6.4.1. Electrolitii
Administrarea
de potasiu si magneziu, fie intravenos in situatii acute, fie oral
pentru cresterea cronica a nivelului lor sangvin, poate
influenta favorabil substratul electrofiziologic implicat in aritmiile
ventriculare. Aceste medicamente sunt utile in special in prezenta hipopotasemiei
si hipomagneziemiei si trebuie luate in considerare ca tratament
adjuvant in absenta nivelurilor electrolitice mici. Remodelarea
ventriculara apare dupa un infarct miocardic sau este asociata
unei cardiomiopatii non-ischemice; aceste modificari structurale cu alterarea
secundara a canalelor ionice poate exacerba potentialul pentru
aritmii ventriculare. Cateva medicamente, precum inhibitorii enzimei de
conversie a angiotensinei, blocantii receptorilor angiotensinei si
blocarea aldosteronului cu spironolactona sau eplerenona,
imbunatatesc substratul miocardic prin reversia remodelarii
si se asociaza cu reducerea mortii cardiace subite si
non-subite.110,258 Este important de retinut ca
tulburarile electrolitice sunt comune la pacientii cu
insuficienta cardiaca, in special la cei care folosesc doze
mari de diuretice de ansa.
6.4.2.
Antitrombinice/antiplachetare
Intr-o
analiza retrospectiva a mai mult de 6700 pacienti
participanti in Studies Of Left Ventricular Dysfunction (SOLVD),
trialuri de preventie si tratament, tratamentul antitrombinic a fost
asociat cu reducerea mortii subite cardiace.259 Tratamentul
antiplachetar care include aspirina si tratamentul anticoagulant au contribuit
la aceasta reducere a mortii subite cardiace, posibil ca rezultat al
reducerii frecventei ocluziilor coronariene trombotice in grupul de
pacienti cu risc mare.
6.4.3. Acizii grasi n-3
si lipidele
Cresterea
dovezilor experimentale si clinice sugereaza ca acizii
grasi n-3 sunt antiaritmici260 si pot preveni moartea
subita cardiaca la oameni.261 Oricum, datele sunt
contradictorii. Intr-un trial randomizat incluzand pacienti cu un episod
recent de aritmie ventriculara sustinuta si
defibrilator-cardioverter implantat, suplimentarea dietei cu ulei de
peste nu a redus riscul de tahicardie ventriculara/fibrilatie
ventriculara si probabil a avut efect proaritmic la unii
pacienti.262 Un al doilea studiu similar a aratat o
tendinta de prelungire a timpului pana la primul episod de
TV/FV sau decesul de orice cauza (p=0,057) si reducerea
semnificativa a riscului cand au fost incluse toate evenimentele probabile
TV/ FV.262,263
Descoperirile
arata ca statinele reduc aparitia aritmiilor
amenintatoare de viata la pacientii cardiaci cu risc
crescut cu instabilitate electrica.264 Ambele terapii
sugereaza ca mecanismul efectelor antiaritmice poate fi legat de
stabilizarea electrofiziologica a membranei miocitare bilipidice
implicata in mentinerea gradientilor electrolitici.
6.5. Dispozitive implantabile
si externe
6.5.1.
Defibrilatorul-cardioverter implantabil
Cateva
trialuri clinice prospective multicentrice au demonstrat
imbunatatirea supravietuirii cu implantarea de
defibrilator-cardioverter la pacientii cu risc crescut si
disfunctie VS datorata unui infarct miocardic vechi si
cardiomiopatie non-ischemica8,192,265-270 (Figura 2).
Tratamentul
cu ICD, comparativ cu tratamentul antiaritmic conventional sau
traditional, a fost asociat cu reducerea
mortalitatii de la 23% la 55% in functie de grupul de risc al
participantilor la trial, cu imbunatatirea
supravietuirii datorata aproape in exclusivitate reducerii
mortii subite cardiace. Trialurile pot fi subclasificate in 2 tipuri:
trialuri de preventie primara (profilactice) in care subiectii
nu au avut aritmii ventriculare amenintatoare de viata sau
echivalente simptomatice si trialuri de preventie secundara
implicand subiecti care au avut in antecedente oprire cardiaca,
tahicardie ventriculara amenintatoare de viata sau
sincopa neexplicata cu probabilitate mare ca o tahiaritmie
ventriculara ar fi fost cauza sincopei.
Progresele
importante privind tratamentul cu ICD continua prin procedeul de
implantare transvenoasa, reducerea dimensiunilor generatorului, longevitatea
sistemului, detectia aritmiei si modalitatile de multiprogramabilitate.
Oricum, este important de retinut ca defectarea
dispozitivului, cu toate ca e rara, poate aparea. ICD-urile
actuale au optiuni pentru o singura camera, doua camere
si resincronizare cardiaca biventriculara, pentru terminarea
fara soc electric a aritmiilor ventriculare, in plus cu
descarcarea socului la mai multe niveluri pentru tahicardie
ventriculara sau fibrilatie ventriculara. Problemele asociate
cu tratamentul ICD includ descarcarea neadecvata a socului
electric in special pentru fibrilatia atriala cu raspuns
atrioventricular rapid, furtuna defibrilatorului cu descarcare adecvata
recurenta a ICD pentru tahiaritmii ventriculare recurente sau descarcarea
neadecvata pentru o multitudine de motive, infectii legate de
implantarea dispozitivului si exacerbarea insuficientei cardiace
cand un procent mare de batai cardiace sunt produse de la apexul VD,
in special cand functia VS este deja compromisa.
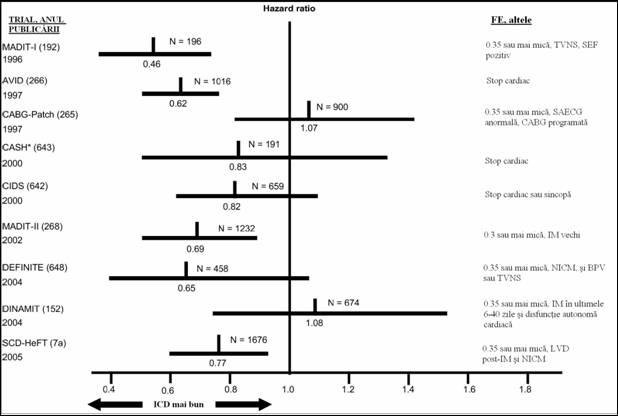
Figura 2. Trialuri majore cu ICD. Hazard ratio (linii verticale) si
intervale de incredere 95% (linii orizontale) pentru deces de orice cauza
in grupul cu defibrilator-cardioverter comparativ cu grupul
fara defibrilator-cardioverter.
CABG, bypass
aorto-coronarian; SEF, studiu electrofiziologic; LVD, disfunctie ventricul
stang; FE, fractie de ejectie ventricul stang; IM, infarct miocardic;
N, numar pacienti; NICM, cardiomiopatie non-ischemica; TVNS,
tahicardie ventriculara nesustinuta; BPV, complexe ventriculare
premature; SAECG, electrocardiograma cu semnal mediat. * Include doar
pacientii cu defibrilator-cardioverter si amiodarona din CASH.
Pentru numele intreg al trialurilor, vezi Anexa 3.
Este
probabil recomandabila limitarea pacingului VD la minimum pentru orice
pacient. Solutiile posibile includ selectarea unei frecvente minime
adecvate si a unui interval atrioventricular suficient de lung. Evitarea
unei accelerari agresive a frecventei, a modului de modulare a
frecventei si, la unele modele de stimulatoare recente, folosirea
modului automatic de pacing cu selectarea algoritmilor care favorizeaza
semnificativ pacingul atrial comparativ cu cel ventricular.271
Insuficienta cardiaca apare de obicei in situatii cu
disfunctie VS avansata cu ICD programat pentru pacing bicameral la
frecvente cardiace care domina ritmul, ceea ce contribuie la
desincronizarea pacingului ventricular. Ghidul ACC/AHA/NASPE 2002 updatat
pentru implantarea de stimulatoare cardiace si dispozitive antiaritmice,
ghidul ACC/AHA 2004 pentru tratamentul pacientilor cu infarct miocardic cu
supradenivelare de segment ST, ghidurile ESC 2001 si 2003 de
preventie a mortii subite cardiace, ghidul ESC de diagnostic si
tratament al insuficientei cardiace cronice, ghidul ACC/AHA 2005 updatat
de diagnostic si tratament al insuficientei cardiace la adulti
includ un numar mare de recomandari privind tratamentul cu ICD.1-6
Detaliile si referintele provin din textele complete ale ghidurilor
care se gasesc pe website-urile ACC, AHA, HRS (cunoscuta anterior ca
NASPE) si ESC. Descoperirile din trialul SCD-HeFT furnizeaza dovezi
suplimentare ca ICD-ul este eficient la pacientii cu risc crescut cu
cardiomiopatie ischemica si non-ischemica. Diferentele in
recomandarile acestui ghid fata de cele publicate anterior
reflecta in principal datele din studiile noi. Discutii detaliate
privind consideratiile pentru recomandarile de tratament se
gasesc in introducere. Oricum, exista inconsecvente intre
ghiduri privind limitele utilizarii electrofiziologiei folosite in
recomandari.
6.5.2. Defibrilatoare
automate externe
DAE
salveaza vieti cand defibrilarea externa poate fi efectuata
in cateva minute de la instalarea fibrilatiei ventriculare. DAE
reprezinta o metoda eficienta de defibrilare a persoanelor care
au un stop cardiac in afara spitalului, si folosirea lor de catre
primii responsedii traditionali si non-traditionali, pare
sa fie sigura si eficienta. Localizarea dispozitivului
cat mai aproape pentru a reduce intarzierea de la oprirea cardiaca este
critica. Eforturile federale, statale si ale comunitatii
au fost eficiente in plasarea DAE in scoli, la locul evenimentelor
sportive, locuri cu densitate rezidentiala mare, aeroporturi,
avioane si vehicule ale politiei si pompierilor. Aproximativ
80% din cazurile de oprire cardiaca apar la domiciliu si plasarea de
DAE la domiciliu pare sa fie rezonabila si adecvata pentru
pacientii cu risc mare de aritmii amenintatoare de
viata. Autoritatile federale din SUA au aprobat folosirea
la domiciliu a DAE in familiile cu risc mare de aritmii mostenit precum
sindromul de QT lung si cardiomiopatia hipertrofica. FDA a aprobat
vanzarea libera a DAE.
6.5.3. Defibrilatoarele
automate portabile
Defibrilatorul
automatic portabil este un dispozitiv asemanator cu o vesta care
se poarta pe sub haine, monitorizeaza continuu ritmul cardiac
si elibereaza automat soc electric cand este detectata
fibrilatia ventriculara. Acest dispozitiv este purtat permanent 24
ore/zi cu exceptia perioadei in care pacientul isi face baie sau
dus. Defibrilatorul automatic portabil a fost aprobat in SUA de catre
FDA pentru pacientii cardiaci cu risc tranzitor mare pentru
fibrilatie ventriculara precum cei care sunt in asteptarea unui
transplant cardiac, cei cu risc foarte mare dupa un infarct miocardic
recent sau o procedura cardiaca invaziva, sau cei care
necesita inlocuire temporara a unui defibrilator implantat infectat
pentru tratament antibiotic.
6.6. Ablatia
Recomandari
Clasa I
Ablatia
este indicata la pacientii care au risc mic de morte subita cardiaca
si au tahicardie ventriculara sustinuta predominant
monomorfa rezistenta la medicamente, cu intoleranta la
medicamente sau care nu doresc tratament medicamentos pe termen lung. (Nivel de dovezi: C)
Ablatia
este indicata la pacientii cu tahicardie ventriculara cu
reintrare in ramura. (Nivel de
dovezi: C)
Ablatia
este indicata ca tratament adjuvant la pacientii cu ICD care
necesita socuri multiple pentru tahicardie ventriculara
sustinuta care nu se pot rezolva prin reprogramare sau schimbarea tratamentului
medicamentos sau care nu doresc tratament medicamentos pe termen lung.206,278
(Nivel de dovezi: C)
Ablatia
este indicata la pacientii cu sindrom WPW resuscitat din oprire
cardiaca subita datorata fibrilatiei atriale cu conducere
rapida pe calea accesorie determinand aparitia fibrilatiei ventriculare.279
(Nivel de dovezi: B)
Clasa IIa
Ablatia poate fi
utila la pacientii care au risc mic de morte subita
cardiaca si au tahicardie ventriculara nesustinuta
monomorfa simptomatica rezistenta la medicamente, cu intoleranta
la medicamente sau care nu doresc tratament medicamentos pe termen lung. (Nivel de dovezi: C)
Ablatia
poate fi utila la pacientii care au risc mic de morte subita
cardiaca si extrasistole ventriculare predominant monomorfe, frecvente,
simptomatice, rezistente la medicamente, cu intoleranta la
medicamente sau care nu doresc tratament medicamentos pe termen lung. (Nivel de dovezi: C)
Ablatia
poate fi utila la pacientii cu sindrom WPW care au calea accesorie cu
durata perioadei refractare mai mica de 240ms.279 (Nivel de dovezi: B)
Clasa IIb
Ablatia
potentialelor fibrelor Purkinje poate fi considerata la
pacientii cu furtuna aritmica ventriculara provocata
de extrasistole ventriculare cu morfologie similara.280 (Nivel de dovezi: C)
Ablatia
extrasistolelor ventriculare simptomatice poate fi considerata daca
sunt foarte frecvente, pentru a evita sau trata cardiomiopatia indusa de
tahicardie.281 (Nivel de dovezi:
C)
Clasa III
Ablatia
extrasistolelor ventriculare relativ rare nu este indicata. (Nivel de
dovezi: C)
6.6.1. Ablatia pe
cateter
Ablatia
prin aplicarea specifica de radiofrecventa pentru tahicardia
ventriculara a evoluat pe masura progreselor tehnologiei.
Ablatia cu radiofrecventa poate fi aplicata ca tratament al
pacientilor cu tahicardie ventriculara cu disfunctie VS
datorata unui infarct miocardic vechi, cardiomiopatiei, reintrarii in
ramura si diferitelor forme de tahicardie ventriculara
idiopatica.282-284
6.6.2. Boala
cardiaca organica aparent absenta
Mapping-ul
specific si tehnicile de ablatie sunt utilizate diferit in
functie de tipul de tahicardie ventriculara. In timp ce
pacientii fara boala cardiaca organica evidenta
reprezinta un mic procent din pacientii cu tahicardie
ventriculara, acestia prezinta interes particular pentru
tratamentul ablativ deoarece aceasta tehnica poate fi curativa.295,296
Acestea se prezinta tipic ca tahicardie ventriculara cu punct de
plecare din VD cu morfologie de BRS cu ax inferior, sau din VS cu morfologie de
BRD, si se asociaza, in general, cu prognostic bun.289,297-300
6.6.3. Tahicardia
ventriculara cu reintrare in ramura
Tahicardia
ventriculara cu reintrare in ramura este adeseori asociata cu
cardiomiopatie.279 Cateter ablatia cu radiofrecventa
a ramurilor este curativa pentru aritmie dar nu si pentru anomalia
structurala de baza.301 Datorita
severitatii bolii de baza si prevalentei mari a
anomaliilor de conducere, tratamentul adjuvant cu dispozitive trebuie luat in
considerare la acesti pacienti.301
6.6.4. Boala
cardiaca structurala
Tahicardia
ventriculara este o complicatie comuna a bolii cardiace organice
si determina un risc de mortalitate semnificativ la pacientii
cu boala cardiaca cronica si FE mica. La cei cu
anomalii structurale extinse, in special cei cu infarct miocardic in
antecedente, este adeseori prezenta tahicardia ventriculara cu
morfologii diferite. Ca rezultat, ablatia unei tahicardii ventriculare cu
o singura morfologie poate fi paliativa dar nu elimina
necesitatea dispozitivului sau tratamentului antiaritmic. La acesti
pacienti, tahicardia ventriculara isi poate avea originea in,
sau implica, zone extinse de miocard si eliberarea de curent de
radiofrecventa standard are o rata mica de succes.302-304
Data fiind heterogenitatea cicatricilor din tahicardia ventriculara
ischemica, tehnicile de mapping au evoluat luand in calcul natura
complexa a circuitelor, inclusiv regiunile bystander de conducere
anormala. Noul sistem de mapping tridimensional permite
reconstructia anatomica si corelarea caracteristicilor
electrofiziologice cu anatomia. Aceste sisteme au condus la intelegerea
mijloacelor prin care circuitele pot fi cartografiate in timpul ritmului
sinusal si pot facilita ablatia la pacientii ischemici care
adeseori nu tolereaza bine tahicardiile ventriculare.303,309-312
Utilizarea acestor tehnici poate duce la o rata mai buna a
succesului pe termen lung.313
6.6.5. Instrumente
aditionale ablatiei
In
functie de substratul aritmic, circuitele tahicardiei ventriculare pot fi
aproape de endocard sau se gasesc in profunzimea miocardului. Leziunea
focala produsa de sistemele de eliberare a curentului de
radiofrecventa traditional poate sa nu creeze leziuni
suficient de adanci pentru a penetra circuitele intramiocardice. Ca rezultat,
cateterele cu racire si irigare cu aolutie salina au fost
create si folosite pentru ablatia tahicardiei ventriculare.
Racirea varfului cateterului permite incalzirea tesutului in
profunzime. Rezultatele preliminare sunt promitatoare dar sunt
necesare date suplimentare. 314 O alta tehnica noua
implica accesul pericardic transtoracic pentru mapping si
ablatie. Aceasta tehnica a fost dezvoltata pentru a se
adresa tahicardiilor ventriculare care sunt extrem de profunde la nivelul
miocardului sau chiar epicardice. Implica inserarea unei teci la nivelul
spatiului pericardic si efectuarea cartografierii la nivel epicardic.206,315,316
Cateva centre aplica deja aceasta abordare. Aceasta tehnica
trebuie efectuata cu suport chirurgical disponibil daca e necesar
si trebuie luate precautii privind arterele coronare epicardice.317,318
O alta tehnica noua, neutilizata recent, este ablatia
chimica transcoronara a tahicardiei ventriculare incesante si a
fibrilatiei ventriculare.319,320 O tehnica si mai
recenta implica modularea maduvei spinarii pentru supresia
aritmiilor ventriculare.255-257 Studii aditionale au sugerat
ca ablatia cu cateter a fibrilatiei ventriculare pe cord
structural normal poate fi posibila prin tintirea triggerilor din
portiunea distala a sistemului Purkinje. Aceste tehnici sunt
considerate inalt experimentale.280,317,318,321
6.7. Chirurgia si
procedurile de revascularizare
Tratamentul
chirurgical pentru managementul aritmiilor ventriculare poate implica
ablatia sau rezectia chirurgicala a focarului aritmogen,
simpatectomie cardiaca sau rezectia anevrismului.
Revascularizatia coronariana chirurgicala sau percutanata
cu imbunatatirea fluxului sangvin coronarian si reducerea
ischemiei miocardice are efecte antiaritmice favorabile. (Vezi ghidul ACC/AHA
updatat in 2004 pentru bypass aorto-coronarian.322)
6.7.1. Chirurgia
antiaritmica
La
pacientii cu tahicardie ventriculara recurenta refractara
la tratamentul medicamentos, defibrilatoare implantate si ablatie cu
radiofrecventa, ablatia chirurgicala directa sau
rezectia focarului aritmogen este o abordare care continua sa
fie utilizata in centre experimentate. Interventia chirurgicala
necesita cartografierea precisa preoperator si intraoperator
pentru determinarea locului sau locurilor tahicardiei. Unele centre folosesc
abordarea bazata pe cicatrice pentru rezectia focarelor aritmogene.
Ratele de succes pe termen scurt si lung ale tratamentului chirurgical
ghidat de mapping pentru tahicardie ventriculara recurenta refractara
se bazeaza in principal pe datele vechi din literatura de specialitate
si doar cateva date sunt disponibile pentru evaluarea raportului
risc-beneficiu in zilele noastre la pacientii refractari la cateter
ablatie si implantare de defibrilator.323
Rezectia
ganglionului simpatic cardiotoracic stang a fost introdusa in 1971 pentru
tratamentul aritmiilor ventriculare amenintatoare de
viata declansate prin mecanism adrenergic asociate cu sindrom
QT lung.324 Aceasta procedura, efectuata prin
abordare supraclaviculara limitata, implica rezectia
jumatatii inferioare a ganglionului stelat stang si
indepartarea cel putin a ganglionilor simpatici toracici 2 si 3
localizati pe partea stanga.325 Acest tratament
chirurgical este asociat cu reducerea frecventei sincopei aritmogene in
acest sindrom si poate fi utila ca tratament adjuvant la
pacientii cu sindrom de QT lung cu risc mare care au sincopa
recurenta si/sau oprire cardiaca in ciuda combinarii
implantarii de defibrilator-cardioverter cu tratamentul betablocant sau
la pacientii cu sindrom de QT lung care nu pot tolera beta-blocantele.326
Anevrismul
miocardic mare secundar unui infarct miocardic se asociaza cu compromitere
hemodinamica si este frecvent insotit de aritmii ventriculare
majore. La pacienti selectionati, rezectia anevrismului
poate imbunatati functia cardiaca si,
alaturi de cartografierea electrofiziologica si rezectia
miocardului ventricular aritmogen, poate reduce sau elimina asocierea
aritmiilor ventriculare.327
6.7.2. Revascularizarea
pentru tratamentul aritmiei
La
pacientii cu aritmii ventriculare, evaluarea prezentei bolii
coronariene obstructive si ischemiei active este esentiala.
Revascularizarea coronariana implicand fie angioplastia percutana cu
balon/stent, fie bypass-ul este tratamentul antiischemic eficient. O revizuire
a studiilor privind revascularizarea coronariana releva
imbunatatirea supravietuirii si reducerea mortii
subite cardiace pe termen lung.328,329 Daca boala cardiaca
ischemica este complicata cu aritmii ventriculare, in special la pacientii
cu afectarea trunchiului coronarei stangi si LAD proximala, este
probabil rezonabil ca revascularizarea va reduce frecventa si
complexitatea aritmiei iar la cativa pacienti va elimina aceste
aritmii. Nici un trial controlat nu a evaluat efectele revascularizarii
miocardice asupra TV/FV. Totusi studii observationale sugereaza
ca:
TVSM
la pacientii post-IM este putin probabil sa fie afectata de
revascularizare.
Revascularizarea miocardica este improbabil sa
previna recurentele opririi cardiace la pacientii cu disfunctie
marcata de VS chiar daca aritmia apare ca rezultat al ischemiei
tranzitorii.
Discutii
suplimentare pot fi gasite in sectiunea 8.7.
Pentru
ca aritmiile ventriculare nu sunt reduse intotdeauna de revascularizare si pot fi de fapt exacerbate
de infarctul miocardic ocult din timpul procedurii, este indicata monitorizarea
atenta postprocedural pentru suprimarea aritmiilor. Suprimarea aritmiilor
ventriculare determinate de ischemie si imbunatatirea
supravietuirii asociata cu revascularizarea miocardica se poate
sa fi contribuit la lipsa eficacitatii ICD in Coronary Artery
Bypass Graft (CABG) Patch Trial.265 La pacientii cu
revascularizare miocardica dupa stop cardiac fara
legatura cu infarctul miocardic se recomanda implant de defibrilator
dupa revascularizare in contextul starii de risc presupus crescut.
Totusi este rezonabil sa nu se implanteze defibrilator daca
exista dovezi clare si directa de ischemie miocardica care a
precedat imediat debutul FV si nu exista dovezi de IM in antecedente
(vezi de asemenea sectiunile 8.1 si 8.3.).
7.
Managementul acut al aritmiilor specifice
7.1. Managementul stopului
cardiac
Oprirea
cardiaca este caracterizata prin pierderea brusca a fluxului
sanguin efectiv, suficient pentru a determina pierderea imediata a
constientei determinand decesul imediat daca este
netratata. Cele mai comune mecanisme electrice ale opririi cardiace sunt
FV si TV fara puls (vezi sectiunea 3), dar un numar
mare de stopuri cardiace incep cu bradiaritmii severe, asistola sau
activitate electrica fara puls. Probabilitatea de supravietuire
este mai buna la persoanele care prezinta TV/ FV decat la cei cu
bradiaritmii sau asistola. Raspunsul rapid este determinantul major
al supravietuirii.
Recomandari
Clasa I
Dupa stabilirea
prezentei stopului cardiac cert, suspectat sau iminent, prima prioritate
trebuie sa fie activarea unei echipe de raspuns capabila sa
identifice mecanismul specific si sa intervina prompt. (Nivel de
dovezi: B)
Resuscitarea
cardiopulmonara (RCP) trebuie inceputa imediat dupa contactarea echipei. (Nivel de
dovezi: A)
In
afara spitalului, daca este disponibil un DAE, trebuie aplicat imediat cu
administrarea socului conform algoritmului RCP descris de AHA in asociere
cu International Liaison Commitee on Resuscitation
(ILCOR) si/sau European Resuscitation
Council (ERC). (Nivel de dovezi: C)
Pentru
pacientii cu stop cardiac determinat de tahiaritmii ventriculare, cand
recurentele apar dupa socuri maximale (in general 360J pentru
defibrilatoarele monofazice), amiodarona i.v. trebuie sa fie
antiaritmicul preferat pentru a incerca obtinerea unui ritm stabil. (Nivel de dovezi: B)
Pentru
tahiaritmiile ventriculare recurente sau mecanismele non-tahiaritmice care
determina stopul cardiac, se recomanda urmarirea algoritmului
de RCP al AHA in asociere cu ILCOR si/sau al ERC. (Nivel de
dovezi: C)
Cauzele
reversibile sau factorii care contribuie la stopul cardiac trebuie tratate in
timpul suportului vital avansat, incluzand hipoxia, dezechilibre electrolitice,
factori mecanici si depletia volemica. (Nivel de
dovezi: C)
Clasa IIa
In
cazul raspunsului dincolo de primele 5 minute, o scurta (mai
putin de 90-180 sec) perioada de RCP este rezonabila inaintea
incercarii defibrilarii. (Nivel
de dovezi: B)
Clasa IIb
O
singura lovitura precordiala poate fi aplicata de
catre personalul medical care asista la un stop cardiac. (Nivel de dovezi: C)
Un
numar de strategii de raspuns la stopul cardiac neasteptat au
adus imbunatatirea probabilitatii supravietuirii.336
Totusi numarul absolut si proportia supravietuitorilor
raman reduse cu exceptia situatiilor rare cand exista un
raspuns rapid la pacientii cu TV/FV. Reducerea supravietuirii
dupa stop cardiac este de 7-10% pe minut daca RCP nu este
initiata si de 3-4% pe
minut cu RCP din partea martorilor stopului. Cand este disponibila
defibrilarea imediata in conditii corespunzatoare, ca de exemplu
in unitati de terapie intensiva si in laboratoarele de
EF, unde un timp de raspuns sub 30 sec este de obicei posibil,
supravietuirea dupa FV este peste 90%, exceptand pacientii cu
conditii fiziopatologice care favorizeaza persistenta acestei
aritmii potential fatale. Probabilitatea supravietuirii scade rapid
dupa 2 minute de la debutul stopului cardiac, astfel incat la 4-5 min
poate fi de 25% sau mai putin, iar
la 10 min este sub 10%. Studiile au aratat ca in timp ce defibrilarea
imediata este metoda preferata in primele 1-2 min dupa
aparitia stopului cardiac, o scurta perioada de RCP pentru a
sustine oxigenarea imbunatateste supravietuirea
cand timpul scurs pana la defibrilare este mai mare.338-340
Suportul
vital avansat, in afara celui legat direct de metodele electrice pentru
controlul tahiaritmiilor, presupune protocoale complexe de ghidare a
responderilor. Aceste documente, publicate de AHA334 si ERC335
acopera o intindere larga de circumstanter clinice
si mecanisme. Ele furnizeaza informatii despre management,
stratificate pentru circumstante speciale ca de pilda varsta victimei
(de la nou-nascuti la batrani), statusul fiziopatologic
si probabilitatea de supravietuire. Algoritmii raspunsului in
aceste circumstante variate sunt complicati; detalii se pot
gasi in documentele sursa.334,335 Ca ghiduri de
management, aceste documente sunt clasificate ca avand Nivel de Dovezi: C, dar
ele deriva din combinarea unor studii si opinii cu nivel variat de
dovezi: A, B sau C. Versiuni prescurtate pentru tahiaritmii si mecanisme
nontahiaritmice sunt descrise in Figura 3.
Consecvent
ghidului AHA/ERC 2005, valoarea energiei si timing-ul socurilor
pentru tratamentul TV cu puls sunt determinate de starea pacientului si
caracteristicile morfologice ale TV. TV monomorfa instabila este
tratata prin cardioversie, in timp ce TV polimorfa instabila
este tratata ca si FV folosind socuri asincrone la doze
defibrilatorii. TV monomorfa la pacienti cu puls raspunde in
general bine la socuri monofazice sincrone cu energie initiala
de 100 J sau mai mare. Sunt necesare mai multe date inainte de a formula
recomandari comparative specifice privind energia necesara pentru socurile
bifazice. Cardioversia sincrona nu este recomandata pentru
tratamentul TV polimorfe instabile datorita sincronizarii incerte
cu complexul QRS fiind recomandate socurile electrice asincrone la doze
defibrilatorii. Daca exista orice indoiala asupra formei de TV
prezenta la un pacient instabil, socul nu trebuie intarziat pentru
analiza detaliata a ritmului. Energia socului recomandata
initial pentru un defibrilator bifazic este de 150-200 J (se vor folosi
energiile recomandate de producator; in absenta recomandarilor,
se pot utiliza 200 J) si o doza egala sau mai mare este
recomandata pentru socurile urmatoare. Daca se utilizeaza
un defibrilator monofazic energia este de 360 J pentru toate socurile.
Doze mai mici de energie nu trebuie folosite pentru socurile asincrone
pentru ca pot provoca FV cand se administreaza asincron. Dupa
eliberarea socului, reanimatorul trebuie sa fie pregatit pentru
RCP si sa respecte algoritmul ACLS pentru stopul fara puls
daca acesta apare (Figura 3).
Scopurile
generale ale suportului vital avansat sunt de a stabiliza un ritm eficient
hemodinamic, a optimiza ventilatia, a mentine si sustine
circulatia reluata. In timp ce in versiunea anterioara a ghidului ECC341
erau recomandate 3 socuri succesive, acum este recomandata o
strategie cu un soc pentru a reduce timpul dintre compresiile toracelui,
eliberarea socului si reluarea compresiilor6,334,335
(vezi Figura 3). Epinefrina, 1 mg i.v., este administrata si
urmata de repetarea defibrilarii cu 360 J. Epinefrina se poate
readministra la intervale de 3-5 min cu defibrilare intre doze, dar dozele mari
de epinefrina nu par sa aduca beneficii suplimentare.342
Amiodarona
i.v. a inlocuit lidocaina i.v. si alte medicamente antiaritmice pentru
tratamentul tahiaritmiilor ventriculare rezistente si repetate.343
Amiodarona nu trebuie administrata de rutina la pacientii care
raspund la prima defibrilare cu un ritm stabil. Daca sunt dovezi
clinice suficiente ca stopul cardiac a survenit in cadrul unui SCA, se
poate administra lidocaina i.v. pentru aritmiile rezistente.
Betablocantele pot fi preferate in cazul SCA daca nu au fost deja
administrate. Pentru suportul hemodinamic in managementul stopului cardiac,
vasopresina a fost propusa ca alternativa la epinefrina,344
dar superioritatea acesteia nu a fost clar stabilita. Managementul
stopului cardiac nontahiaritmic se
focalizeaza pe controlul factorilor metabolici si tranzitori care
pot precipita evenimentele bradiaritmice sau activitatea electrica
fara puls (Figura 3).
Simultan
reanimatorul trebuie sa se concentreze asupra ventilatiei pentru a
corecta dezechilibrele sanguine, asupra eforturilor de creste
probabilitatea de obtinerii ritmului stabil
(imbunatatirea oxigenarii, corectarea acidozei,
imbunatatirea starii EF). Desi oxigenarea sanguina
adecvata este cruciala in managementul imediat al acidozei
metabolice din stopul cardiac, corectarea suplimentara poate fi
realizata la nevoie prin administrarea i.v. a bicarbonatului de sodiu.
Aceasta este recomandata pentru situatiile cand se cunosc sau sunt
suspectate cauze preexistente de
acidoza corectabila cu bicarbonat, unele supradozari
medicamentoase si in resuscitarea prelungita.334 Un rol
mai general al bicarbonatului in timpul stopului cardiac a fost pus la indoiala;
dar oricum, pentru corectarea acidozei in aceste conditii sunt necesare
doze mult mai mici de bicarbonat de sodiu decat se recomanda anterior. Cantitatile
excesive pot fi periculoase.
La
pacientii la care hiperpotasemia acuta este factorul determinant
pentru FV rezistenta, sau la cei care au hipocalcemie sau supradozaj cu
blocanti ai canalelor de calciu, calciul gluconat 10%, 5-20 ml administrat
in ritm de 2-4 ml/min, poate fi de ajutor.334 Calciul nu trebuie
utilizat de rutina in timpul resuscitarii, chiar daca nivelul
Ca2+ ionizat poate fi scazut. Unele forme rezistente de TV
polimorfa sau torsada varfurilor, TV monomorfa rapida sau
flutter ventricular (frecventa mai mare sau egala cu 260/min),
sau FV rezistenta pot raspunde la administrarea i.v. de betablocante
(propranolol 1 mg i.v. bolusuri pana la doza totala de 15-20 mg;
metoprolol 5 mg i.v., pana la 20 mg) sau MgSO4 (1-2 g i.v. in
1-2 min).
Abordarea
pacientilor cu bradiaritmii, asistola sau activitate electrica
fara puls este diferita de cea a pacientilor cu evenimente
tahiaritmice ca TV/FV.334 Odata ce aceasta forma de
stop cardiac este recunoscuta, eforturile trebuie concentrate initial
asupra stabilirii controlului statusului cardiorespirator (RCP continua,
intubare, stabilirea abordului venos), apoi reconfirmarea ritmului (in 2
derivatii daca este posibil) si in final asupra actiunilor
care favorizeaza ritmul stabil spontan sau incercarilor de pacing. Cauzele
potential reversibile, in special pentru bradiaritmii si
asistola, trebuie considerate si excluse (sau tratate) cu
promptitudine. Acestea includ: embolia pulmonara, IMA, hipovolemia,
hipoxia, tamponada cardiaca, pneumotoraxul in tensiune, acidoza preexistenta,
supradozajul medicamentos, hipotermia si hiperpotasemia. Pacingul cardiac
pentru stopul bradiaritmic sau asistola este de obicei ineficace,334
dar corectarea hipoxemiei, acidozei, dezechilibrelor electrolitice poate ajuta
in unele cazuri. Epinefrina (1 mg i.v. la fiecare 3-5 min) este obisnuit
utilizata in incercarea de a obtine activitate electrica
spontana sau pentru cresterea frecventei bradicardiei. Pentru
asistola si activitatea electrica fara puls, se
recomanda atropina 1 mg intravenos sau intraosos, repetat la fiecare
3-5 min pana la 3 doze, sau 0,03-0,04 mg/kg. Pentru bradicardie, se recomanda
atropina 0,5 mg i.v./i.o., repetat la 3-5 min pana la doza totala de 0,04 mg/kg.
Bicarbonatul de sodiu, 1 mEq/kg, poate fi incercat cand este cunoscuta sau
suspectata hiperpotasemia sau acidoza responsiva la bicarbonat.
7.1.1. Aritmiile asociate cu
sindroamele coronariene acute
Pentru
recomandari, vezi sectiunea 7.1. din ghidul actual si ghidurile
curente de ACLS.334,335 SCA pot determina aritmii
amenintatoare de viata care pot fi prima manifestare a
ischemiei. Mecanismele acestor aritmii pot fi diferite de cele din boala
cardiaca iscemica stabila. Aritmiile din ischemia acuta pot
fi prin reintrare, automatism anormal sau prin activitate declansata
si sunt influentate de o varietate de factori endogeni cum ar fi
nivelul potasiului seric sau statusul autonom. Aceste aritmii pot fi cauza
multor morti subite la pacientii cu sindroame ischemice. FV sau TV
sustinuta au fost raportate in pana la 20% din IMA.346,347
Incidenta
FV (aparuta in primele 48 ore de la debutul SCA) a scazut probabil
datorita revascularizarii agresive care limiteaza marimea
infarctului si cresterii utilizarii betablocantelor.348
FV aparuta precoce in SCA a fost asociata cu cresterea
mortalitatii intraspitalicesti dar nu cu cresterea
mortalitatii pe termen lung.346 Profilaxia cu
lidocaina poate reduce incidenta FV din SCA dar pare a fi
asociata cu cresterea mortalitatii probabil datorita
bradicardiei si acest tratament a fost in mare masura abandonat.349
Folosirea profilactica a betablocantelor IMA reduce incidenta FV
si aceasta practica este incurajata cand este cazul.
Similar, corectarea hipomagneziemiei si hipopotasemiei este
incurajata datorita contributiei potentiale ale
perturbarilor electrolitice la FV.350
Date
recente arata beneficiul eplerenonei, antagonist aldosteronic, in
reducerea riscului mortalitatii prin MSC cu 37% (p=0,051) la 30 zile
dupa randomizare la pacientii cu IMA (cand tratamentul a fost
initiat in medie la 7,3 zile dupa IMA), aditional tratamentului
conventional al pacientilor cu FEVS mai mica sau egala cu
40% si semne de IC.351

Figura 3. Algoritm de suport vital avansat
pentru stopul fara puls. Republicat din Circulation 2005;112:IV5766.
DAE, defibrilator automat extern; BLS, basic life support suport vital de
baza; RCP, resuscitare cardiopulmonara; iv/io, intravenos/intraosos;
AEP, activitate electrica fara puls; FV, fibrilatie
ventriculara; TV, tahicardie ventriculara.
7.1.1.1. Tahicardia
ventriculara fara puls/fibrilatia ventriculara
In FV
sau TV fara puls din SCA protocolul standard ACLS este initiat,
incluzand socul electric asincron urmand evaluarii fundamentale a
respiratiei si initierii RCP. Defibrilarea consta intr-unul
sau mai multe socuri electrice monofazice de 360 J, sau bifazice cu doza
recomandata de producatorul defibrilatorului ca fiind eficienta.
Daca nu sunt disponibile aceste informatii, se recomanda 200 J
pentru primul soc si o doza mai mare sau egala pentru
socurile urmatoare. Energia optima pentru socurile bifazice
nu a fost determinata si nu se pot face recomandari la acest
moment privind tipul undei de soc sau amplificarii nivelului
energiei. Daca restabilirea ritmului normal nu este realizata prin
defibrilare se urmareste protocolul ACLS al TV fara puls
sau FV. Acesta include epinefrina (1 mg i.v. la fiecare 3-5 min) sau
vasopresina (40 U i.v. o sigura data; o doza de vasopresina
i.v./i.o. poate inlocui fie prima fie a doua doza de epinefrina)
si amiodarona (300 mg sau 5 mg/kg i.v. rapid, cu posibila repetare
150 mg i.v. rapid o singura data) sau ca a doua linie lidocaina
(1-1,5 mg/kg cu repetare 0,5-0,75 mg i.v./i.o. pana la doza totala de 3
mg/kg). Tratamentul de linia a doua poate include Mg i.v. (1-2 g) sau
procainamida (30mg/min pana la 17 mg/kg). Ultima este considerata
acceptabila dar nu mai este recomandata.334
Dupa
resuscitarea FV, administrarea profilactica de medicamente, de obicei
amiodarona si betablocant poate fi continuata. Antiaritmicul ar
trebui oprit cand se considera necesar, pentru evaluarea recurentei
aritmiei.
7.1.1.2. Ritmul
idioventricular si tahicardia ventriculara nesustinuta
Nici
ritmul idioventricular, nici TVNS (dureaza mai putin de 30 sec)
aparute in SCA nu sunt markeri predictivi de incredere pentru FV precoce.
De fapt, ritmul idioventricular accelerat a fost asociat cu reperfuzia.352
Astfel, aceste aritmii nu justifica tratamentul antiaritmic profilactic.
Totusi, TV sustinuta si/sau cu deteriorare
hemodinamica in SCA necesita tratament supresiv.2 Managementul
TV fara puls urmareste recomandarile ghidului ACLS pentru
TV fara puls/FV.
7.1.1.3. Tahicardia
ventriculara sustinuta instabila
Pentru
TV recurenta, daca TV este monomorfa si FE este
normala, procainamida, sotalolul, amiodarona sau lidocaina pot fi
utilizate. Alternativ, daca FE este scazuta, se recomanda
amiodarona sau lidocaina (amiodarona 150 mg i.v. timp de 10 min sau lidocaina
0,5-0,75 mg/kg i.v. rapid). Daca TV este polimorfa si intervalul
QT de baza este normal se pune accent pe corectarea ischemiei si
dezechilibrelor electrolitice. Aceasta poate fi urmata, sau
insotita de administrarea de betablocant, amiodarona, procainamida
sau sotalol. Daca TV este polimorfa si FE scazuta se
recomanda tratamentul cu amiodarona 150 mg i.v. in 10 min sau
lidocaina 0,5-0,75 mg/kg i.v. rapid. In TV polimorfa, daca
intervalul QT de baza este lung, se recomanda corectarea electrolitica
iar alte tratamente pot include: magneziu, pacing overdrive, ispoproterenol,
fenitoina sau lidocaina.
7.1.1.4. Bradicardia si
blocurile
Bradicardia
si blocurile pot apare ca urmare a infarctului miocardic. Probabilitatea
de a dezvolta bloc complet ca o complicatie a IM creste in
prezenta unei tulburari preexistente a sistemului de conducere.
Aparitia blocurilor ca rezultat al IM a fost asociata cu cresterea
mortalitatii intraspitalicesti dar nu influenteaza mortalitatea
pe termen lung.353 Cresterea mortalitatii in spital
este legata de gradul mare de afectare miocardica necesar pentru a
dezvolta blocul, mai degraba decat de prezenta blocului in sine. In
timp ce pacingul nu a crescut supravietuirea pe termen lung post-IM, este
inca indicat in bradiaritmiile simptomatice asociate cu IMA, iar
recomandarile sunt cele din 2004 ACC/AHA Guidelines for the Management
of Patients With STElevation Myocardial Infarction2 si
ACC/AHA/NASPE 2002 Guidelines Update for Implantation of Cardiac Pacemakers
and Antiarrhythmia Devices.1
7.1.2. Tahicardia
ventriculara asociata infarctului miocardic cu troponina
mica
Recomandari
Clasa I
Pacientii
cu TV sustinuta la care sunt documentate cresteri cu nivel
scazut al biomarkerilor de leziune/necroza miocardica trebuie
tratati similar cu pacientii cu TV sustinuta la care nu
este documentata cresterea biomarkerilor. (Nivel de Dovezi: C)
Episoadele
prelungite de TV monomorfa sustinuta pot fi asociate cu
cresterea biomarkerilor miocardici datorita cererii metabolismului miocardic
crescute fata de oferta, in special la pacientii cu
boala coronariana. Acesti pacienti au de obicei antecedente
de infarct miocardic. Este rezonabil de evaluat ischemia miocardica la
pacientii cu aceste constatari. Cand TV sustinuta este
insotita de cresterea modesta a enzimelor cardiace nu
trebuie presupus ca un nou IM a cauzat tahicardia. In absenta altor
date, trebuie considerat ca pacientul cu TV sustinuta
monomorfa are risc de TV recurenta si trebuie tratat pentru
aceasta aritmie in aceeasi maniera ca pacientii
fara eliberare de biomarkeri ce acompaniaza TV.
7.2. Tahicardia
ventriculara
monomorfa sustinuta
Recomandari
Clasa I
Tahicardia cu QRS larg
trebuie considerata a fi TV daca diagnosticul este neclar. (nivel de dovezi: C)
Cardioversia
electrica cu sedare corespunzatoare este recomandata in orice
moment al cascadei tratamentului la pacientii suspecti de TV monomorfa
sustinuta cu compromitere hemodinamica. (nivel de dovezi: C)
Clasa IIa
Procainamida intravenos
(sau ajmalina in unele tari europene) este rezonabila pentru tratamentul
initial al pacientului cu TV monomorfa stabila. (nivel de dovezi: B)
Amiodarona
intravenos este rezonabila la pacientii cu TV monomorfa
sustinuta instabila hemodinamic, refractara la conversia
cu soc electric sau recurenta in ciuda administrarii
procainamidei sau altor agenti. (nivel
de dovezi: C)
Pacingul
prin cateterizare transvenoasa poate fi util in tratamentul
pacientilor cu TV monomorfa sustinuta refractari la
cardioversie sau frecvent recurenta in ciuda medicatiei
antiaritmice. (nivel de dovezi: C)
Clasa IIb
Lidocaiana
intravenos poate fi rezonabila pentru tratamentul initial al
pacientilor cu TV monomorfa sustinuta stabila specific
asociata cu ischemie sau infarct miocardic acut. (nivel de dovezi: C)
Clasa III
Blocantii
de canal de calciu ca verapamilul sau diltiazemul nu trebuie folositi la
pacienti pentru a stopa tahicardia cu QRS larg de origine necunoscuta,
in special la pacientii cu disfunctie miocardica in antecedente.
(nivel de dovezi: C)
Conversia
electrica este intotdeauna indicata in tahicardia instabila
hemodinamic. Managementul pacientilor cu tahicardie cu QRS larg bine
tolerata hemodinamic, este facilitata de diferentierea intre
TV, TSV cu conducere aberanta si tahicardia prin preexcitatie.354
Aceasta poate fi realizata cu date din anamneza si examinarea
ECG cu 12 derivatii in timpul tahicardiei. Statusul hemodinamic al
pacientilor nu este de ajutor pentru diferentierea mecanismului.
Un diagnostic de lucru de TV este util cand diagnosticul este neclar pentru
ca TV este mai frecventa, in special la cei cu boala
cardiaca structurala, si terapia adresata necorespunzator
TSV, poate avea consecinte nedorite.355,356 TV monomorfa
este in general in relatie cu o anomalie structurala precum
cicatricea post-IM, dar poate avea mecanisme heterogene. Unele TV idiopatice
raspund bine si se intrerup la verapamil si adenozina i.v.
si medicii cu experienta in managementul aritmiilor pot alege
sa trateze un astfel de episod cu acesti agenti.357,358
Daca aceste entitati de TV nu pot fi recunoscute, este mai
prudent sa presupunem ca este vorba de TV in relatie cu boala
cardiaca structurala.
Corectarea
potentialelor cauze sau cauze agravante cum ar fi hipopotasemia si ischemia
este o prioritate importanta. Stoparea rapida a aritmiei este de
dorit chiar daca TV este bine tolerata. Aceasta poate fi
obtinuta cu cardioversie, medicamentos sau pacing. Cardioversia,
chiar si in stadii precoce sau de prima intentie este rezonabila.359,360
Avantajele includ absenta proaritmiei si eficacitatea inalta.
Cardioversia nu previne recurenta si un dezavantaj major este nevoia
de sedare profunda sau anestezie. Trebuie luate masuri de
siguranta daca pacientul are si FA concomitenta (ex,
tahicardie dubla) in astfel de cazuri poate fi urmarit ghidul 2006
ACC/ AHA/ESC pentru tratamentul pacientilor cu fibrilatie
atriala.361
Tratamentul
initial include frecvent administrarea intravenoasa a medicamentelor
antiaritmice. Avantajul este evitarea anesteziei si buna disponibilitate.
Dezavantajul include intarzierea conversiei, esecul iesirii din TV
la unii pacienti si efecte adverse ca hipotensiunea si
proaritmia. Desi unele medicamente ca flecainida, propafenona si
sotalolul sunt disponibile ca preparate i.v. in unele tari, numai
amiodarona, lidocaina si procainamida sunt larg disponibile. Ajmalina
i.v. este frecvent utilizata in unele tari europene.
Incarcarea cu amiodarona i.v. s-a dovedit utila in TV
recurenta si instabila, in special cand TV e recurenta
dupa soc si alte masuri antiaritmice.362-366
Este de asemeni rezonabila la pacientii la care va fi nevoie de
administrare orala ulterioara. S-a dovedit superioara
lidocainei in imbunatirea supravietuirii la pacientii cu
stop cardiac si FV rezistenta la soc.343 Desi
amiodarona i.v. are efect precoce pe conducerea nodului AV si efecte
antiadrenergice precoce, efectele pe conducerea miocardica si
refractaritate se instaleaza treptat si efectul maxim poate fi
vazut in saptamani-luni.367-369 Amiodarona
intravenos nu este ideala in conversia precoce a TV monomorfa
stabila. Procainamida i.v. este mult mai potrivita daca se
doreste incetinirea frecventei TV si oprirea ei rapida.370,371
Este recomandata monitorizarea tensiunii arteriale si statusului
cardiovascular in prezenta IC congestive sau disfunctiei VS severe
pentru ca administrarea procainamidei i.v. determina hipotensiune
tranzitorie.372 Lidocaina este eficienta in TV asociata
ischemiei miocardice.373,374
7.3. Tahicardia
ventriculara
monomorfa repetitiva
Recomandari
Clasa IIa
Amiodarona
i.v., betablocantele si procainamida i.v. (sau sotalolul ori ajmalina in
Europa), pot fi utile in tratamentul TV monomorfe repetitive in contextul
bolii coronariene375 si TV idiopatice. (nivel de dovezi: C)
Tahicardia
ventriculara monomorfa repetitiva se caracterizeaza ECG
prin ectopie ventriculara frecventa si salve de TVNS cu
intercalarea ritmului sinusal. Tipic apare in repaus si este
autolimitata dar aritmia poate dura si mai mult.376
Desi aceasta terminologie se poate aplica la aritmii cu diferite
mecanisme, se refera in general la TV idiopatica, foarte frecvent
tipul din tractul de iesire al VD.377-379 Acesta
tahicardie cauzeaza palpitatii sau, rar, tahicardiomiopatie.380
Multi pacienti nu au nici o simptomatologie data de aritmie. La
unii pacienti tahicardia este provocata de efort.297 Este
mai putin frecventa la pacientii cu boala cardiaca
structurala si, specific, post infarct.375
Tratamentul
este rareori necesar de urgenta si managementul cronic se
bazeaza pe simptome si frecventa TV. Cardiomiopatia indusa
de tahicardie este neobisnuita pentru aceasta entitate si
de obicei nu este nevoie de tratament la pacientii asimptomatici cu
functie VS conservata. Pentru pacientii cu simptome moderate,
linistirea poate fi singurul tratament necesar. Tahicardia
ventriculara monomorfa repetitiva este o problema de
management cronic (farmacologic sau prin ablatie) si strategia
variaza considerabil dependent de situatia clinica si
etiologia TV. Agentii betablocanti sau calciu-blocanti sunt
frecvent eficienti. Ablatia este in general reusita in
tahicardia din tractul de ejectie al VD.381 Cand tratamentul
acut este necesar, medicatia antiaritmica este selectata in
functie de etiologie si functia ventriculara
subiacenta, cu consideratii de selectare a medicamentelor similare
cu cele descrise la TV monomorfa sustinuta (vezi sectiunea
7.2.).
7.4. Tahicardia
ventriculara polimorfa
Recomandari
Clasa I
Cardioversia
electrica cu sedare corespunzatoare este recomandata la
pacientii cu TV polimorfa sustinuta cu compromitere
hemodinamica si este rezonabila in orice moment al cascadei de
tratament. (nivel de dovezi: C)
Betablocanele
i.v. sunt utile la pacientii cu TV polimorfa recurenta, in
special daca ischemia este suspectata sau nu poate fi exclusa. (nivel de dovezi: C)
Incarcarea
i.v. cu amiodarona este utila la pacientii cu TV polimorfa
recurenta in absenta anomaliilor de repolarizare ca SQTL congenital
sau dobandit. (nivel de dovezi: C)
Angiografia
urgenta in vederea revascularizarii trebuie avuta in vedere la
pacientii cu TV polimorfa cand ischemia miocardica nu poate fi
exclusa. (nivel de dovezi: C)
Clasa IIb
Lidocaina
i.v. poate fi tratament rezonabil in TV polimorfa in special asociata
ischemiei acute sau infarctului miocardic acut. (nivel de dovezi: C)
TV
polimorfa poate fi sustinuta, necesitand cardioversie
urgenta, sau autolimitata cu interpunerea ritmului sinusal. Este util
de diferentiat TV polimorfa cu repolarizare normala de cea
asociata cu repolarizare anormala (ex, interval QT lung). Pot fi
similare, cu mari neregularitati in frecventa si morfologia
QRS cu cresterea si descresterea fazica a amplitudinii
QRS, frecvent descrise ca torsada de varfuri. TV polimorfa cu intervalul
QT normal in timpul intercalarii ritmului sinusal este intalnita cel
mai frecvent in contextul ischemiei acute sau IM, dar aspectul QRS in timpul TV
nu este specific si poate fi observat in cadrul altor boli cardiace cum ar
fi cardiomiopatia sau insuficienta cardiaca, sau in absenta unei
boli cardiace (ex, TV polimorfa idiopatica, TV
catecolaminergica).15, 382, 383 Betablocantele i.v. sunt utile
in acest context si scad mortalitatea in TV polimorfa cu IMA.384
Incarcarea i.v. cu amiodarona este de asemenea utila.341,385,386
Angiografia coronariana de urgenta trebuie luata in
consideratie in TV polimorfa recurenta cand ischemia este
suspicionata sau nu poate fi exclusa.387 In toate
situatiile, tratamentul insuficientei cardiace si al
conditiilor corectabile asociate si repletia cu potasiu si
magneziu trebuie realizate concomitent cu cele de mai sus.
7.5. Torsada varfurilor
Recomandari
Clasa I
Inlaturarea
oricaror medicamente daunatoare si corectarea anomaliilor
electrolitice este recomandata la pacientii cu torsada de
varfuri. (nivel de dovezi: A)
Pacingul
temporar si pe termen lung este recomandat la pacientii cu
torsada de varfuri datorata blocului si brahicardiei
simptomatice. (nivel de dovezi: A)
Clasa IIa
Tratamentul cu sulfat de
magneziu i.v. este rezonabil pentru pacientii cu QT lung si cateva
episoade de torsada. Magneziul nu pare sa fie eficient la
pacientii cu interval QT normal. (nivel
de dovezi: B)
Pacingul
temporar si pe termen lung este rezonabil la pacientii cu torsada
recurenta dependenta de pauze. (nivel
de dovezi: B)
Betablocantele
si pacingul sunt rezonabile ca tratament de urgenta pentru
pacientii cu torsada si bradicardie sinusala. (nivel de dovezi: C)
Isoproterenolul
este rezonabil ca tratament temporar in faza acuta la pacientii
torsada recurenta dependenta de pauza, care nu au SQTL
congenital. (nivel de dovezi: B)
Clasa IIb
Repletia cu potasiu
la 4,5-5 mmol/l poate fi eficienta la pacientii care prezinta
torsada de varfuri. (nivel de
dovezi: B)
Lidocaina
i.v. sau mexiletina oral pot fi considerate la pacientii cu torsada
de varfuri si LQT3. (nivel de
dovezi: C)
Alungirea
marcata a intervalului QT si TV polimorfa morfologic
distincta ca torsada de varfuri apar in 3 situatii: sindrom de
QT lung congenital, forme induse medicamentos, boala a sistemului de
conducere avansata care a progresat la bloc. (vezi sectiunea
11.1.1). Torsada de varfuri complicand un bloc se trateaza prin stimulare
temporara urmata de stimulare definitiva. Alte cauze, precum tulburari
electrolitice grave sau afectarea sistemului nervos central sunt mai putin
frecvente. Torsada de varfuri in episoade recurente frecvente in sindroamele
congenitale este neobisnuita. In aceste cazuri cotecolaminele trebuie
evitate. Totusi, alte manevre utile in formele medicamentos-induse
(magneziu, potasiu, pacing) pot fi folosite, iar pacingul impreuna cu
betablocantele sau lidocaina pot fi luate in considerare.388
7.6 Tahicardia
ventriculara incesanta
Recomandari
Clasa I
Revascularizarea
si betablocantele urmate de medicamente antiaritmice intravenos ca procainamida
sau amiodarona sunt recomandate la pacientii cu TV poliforma
incesanta sau recurenta datorate ischemiei miocardice acute. (nivel de dovezi: C)
Clasa IIa
Amiodarona
intravenos sau procainamida urmata de ablatia tahicardiei
ventriculare pot fi eficace in tratarea pacientilor cu TV monoforma
incesanta sau recurenta. (nivel
de dovezi:C)
Clasa IIb
Amiodarona intravenos
si betablocantele intravenos, separat sau impreuna, pot fi administrate
la pacientii cu furtuna TV. (nivel
de dovezi: C)
Pacing
overdrive sau anestezia generala pot fi rezonabile la pacientii cu TV
incesanta sau frecvent recurenta. (nivel de dovezi: C)
Modularea
maduvei spinarii poate fi tentata la pacientii cu TV
incesanta sau frecvent recurenta. (nivel de dovezi: C)
7.6.1. Aspecte clinice
Sindromul
cu episoade foarte frecvente de TV care necesita cardioversie a fost
denumit furtuna TV (vezi sectiunea 13.5). O alta varianta o
reprezinta socurile adecvate frecvente date de ICD. Desi a fost
definita ca mai mult de 2 episoade in 24 de ore,389,390 pot
apare mult mai multe asemenea episoade. TV cu durata de cateva ore
hemodinamic stabila a fost numita incesanta. Indicatiile
ghidurilor pentru aceste situatii se bazeaza pe dovezi anecdotice
deoarece sunt rare, au mecanisme potentiale multiple si nu
exista trialuri randomizate.
O
afectare cardiaca severa subiacenta este frecvent prezenta.
Mai rar furtuna TV poate apare (ex, in sindromul Brugada, SQTL, tahicardia
ventriculara catecolaminergica, sau in supradozajul medicamentos)
la pacientii cu cord normal. Furtuna TV poate fi monomorfa sau
polimorfa. Furtuna TV poliforma la un pacient coronarian este
puternic sugestiva pentru ischemia miocardica acuta; pauze pot
apare inaintea tahicardiei ventriculare polimorfe chiar in absenta
alungirii QT. TV dependenta de pauze cu alungire marcata a QT trebuie
tratata ca torsada de varfuri (vezi sectiunea 7.5), desi
si ischemia acuta se poate manifesta astfel. Frecvente socuri
adecvate ale defribilatorului pot fi expresia unei afectari cardiace
avansate si pot sau nu sa prevesteasca o deterioare
importanta a prognosticului.392
7.6.2. Tratamentul
Primul
pas in furtuna TV este identificarea si corectarea factorilor
declasantori, incluzand medicamente, tulburari electrolitice,
ischemia miocardica acuta (vezi sectiunea 13.5 si 13.6).
In cazul socurilor frecvente ale ICD electrocardiogramele si
programarea trebuie revazute pentru a stabili daca se indica reprogramarea
defibrilatorului.393,394
Betablocantele
intravenos trebuie considerate in furtuna TV poliforma fiind singura
terapie mai eficienta. Revascularizarea de urgenta poate fi
necesara. Este foarte important sa intelegem substratul
aritmiei, pentru ca odata diagnosticul stabilit tratamentul
tintit poate fi posibil. De exemplu in sindromul Brugada chinidina sau
isoproterenolul pot opri aritmiile incesante.139,395 In ischemia
acuta, amiodarona intravenos pare sa fie mai eficienta decat
alte antiaritmice.396
Contrapulsatia
intraaortica cu balon poate fi incercata. Pacing poate fi util in
special daca debutul tahicardiei este dependent de pauze. Alte terapii
potentiale includ ablatia397 sau anestezia generala.398
Poate fi incercata alternativa autonomica cu modularea
maduvei spinarii.
Furtuna
TV monoforma poate fi tratata cu antiaritmice intravenos (ex,
amiodarona, procainomida) pentru a scadea frecventa
ventriculara, dar acestea pot agrava tahicardia prin promovarea episoadelor
frecvente sau incesante. Ablatia poate fi eficienta. Implantarea de
defibrilator poate fi necesara eventual.
8. Aritmiile
ventriculare si moartea subita cardiaca legate de patologie
specifica
8.1. Disfunctia
ventriculara stanga postinfarct miocardic
Recomandari
Clasa I
Trebuie tratata
agresiv insuficienta cardiaca care poate apare la unii pacienti
cu disfunctie ventriculara stanga post-IM si tahiaritmii
ventriculare (nivel de dovezi: C)
Tratament
agresiv al ishemiei miocardice care poate fi prezenta la unii
pacienti cu tahiaritmii ventriculare. (nivel
de dovezi: C)
Revascularizarea
coronariana este indicata in vederea reducerii riscului de MSC la
pacientii cu fibrilatie ventriculara, cand exista dovezi
documentate, directe, clare ca ischemia acuta miocardica a
precedat imediat debutul fibrilatiei ventriculare. (nivel de dovezi: B)
Daca
revascularizarea coronariana nu poate fi efectuata si
exista dovezi ale unui IM si disfunctie ventricualara
stanga semmnificativa, prima terapie a pacientilor
resuscitabili pentru FV trebuie sa fie ICD la pacientii care primesc
terapie medicala optima si care au o speranta de
viata rezonabila, cu un status functional bun pentru mai
mult de 1 an. (nivel de dovezi: A)
Impantarea
de defibrilator este recomandata pentru preventia primara pentru
a reduce mortalitatea totala prin reducerea MSC la pacientii cu
disfunctie ventriculara stanga post-IM care sunt la cel
putin 40 zile post IM, au FE ≤30%-40%, sunt in clasa NYHA II
sau III, primesc terapie optima medicamentoasa si au
speranta rezonabila de supravietuire cu un status
functional bun pentru cel putin 1 an. (nivel de dovezi: A) (vezi sectiunea 1.2)
ICD
este terapia eficienta pentru reducererea mortalitatii prin
reducerea MSC la pacientii cu disfunctie ventriculara
stanga post-IM, care se prezinta cu TV sustinuta
instabila hemodinamic, sub terapie medicamentoasa cronica
optima, si care au speranta de viata rezonabila,
cu un status functional bun pentru cel putin 1 an. (nivel de dovezi: A)
Clasa IIa
Implantarea unui ICD
este rezonabila la pacientii cu disfunctie ventriculara
stanga post-IM, la cel putin 40 de zile postinfarct, care au FE
≤30%-35%, in clasa functionala NYHA I, cu terapie
medicamentoasa optima si care au speranta de viata
rezonabila, cu un status functional bun pentru cel putin 1 an. (nivel de dovezi: B) (vezi sectiunea
1.2)
Amiodarona,
adesea in combinatie cu betablocantele, poate fi utila la
pacientii cu disfunctie ventriculara stanga post-IM, cu
simptome date de TV neresponsiva la agentii betablocanti. (nivel de dovezi: B)
Sotalolul
se poate administra pentru reducerea simptomelor induse de TV pentru pacientii
cu disfunctie ventriculara stanga post-IM, care nu raspund
la agentii betablocanti. (nivel
de dovezi: C)
Terapiile
asociate defibrilatorului implantabil, incluzand ablatia prin
radiofrecventa sau rezectie chirurgicala si terapia
medicamentoasa cu agenti ca amiodarona sau sotalolul sunt
rezonabile pentru imbunatatirea simptomatologiei data de episoadele
frecvente de TV sustinuta sau fibrilatie ventriculara la
pacientii cu disfunctie ventriculara stanga post-IM. (nivel de dovezi: C)
Amiodarona
este recomandata pentru reducerea simptomelor date de TV recurente stabile
hemodinamic la pacientii cu disfunctie ventriculara stanga
post IMA la care nu se poate sau refuza implantarea unui defibrilator. (nivel de dovezi: C)
Implantarea
de defibrilator este rezonabila pentru tratamentul TV recurente la
pacientii post-IM cu functie ventriculara normala sau
aproape normala si care au speranta de viata
rezonabila, cu un status functional bun pentru cel putin 1 an. (nivel de dovezi: C)
Clasa IIb
Ablatia
curativa prin radiofrecventa sau amiodarona pot fi utilizate
in locul terapiei cu defibrilator implantabil pentru a
imbunatatii simptomatologia la pacientii cu disfunctie
ventriculara stanga post-IM cu TV recurenta hemodinamic
stabila care au FE >40%. (nivel
de dovezi: B).
Amiodarona
poate fi indicata la pacientii cu disfunctie ventriculara
stanga post-IM cu indicatie pentru defibrilator implantabil, precizata
mai sus, pacienti la care nu se poate sau refuza implantarea de
defibrilator. (nivel de dovezi: C)
Clasa III
Terapia
antiaritmica profilactica nu este indicata pentru reducerea mortalitatii
la pacientii cu aritmii ventriculare nesustinute, asimptomatici. (nivel de dovezi: B)
Antiaritmicele
de clasa IC nu trebuie utilizate la pacientii cu istoric de infarct
miocardic. (nivel de dovezi: A)
Elementele
luate in considerare de comitet pentru formularea recomandarilor din
acest capitol sunt discutate detaliat in Introducere.
Pacientii
cu boala coronariana cronica prezinta 3 tipuri generale de
tahiaritmii ventriculare: TVNS (definita ca 3 sau mai multe
batai ventriculare succesive ce dureaza sub 30 s la o
frecventa mai mare de 100 bpm), TV sustinuta, stop cardiac
prin TV sau FV. Mortalitatea cardiaca a pacientilor cu oricare
tahiaritmie ventriculara este inalta, rezultand atat din MSC cat
si din mortalitatea nonsubita. Aceste aritmii pot fi rezultatul
ischemiei miocardice sau al insuficientei cardiace, in asociere cu
anomalii electrice primare. Este necesara o abordare agresiva pentru
tratamentul insuficientei cardiace si trebuie incercata
corectarea ischemiei miocardice la pacientii cu tahiaritmii ventriculare.
In unele cazuri, tratamentul adecvat al insuficientei cardiace si
ischemiei va aboli aritmia (TV primara poliforma, FV si TVNS).
Chiar daca terapia antiaritmica specifica este necesara,
frecventa aritmiilor poate fi redusa si toleranta poate fi
imbunatatita cu terapia adecvata a insuficientei
cardiace si ischemiei.
8.1.1. Tahicardia
ventriculara nesustinuta
Majoritatea
TVNS la pacientii cu cardiopatie ischemica cronica sunt scurte
si nu produc simptome. Nu exista dovezi ca supresia TVNS
asimptomatice prelungeste viata. Astfel, nu exista nici o
indicatie pentru tratarea TVNS, exceptand rare cazuri cand episoade frecvente
(incesante) sau foarte rapide compromit stabilitatea hemodinamica. In
aceste cazuri TVNS pot fi tratate cu medicamente antiaritmice, ablatie pe
catater sau rezectie chirurgicala. Cand TVNS provoaca simptome
care necesita terapie, ar trebui determiniate caracterele
electrocardiografice ale TVNS, pentru a afla daca TVNS este data de
un IM vechi sau are un mecanism distinct care poate fi supus ablatiei prin
radiofrecventa, precum tahicardia cu punct de plecare in tractul de
ejectie ventricular. Terapia farmacologica initiala a TVNS
trebuie sa fie reprezentata de agenti betablocanti,
daca nu sunt deja folositi la o doza adecvata. Terapia medicamentoasa
cea mai adecvata la pacientii cu TVNS simptomatica
neresponsiva la betablocanti este amiodarona sau sotalolul.
8.1.2. Tahicardia
ventriculara sustinuta
Tratamentul
TV sustinute la pacientii cu cardiopatie ischemica cronica
trebuie adaptat la manifestarile clinice produse de tahicardie ca si
la frecventa episoadelor. Pacientii care se prezinta cu TV
sustinuta monomorfa care nu determina stop cardiac si
nu cauzeaza instabilitate hemodinamica severa sunt de obicei,
dar nu intotdeauna, cu risc scazut pentru moarte subita cardiaca
(2% pe an).399,400 Trebuie efectuat un ECG pe 12 derivatii in
timpul episodului de TV sustinuta si evaluata morfologia
pentru a fi siguri ca e in concordanta cu un IM precedent. Trebuie
avut in vedere ca pacientii cu un IM vechi pot dezvolta TV
sustinuta fara legatura cu infarctul, prin alte
mecanisme ca reintrarea prin ramura sau TV idiopatica. Daca
episoadele sunt relativ rare, ICD singur poate terapia initiala cea
mai potrivita, deoarece pacingul antitahicardic sau terapia cu soc
electric cu energie inalta pot reduce necesarul de spitalizare si
terapie antiaritmica medicamentoasa. Mijloace adjuvante pot fi
ablatia pe cateter, rezectia chirurgicala si terapia
medicamentoasa cu amiodarona sau sotalol.
Terapia
curativa a TV sustinute utilizand fie rezectia chirurgicala
fie ablatia pe cateter, trebuie avuta in vedere la pacientii cu
recurente frecvente de TV neresponsiva la terapia antiaritmica
medicamentoasa. Pacientii la care tahicardia este stabila
hemodinamic pot fi selectati pentru ablatia prin
radiofrecventa curativa. Limita majora a ablatiei este
faptul ca cei mai multi pacienti cu TV sustinute post-IM au
multiple tahicardii si e dificil de inlaturat toate focarele complet
utilizand tehnologia disponibila actual la ablatia prin radiofrecventa.
Unii pacienti au doar 1 sau 2 circuite de tahicardie si pot fi
vindecati de prin ablatie; oricum ei pot dezvolta din nou TV in
viitor, cu un circuit diferit. Desi nu toate tipurile morfologice de TV
pot fi vindecate prin ablatie pe cateter, substratul tahicardiei poate fi
modificat suficient pentru a scadea frecventa episoadelor aritmice.
Ablatia tahicardiei utilizand chirurgia pentru a rezeca sau a modifica
substratul aritmiei este o alternativa terapeutica ce poate fi
potrivita la pacientii la care ablatia pe cateter nu a dat
rezultate.
Dupa
corectia ischemiei, pacientii care se prezinta cu TV
sustinute cu compromitere
hemodinamica severa pot beneficia de studiul
electrofiziologic. Acesta poate releva ocazional aritmii curabile precum cele
prin reintrare in ramura. In plus rezultatul testului deseori ajuta
la programarea adecvata a defibrilatorului implantabil. Defibrilatorul
implantabil este terapia primara pentru acesti pacienti.
8.1.3. Tratamentul
fibrilatiei ventriculare si supravietuitorilor unui stop cardiac
Pacientii
care au suferit un stop cardiac prin fibrilatie ventriculara in
afara primelor 24-48 h post-IM pot avea risc pentru stop cardiac recurent. Ca
si pacientii cu TV sustinute, acesti pacienti trebuie
evaluati si tratati pentru ischemia miocardica. Daca
exista dovezi directe, clare pentru ischemie miocardica precedand
imediat debutul FV si nu exista dovada unui IM vechi, prima
atitudine terapeutica trebuie sa fie revascularizarea coronariana
completa. Daca revascularizarea coronariana nu poate fi
realizata si avem dovada unui IM anterior cu disfunctie
ventriculara stanga semnificativa, terapia de prima linie
pentru pacientii resuscitati dupa FV trebuie sa fie implantarea
unui defibrilator.
8.1.4. Preventia
primara a mortii subite cardiace
Toti
pacientii coronarieni au risc de MSC si cele mai multe MSC apar la
pacientii fara disfunctie ventriculara stanga
severa. Totusi, in absenta unor aritmii simptomatice, pacientii
fara IM in antecedente, si chiar cei cu IM vechi cu FE >40%,
au un risc atat de mic, incat profilaxia nu este indicata in prezent. In
plus, cand FE >40%, riscul de MSC este suficient de mic astfel incat terapia
profilactica nu este indicata la pacientii cu aritmii
asimptomatice, ca TVNS.
Subgrupuri
de pacienti raman cu risc de MSC cativa ani dupa IM. S-a
demonstrat ca multipli factori, in afara de scaderea
fractiei de ejectie, cresc riscul de MSC post-IM; acesti factori
includ prezenta TVNS, insuficienta cardiaca simptomatica
si TV sustinuta monomorfa inductibila la SEF.
Singurul
tratament antiaritmic dovedit a fi eficace pentru reducerea riscului de MSC
si a mortalitatii totale este ICD. ICD este indicat pentru
reducerea riscului de MSC la doua grupuri de pacienti: pacienti
cu FE ≤40% post-IM si care au TVNS spontana si TV
sustinuta monomorfa inductibila electrofiziologic,267
si pacienti cu FE <30%, ca rezultat al unui IM care a avut loc cu
mai mult de 40 de zile anterior, cand insuficienta cardiaca (clasa
functionala NYHA II sau III) este prezenta.248,268
Motivul indicarii ICD la pacienti cu IC simptomatica, pe
langa fractia de ejectie scazuta, este faptul ca
beneficiul ICD este maxim la acesti pacienti. Cei mai multi
pacienti inrolati in trialuri de preventie primara aveau
insuficienta cardiaca simptomatica.8 Evaluarea
in vederea stabilirii necesitatii implantarii defibrilatorului
si implantarea sa trebuie amanate cel putin 3 luni dupa
revascularizare (i.e., by-pass sau angioplastie percutanta), pentru a
acorda timpul necesar pentru recuperarea functiei ventriculare dupa
revascularizare. In general, implantarea ICD trebuie amanata pana la
cel putin 40 zile post-IM la pacientii care intrunesc criteriile de
mai sus, astfel incat sa permita recuperarea functiei
ventriculare si pentru ca nu s-a demonstrat imbunatatirea
supravituirii cand implantarea avut loc in primele 40 zile post-IM.152,248,401-403
Daca exista indoieli, un studiu electrofiziologic poate fi efectuat.
Terapia
cu amiodarona a fost considerata relativ sigura la
pacientii post-IM care au aritmii simptomatice, care au necesitat
supresie. Desi trialurile randomizate nu au demonstrat un beneficiu al
supravietuirii cand terapia empirica cu amiodarona a fost
initiata precoce post-IM, mortalitatea nu a fost crecuta si
decesele de cauza aritmica au avut un evident trend
descrescator sub tratamentul cu amiodarona.404,405
Oricum, la pacientii cu insuficienta cardiaca severa
(clasa functionala NYHA III) amiodarona se poate sa nu fie
utila.8,248 Astfel amiodarona nu trebuie utilizata de
rutina post-IM, dar este probabil terapia cea mai sigura de utilizat
pentru supresia aritmiilor simptomatice.
8.1.5. Utilizarea
defibrilatorului implantabil pentru tahicardia ventriculara la
pacientii cu fractie de ejectie a ventriculului stang
normala sau aproape normala
TV
sustinuta recurenta este de obicei tratata prin corectarea
conditiilor favorizante, preventia factorilor predispozanti
si declansatori si prin utilizarea terapiei antiaritmice
clasa I sau III. Utilizarea agentilor antiaritmici poate predispune
pacientul la complicatii proaritmice, care pot ameninta semnificativ
viata. Tot mai frecvent, ICD este folosit eficient pentru tratarea
acestor aritmii, care per se pot sa nu fie amenintatoare
de viata, pentru a evita ineficacitatea relativa si
reactiile adverse ale terapiei medicamentoase. In cazul TV monomorfe,
pacing-ul antitahicardic este deseori aplicat cu succes, fara sa
provoace simptome nedorite. Pe de alta parte, TV polimorfa sau FV,
legate sau nu de terapia antiaritmica medicamentoasa, pot necesita
terapie prin soc electric. In orice caz, strategia de utilizare a defibrilatorului
pentru terapia acestor aritmii pare sa fie de succes, desi
scumpa.
8.2. Valvulopatiile
Recomandari
Clasa I
Pacientii
cu valvulopatii si aritmii ventriculare trebuie evaluati si
tratati urmarind recomandarile curente pentru fiecare
boala. (Nivel de dovezi: C)
Clasa IIb
Nu
a fost stabilita cu precizie eficienta repararii valvei
mitrale sau protezarii acesteia pentru a reduce riscul de MSC la
pacientii cu prolaps de valva mitrala, regurgitare mitrala
severa si aritmii ventriculare severe. (nivel de dovezi : C)
Aritmiile
ventriculare care apar la pacientii valvulari pot fi cauzate prin orice
mecanism de producere responsabil pentru aritmiile ventriculare din alte boli
cardiace. Acesti pacienti pot asocia cardiopatie ischemica, disfunctie
miocardica, HVS severa, tulburari de ritm dependente de tonusul
adrenergic sau anomalii moleculare mostenite. Afectiunile valvulare
nu pot produce in mod direct aritmii ventriculare, dar pot contribui la aparitia
acestora prin efectul lor asupra miocardului. Desi MSC la bolnavii cu
leziuni valvulare semnificative este produsa frecvent prin aritmii
ventriculare grave, nu este clar daca evenimentul este declansat de
aritmiile ventriculare preexistente. In linii mari, se cunoaste mai bine
riscul de MSC la pacientii cu afectare valvulara aortica
comparativ cu alte valvulopatii. Desi riscul global este redus, MSC
aritmica pare a fi mai frecventa in stenoza aortica decat in
alte leziuni valvulare: aproximativ 0,4% pe an pentru stenoza aortica, mai
putin de 0,2% pe an pentru regurgitare si mai putin de 0,2 % pe
an pentru valvulopatiile mitrale.406,407
Majoritatea
bolnavilor care mor subit erau simptomatici datorita bolii valvulare.406
Desi TVNS recurente pot situa la risc pentru sincopa un pacient cu
stenoza aortica severa, managementul acestuia este ghidat de
regula in functie de severitatea leziunii valvulare. In prezent,
exista insuficiente date care sa demonstreze o reducere a aritmiilor
ventriculare ca rezultat al repararii sau protezarii valvulare la
majoritatea pacientilor valvulari. Din aceste motive, acesti bolnavi
valvulari si cu aritmii ventriculare ar trebui evaluati si tratati
urmand recomandarile actuale pentru fiecare boala.406
Prezenta unei aritrnii ventriculare per se nu constituie o indicatie
pentru repararea sau inlocuirea valvulara. O exceptie de la aceste
recomandari generale a fost indicata la pacientii cu prolaps de
valva mitrala de etiologie mixomatoasa si cu aritmii
ventriculare grave, la care poate exista un risc crescut pentru MSC, mai ales
la subgrupul care prezinta si un flail al foitelor mitrale.408,409
Din acest motiv, aparitia frecventa a aritmiilor ventriculare la
bolnavii eu regurgitare mitrala mixomatoasa severa a fost
incadrata ca o recomandare de clasa IIb pentru chirurgie,406
desi nu a fost stabilita eficienta sa in reducerea MSC. Rolul
prelungirii intervalului QT la subgrupul pacientilor cu prolaps de
valva mitrala ramane neclar.3,410
Pacientii
cu leziuni valvulare moderate care nu au VS marit, HVS sau disfunctie
trebuie tratati ca si cei fara boala structurala.
8.3. Boli cardiace
congenitale
Recomandari
Clasa I
Implantarea
de ICD este indicata la pacientii cu boli cardiace congenitale
supravietuitori ai unui stop cardiac, dupa evaluare pentru precizarea
cauzei care a provocat evenimentul si eliminarea cauzelor reversibile.
Implantarea ICD este recomandata la bolnavii care primesc terapie medicamentoasa
cronica optima si care au o speranta de
viata rezonabila cu un status
functional bun pentru cel putin 1 an (Nivel de dovezi : B)
Pacientii
cu boli cardiace congenitale si TV sustinute spontane ar trebui sa
fie supusi unei evaluari invazive hemodinamice si unui studiu
electrofiziologic. Terapiile recomandate includ cateter-ablatia sau
rezectia chirurgicala pentru eliminarea TV. Daca acestea nu au
succes, se recomanda implantarea unui defibrilator. (Nivel de dovezi : C)
Clasa IIa
Evaluarea
invaziva hemodinamica si studiul electrofiziologic se pot
efectua la pacientii cu boli cardiace congenitale si sincope inexplicabile
precum si functie ventriculara alterata. In absenta
unei cauze clare reversibile, este rezonabila implantarea unui ICD la
pacientii care primesc terapie medicamentoasa cronica
optima si care au o speranta de viata
rezonabila cu un status functional bun pentru cel putin 1 an. (Nivel de dovezi : B)
Clasa IIb
Studiul
electrofiziologic poate fi luat in considerare la bolnavii cu boli cardiace
congenitale si TVNS sau cuplete ventriculare pentru a evalua riscul unei
aritmii ventriculare sustinute. (Nivel de dovezi : C)
Clasa III
Terapia
antiaritmica profilactica nu este indicata pacientilor
asimptomatici cu boli cardiace congenitale si BPV izolate. (Nivel de dovezi : C)
Bolile
cardiace congenitale alcatuiesc un spectru divers de defecte anatomice
si fiziologice cu diferente semnificative in ceea ce priveste
evolutia naturala, fiziologia pre si postoperatorie precum
si riscul aritmiilor si al MSC. Per ansamblu, defectele cardiace
congenitale sunt o cauza majora de mortalitate infantila (varsta
sub 1 an) in societatile industrializate. Oricum, o data cu
progresele in cardiologie, aceasta rata a mortalitatii a
fost redusa de la 105 la 59 de morti la 100.000 de nasteri
intre anii 1980 si 1995.411 Aproape toate defectele pot fi acum
reparate sau ameliorate, cu un numar estimat de peste 1 milion de
supravietuitori la nivel global ai interventilor chirurgicale pentru
cardiopatiile congenitale.412 Desi supravietuirea pe
termen scurt sau lung a acestor pacienti reprezinta inca un
subiect de studiat, se pare ca bolnavii cu anumite defecte prezinta
un risc crescut de mortalitate tardiva subita si globala.413'
Datorita incidentei scazute a MSC tardive postoperatorii la
pacientii cu boli cardiace congenitale, nu au fost realizate studii
clinice pentru a evidentia factorii de risc pentru MSC sau rolul
terapiilor de preventie primara. De aceea, nivelul dovezilor pentru
majoritatea recomandarilor este de clasa C.
In
timpul perioadei de sugar si a copilariei, mai mult de 75% dintre
decesele la pacientii cu boli cardiace congenitale sunt evenimente
intraspitalicesti, majoritatea petrecandu-se in perioada perioperatorie.414
Restul deceselor se produc in afara spitalelor sau in departamente de
urgenta, adesea la pacientii cu alte anomalii congenitale sau
cu sepsis. De aceea, numarul bolnavilor foarte tineri cu boli cardiace
congenitale care sunt victime ale MSC aritmice este destul de mic.
Peste
varsta de 20 de ani, exista o crestere progresiva a
incidentei mortalitatii subite precum si a mortalitatii
totale cardiace postoperatorii la pacientii cu boli cardiace congenitale.413
Astfel, majoritatea studiilor de moarte subita la bolnavii cu patologie
congenitala cardiaca au evaluat adolescenti si adulti
tineri.425 5 boli cardiace congenitale au fost asociate cu cel mai
mare risc de MSC tardiva: tetralogia Fallot, D- si L-
transpozitia de vase mari, stenoza aortica si ventriculul unic
functional.413,416,417
Cel mai
mare numar de studii privind MSC tardiva postoperator la
pacienti cu boli congenitale au fost cele pentru tetralogia Fallot. O
metaanaliza a 39 de studii ingloband un numar de 4627 de
pacienti a aratat ca asocierea intre disfunctia
ventriculara si ectopia ventriculara complexa a fost
corelata primar cu MSC tardiva.418 Desi au fost
propusi peste 20 de factori de risc pentru MSC 419
supraincarcarea volemica datorata insuficientei pulmonare
si o durata a complexului QRS mai mare de 160 ms par a fi factorii
aditionali cel mai probabil asociati cu un un risc crescut de MSC
datorata aritmiilor ventriculare.420,421 Rezultatele studiului
electrofiziologic pentru stratificarea riscului la acesti bolnavi nu au
fost multumitoare datorita fie protocoalelor diferite de studiu, fie
definirii raspunsului la asemenea teste.422-424
Postoperator,
pacientii cu D- transpozitie de vase mari par a avea riscuri diferite
pentru MSC tardiva, in functie de interventie - switch atrial
(Mustard sau Senning) sau switch arterial. O incidenta foarte
crescuta a aritmiilor atriale tardive a fost observata la
pacientii care au suferit interventii atriale de switch, complicate
cu bradicardii sinusale marcate.425,426 Mecanismul MSC pare a fi
flutterul atrial cu conducere AV 1:1, urmat de ischemie miocardica
si cu degenerare ulterioara in TV polimorfa sau fibrilatie
ventriculara.427 Atat in D- cat si in L- transpozitia
de vase mari, disfunctia ventriculara progresiva poate da
nastere unor aritmii ventriculare care pot fi cauza MSC.416,428
In
principiu, pacientii operati cu sincopa inexplicabila ar
trebui evaluati atat hemodinamic cat si prin studiu
electrofiziologic. A fost raportata o incidenta crescuta a
TV sustinute inductibile la pacientii operati cu sincopa,
care aveau ectopie ventriculara complexa.429,430 Mai
mult, un rezultat pozitiv la studiul electrofiziologic, independent de
indicatia clinica, poate identifica pacientii cu un risc
crescut de MSC tardiva.423 Dimpotriva, ectopia
ventriculara izolata este frecventa postoperator la vechii
pacienti cu boli cardiace congenitale. In absenta disfunctiei
ventriculare sau simptomelor, ectopia ventriculara izolata are o
semnificatie prognostica minima, iar riscul tratamentului antiaritmic
poate depasi potentialul bencficiu.431 Astfel
raman multi pacienti cu ectopie ventriculara simpla
sau complexa, cu simptomatologie vaga sau cu afectare minima a
functiei ventriculare, care necesita o judecata individuala
in ceea ce priveste nevoia de evaluare si tratament.432 Exista
si cauze nonaritmice de MSC tardiva la pacientii operati
incluzand: embolie pulmonara sau cerebrala, endocardita sau
ruptura anevrismala.413,416
O
alta categorie de boli congenitale care pot genera MSC o reprezinta
anomaliile coronarelor. Cea mai frecventa anomalie coronariana
congenitala care provoaca MSC este originea anormala a arterei
coronare stangi din sinusul Valsalva drept. Mecanismul propus de MSC este fie
angularea acuta a ostiumului coronar, fie compresiunea coronarei stangi
in portiunea care traverseaza regiunea cuprinsa intre peretele
aortic si tractul de ejectie al VD, rezultand ischemie
miocardica acuta cu dezvoltarea ulterioara de TV sau
fibrilatie ventriculara. Riscul de MSC pare a fi cel mai mare in timpul
primelor 3 decade de viata. Diagnosticul poate fi dificil deoarece
doar o treime dintre bolnavi au in antecedente sincopa de efort sau
angina. Diagnosticul decisiv prin angiografie coronariana
reprezinta o indicatie pentru revascularizare chirurgicala.
Riscuri asemanatoare de MSC au fost raportate si pentru originea
anormala a arterei coronare drepte din sinusul stang Valsalva.433
Originea
anormala a arterei coronare stangi din artera pulmonara se
descopera, in general, in prima luna de viata. O data
cu declinul normal al rezistentei vasculare pulmonare, se dezvolta
ischemia si disfunctia miocardica pe masura ce perfuzia
coronariana este suntata spre circulatia pulmonara.
Atunci cand diagnosticul este stabilit ecocardiografic in timpul perioadei de
sugar, reimplantarea chirurgicala a ostiumului coronarei stangi este
asociata, in general, cu recuperarea functiei ventriculare. Oricum,
un mic procent dintre acesti pacienti pot supravietui unui IM
precoce si sa dezvolte ulterior circulatie colaterala extensiva
intre coronara dreapta si cea stanga. Acesti pacienti
pot prezenta mai tarziu peste mai multi ani sau decade angina,
insuficienta cardiaca sau aritmii ventriculare.434
8.4. Afectiuni
inflamatorii sau metabolice
Desi
bolile din aceasta categorie reprezinta cauze importante de aritmii
ventriculare amenintatoare de viata, incidenta TV/MSC
este relativ rara si, de aceea, in majoritatea cazurilor,
exista putine date din studii clinice despre cum trebuie abordate
aceste aritmii. Datele referitoare la preventia aritmiilor ventriculare
amenintatoare de viata sunt chiar si mai rare. Din
acest motiv, toate recomandarile din aceasta sectiune au un
nivel de dovezi B sau C.
Urgentele,
consecinta a oricarei boli subiacente din aceasta
sectiune, ar trebui abordate conventional.
8.4.1. Miocardita,
reumatismul
articular si endocardita
Recomandari
Clasa I
Implantarea de
stimulator temporar este indicata la pacientii cu bradicardie
simptomatica si/sau bloc in timpul fazei acute a unei miocardite. (Nivel de dovezi : C)
Regurgitarea
aortica acuta asociata cu TV ar trebui tratata chirurgical
daca nu exista contraindicatii. (Nivel de dovezi : C)
Endocardita
acuta complicata cu abces aortic sau de inel si bloc AV ar
trebui tratata chirurgical daca nu exista contraindicatii.
(Nivel de dovezi: C)
Clasa IIa
Implantarea
ICD poate aduce aduce beneficii pacientilor cu aritmii
amenintatoare de viata, care nu se gasesc in faza
acuta a miocarditei, dupa cum este indicat in Update-ul ghidului
ACC/NASPE 2002 de implantare a stimulatoarelor cardiace si dispozitivelor
antiaritmice,1 care primesc terapie cronica medicamentoasa
optima si care au o speranta de viata rezonabila
cu un status functional bun pentru cel putin 1 an. (Nivel de dovezi : C)
Terapia
antiaritmica poate fi utila la pacientii cu TVNS sau TV
sustinute simptomatice in timpul fazei acute a miocarditei. (Nivel de dovezi: C)
Clasa III
Implantarea
ICD nu este indicata in timpul fazei acute a miocarditei. (Nivel de dovezi : C)
8.4.1.1. Miocardita
Miocardita
este un proces inflamator care afecteaza miocardul fiind, cel mai adesea,
asociata cu infectia. Oricum, alte expuneri la toxice, cum ar fi
radiatiile, substantele chimice sau alti agenti fizici pot
conduce la inflamatie cardiaca. Cei mai frecventi agenti
infectiosi care provoaca miocardita sunt virusurile.435,436
Alti agenti infectiosi implicati in etiologia
miocarditelor includ bacterii, fungi, protozoare, metazoare, spirochete si
rickettsii.435,437-453 Imunosupresia nu pare a influenta semnificativ
prognosticul, nefiind recomandata in acest moment.453
Evolutia
miocarditei acute variaza ca si modul de prezentare.454
Prezentarea variaza de la o descoperire asimptomatica datorata
modificarilor tranzitorii ST-T pe ECG pana la o afectiune fulminanta
amenintatoare de viata cu simptome care mimeaza
ischemia. Abordarea de urgenta este in mare masura de
sustinere, putand fi destul de agresiva in functie de modul de
prezentare.455 Aritmiile cardiace asociate cu miocardita acuta
pot varia de la tulburari de conducere pana la aritmii ventriculare
amenintatoare de viata. Mortalitatea este datorata
insuficientei cardiace si aritmiilor, inclusiv blocurilor cardiace.
444,445,455-460 Pacieniti cu aritmii sau sincopa pot necesita
medicamente antiaritmice si/sau terapie invaziva.461
Implantarea unui stimulator cardiac temporar este indicata bolnavilor cu
miocardita acuta care prezinta bloc simptomatic, ca si in
cazul altor situatii cu bloc simptomatic. Pacing-ul este indicat
pacientilor cu disfunctie simptomatica de nod sinusal sau cu
bloc AV, ca si in cazul altor situatii de disfunctie a nodului
sinusal sau nodului AV.
Miocardita
acuta poate evolua spre cardiomiopatie cronica prin mai multe
mecanisme.455 La bolnavii cu cardiomiopatie reziduala
severa si aritmii ventriculare, defibrilatoarele si/sau
dispozitivele biventriculare sunt implantate pentru aceleasi
indicatii precum cele recomandate in sectiunile de
insuficienta cardiaca si cardiomiopatii.
Miocardita
idiopatica cu celule gigante este destul de rara, dar are ca
particularitate faptul ca afecteaza indivizii tineri si este de
regula fatala, daca nu este tratata.462-467 Diagnosticul
este confirmat prin biopsie endomiocardica. Pacientii pot dezvolta
blocuri, necesitand pacemakere temporare sau permanente. Un defibrilator sau
antiaritmice de genul amiodaronei pot fi necesare in cazul TV.462
Cardita
Lyme este o complicatie a bolii Lyme afectand intre 0,3% si 8%
dintre cei infectati cu Borrelia burgdorferi.468-471 Bolnavii
pot dezvolta tulburari diverse de conducere. Pot apare ritmul
jonctional sau perioade de asistola. Disfunctia de VS este in
general moderata, iar procesul este de regula autolimitat atunci cand
este tratat cu antibiotice.468 TV, in general nesustinuta,
a fost raportata rareori.473-475
Implicarea
cardiaca a fost mentionata adeseori la pacientii cu
sindromul imunodeficientei dobandite (SIDA) si a fost intalnita,
de asemenea, la cei cu infectie cu HIV fara SIDA.476-479 MSC
a fost raportata in implicarea miocardica primara a HIV.480,481
Prelungirea QT si aritmiile au fost atribuite terapiei medicamentoase.482-484
Boala
Chagas este provocata de protozoarul Trypanosoma cruzi; este
transmisa printr-un insecta vector si este comuna in
America Centrala si de Sud. Miocardita acuta este rara, dar
peste o treime dintre pacienti dezvolta deteriorare miocardica
tardiva cu insuficienta cardiaca progresiva si au
o supravietuire redusa. Tulburarile de conducere cu progresie
spre bloc complet sunt frecvente. Amiodarona pare a fi eficienta in
tratamentul tahiaritmiilor ventriculare, iar moartea se produce ca rezultat al
insuficientei cardiace refractare sau datorita aritmiilor.485
Terapia cu dispozitive intracardiace, inclusiv ICD este utilizata adesea
in faza tardiva.486 La cei cu un status functional bun
(ex, clasa functionala NYHA I sau II), MSC este un eveniment rar,
atunci cand pacientii sunt tratati cu amiodarona. Oricum, rata
recurentelor TV este crescuta, la 30% pe an. Ablatia prin RF de
la suprafata epicardica a fost raportata ca fiind o metoda
folositoare. La cei cu insuficienta cardiaca avansata, terapia
medicamentoasa aduce un beneficiu minor, iar rata recurentei
aritmiilor se apropie de 100%. Mortalitatea este crescuta la acesti
pacienti, cu o medie de 40% la 1 an.487
8.4.1.2. Boala
reumatismala
Reumatismul
articular acut produce pancardita implicand pericardul, miocardul si
endocardul. Tahicardia sinusala si prelungirea PR sunt comune. Pot
apare blocuri de ramura, modificari nespecifice ST-T precum si
batai ventriculare sau atriale premature. Blocul complet si
aritmiile ventriculare sunt rare.488-490 A fost asociat cu
intervalul QT prelungit si cu torsada varfurilor.489
8.4.1.3. Endocardita
Endocardita
infectioasa poate apare ca endocardita bacteriana
subacuta sau acuta. Endocardita bacteriana subacuta este
legata cel mai adesea de infectiile cu specii de streptococi si
mai rar cu Staphylococcus aureus, S. Epidermidis sau cu dificilul Haemophylus
sp. In mod caracteristic, se dezvolta pe valve anormale dupa
bacteriemii asimptomatice de la nivelul gingiilor infectate sau din tractul
genitourinar sau gastrointestinal. Endocardita acuta este legata
cel mai adesea de infectiile cu S. aureus, streptococi hemolitici
de grup A, pneumococi sau gonococi si cu microorganisme cu virulenta
mai scazuta. Se poate dezvolta pe valve normale.491
Endocardita netratata este aproape intotdeauna fatala. Endocardita
pe valve protezate reprezinta un procent important din toate cazurile de
endocardita infectioasa. Desi incidenta globala
a endocarditei infectioase nu s-a modificat de-a lungul ultimelor 3
decade, a crescut varsta debutului. Atunci cand apare endocardita cordului
drept, cel mai adesea este legata de abuzul de substante
intravenoase.
Endocardita
valvelor aortice si mitrale a fost asociata cu decesul rapid
datorita rupturilor valvulare, emboliilor in arterele coronare sau
abceselor din inelele valvulare sau din sept.492,493 Desi
aceste morti sunt de regula rapide, ele nu sunt de obicei
clasificate drept morti subite. Mai rar, endocardita a fost asociata
cu MSC datorata tamponadei secundara rupturii.494,495
Aparitia tulburarilor de ritm are un prognostic prost in endocardita
infectioasa.496 Formarea abceselor in inelul valvular
poate determina blocuri de gradul I sau II. Acest lucru se produce mai frecvent
in endocardita valvei aortice decat in cea a valvei mitrale.497
Blocul cardiac avansat poate apare daca abcesul erodeaza septul
si intrerupe sistemul de conducere. Blocul cardiac cu debut recent la un
patient cu endocardita are specificitate foarte mare pentru abces.498
Pacientii cu abcese perivalvulare au un risc foarte mare de a face alte
complicatii, cum ar fi emboliile sau moartea.499
Terapia
antimicrobiana va fi initiata in functie de agentul cauzal
specific.500 Interventia chirurgicala este recomandata
acelora cu embolii recurente sau cu insuficienta cardiaca
refractara sau celor care nu raspund la terapia antimicrobiana.
Majoritatea medicilor sunt convinsi ca formarea abceselor sau
endocardita fungica sunt indicatii chirurgicale.501,502
Deteriorarea hemodinamica acuta datorata regurgitarii
aortice acute secundare endocarditei poate determina TV si este o
indicatie pentru interventia chirurgicala precoce.498,499,503
Terapia medicamentoasa a aritmiilor nu difera de la
principiile clinice acceptate in general. Interventia chirurgicala
poate fi recomandata in cazul implicarii miocardice documentate sau
formarii abceselor.504
8.4.2. Cardiomiopatiile infiltrative
Recomandari
Clasa I
In
plus fata de abordarea cardiomiopatiilor infiltrative subiacente,
aritmiile amenintatoare de viata ar trebui tratate in
aceeasi maniera cu aritmiile care apar in alte cardiomiopatii,
inclusiv cu folosirea defibrilatoarelor sau stimulatoarelor la pacientii
care primesc terapie cronica medicamentoasa optima si
care au speranta de viata rezonabila, cu un status
functional bun timp de peste 1 an. (Nivel de dovezi: C)
Asocierea
dintre cardiomiopatiile infiltrative si TV/ MSC este bine
documentata. In toate cazurile, atunci cand se impune, tratamentul
afectiunii de baza trebuie sa insoteasca abordarea
manifestarilor cardiace.
8.4.2.1. Sarcoidoza
Un sfert
dintre pacientii cu sarcoidoza prezinta leziuni cardiace, dar
exista o corelare slaba intre simptomatologie si implicarea
miocardica, chiar si in cele mai avansate cazuri, iar MSC poate fi
astfel prima manifestare a bolii.505 In cazurile dovedite de
sarcoidoza cardiaca, aritmiile supraventriculare si ventriculare
apar frecvent (73%), iar blocul de ramura este prezent la aproximativ
doua treimi dintre pacienti.
Aproximativ
un sfert dintre acesti bolnavi dezvolta bloc complet; un procent
asemanator au insuficienta cardiaca congestiva.
Monitorizarea Holter sau ECG nu sunt destul de sensibile sau specifice pentru
aprecierea implicarii miocardice, dar pot fi utile in identificarea
tulburarilor de ritm, o data ce diagnosticul a fost confirmat prin
alte metode (ex, SPECT cu Thallium-201 si Gallium 67 sau RMN). Biopsia
miocardica, desi insensibila, are o specificitate
crescuta pentru diagnosticul de sarcoidoza miocardica. Terapia
corticoida poate reduce numarul batailor premature
ventriculare si al episoadelor de tahicardie, facand astfel aritmia
mai usor de tratat;506 poate fi astfel redus si pericolul
de MSC, iar in tulburarile de conducere poate fi observata o
imbunatatire. Folosirea imunosupresoarelor nu poate elimina riscul
aparitiei ulterioare a aritmiilor. Rezolutia granuloamelor poate
constitui un substrat pentru aritmogeneza. Nu exista date din studii
clinice prospective, dar TV spontane, disfunctia severa de VS si
tulburarile de conducere intraventriculare severe justifica
implantarea de ICD sau stimulatoare.507
8.4.2.2. Amiloidoza
Afectarea
cardiaca din amiloidoza, indiferent de tipul interventiei
chimioterapice, poarta un prognostic foarte slab. In subtipul AL, media
supravietuirii este de 6 luni, cu o rata a supravietuirii de 6%
la 3 ani.508,509 Insuficienta cardiaca progresiva
reprezinta, de regula, modalitatea de deces, dar bradiaritmiile
si, mai ales, TV pot fi evenimentul final. Aritmiile ventriculare complexe
sunt frecvente, afectand 57% dintre pacienti; 29% au cuplete, iar 18% au
TVNS.510 Troponinele cardiace, mai ales troponina T;511
grosimea peretelui VS, in special cea mai mare de 12-15 mm la ecocardiografia
bidimensionala;512 prezenta potentialelor tardive pe
SAECG;513 si timpul prelungit de conducere infrahisian (HV) la
studiul electrofiziologic514 pot fi predictori independenti ai
mortalitatii. Troponinele cardiace crescute pot influenta
decizia finala, deoarece supravietuirea medie la pacientii cu
valori detectabile este intre 6 si 8 luni, comparativ cu cei
fara valori detectabile a caror supravietuire medie este
intre 21 si 22 de luni.511 QTc este prelungit la pacientii
cu amiloidoza cardiaca, dar acest lucru nu pare a se corela cu
aritmiile amenintatoare de viata.515 Utilizarea
ICD sau a stimulatoarelor cardiace permanente poate sa nu influenteze
prognosticul pe termen lung, dar in cazurile familiale pot fi folosite drept
punte terapeutica pana la transplant.516
8.4.2.3.
Boala Fabry
Boala
Fabry este o afectiune recesiva X-linkata a depozitelor
lizozomale, produsa prin deficitul de alfa galactozidaza
lizozomala. Cardiomiopatia Fabry are o prevalenta intre 3
si 6% la barbatii cu HVS inexplicabila.517,518
Femeile care au o activitate scazuta a alfa-1 galactozidazei pot
prezenta, de asemenea, manifestari cardiace.519 Desi
afectarea cardiaca provoaca o serie de anomalii ECG si
tulburari de conducere, blocurile cardiace, aritmiile ventriculare
si MSC par sa fie foarte rare.520-525 Ameliorarea
hipertrofiei cardiace si a tulburarilor de conducere a fost
obtinuta cu terapie de substitutie enzimatica.526
8.4.2.4. Hemocromatoza
Pana
la o treime din homozigotii cu hemocromatoza au afectare
cardiaca. Desi evolutia naturala a bolii cardiace
netratate este spre insuficienta cardiaca progresiva, au
lost raportate si aritmii ventriculare;527,528 incidenta
lor, ca si a MSC, este insa necunoscuta. Diagnosticul precoce
si abordarea corespunzatoare a hemocromatozei sunt esentiale
pentru un prognostic favorabil, deoarece afectarea cardiaca si
hepatica pot fi reversibile in stadiile precoce ale bolii.529
Aritmiile trebuie abordate conventional.
8.4.3. Bolile endocrine
si diabetul
Recomandari
Clasa I
Abordarea
aritmiilor ventriculare secundare bolilor endocrine ar trebui sa se
adreseze dezechilibrului electrolitic (potasiu, magneziu si calciu)
si terapiei endocrinopatiei subiacente. (Nivelde dovezi: C)
Aritmiile
amenintatoare de viata persistente care apar la
pacientii cu afectiuni endocrine ar trebui tratati in
aceeasi maniera cu aritmiile care apar la bolnavii cu alte boli,
inclusiv folosirea ICD si a stimulatoarelor la cei care primesc terapie
cronica medicamentoasa optima si care au o
speranta de supravietuire rezonabila cu un status
functional bun timp de peste 1 an. (Nivel de dovezi: C)
Pacientii
cu diabet si cu aritmii ventriculare ar trebui tratati, in principiu,
in aceeasi maniera ca si cei fara diabet. (Nivel de dovezi: C)
8.4.3.1. Introducere
Bolile
endocrine pot induce TV/MSC prin activitate hormonala in exces sau
insuficienta pe receptorii miocardici (ex, feocromocitom,
hipotiroidism). Endocrinopatiile pot produce modificari ale miocardului
(ex, acromegalie), precum si tulburari electrolitice datorate excesului
hormonal (ex, hiperkalemia din boala Addison, hipokalemia din sindromul Conn),
iar anumite tulburari endocrine pot accelera progresia unor afectiuni
cardiace structurale secundare dislipidemiei sau hipertensiunii, crescand
astfel riscul de aparitie al aritmiilor severe.
8.4.3.2.
Afectiunile tiroidiene
Tireotoxicoza
produce in mod frecvent aritmii atriale, cazurile de TV/MSC sunt extrem de rare
dar pot surveni cand exista si tulburari electrolitice concomitente.530
TV/MSC sunt mai frecvente in hipotiroidism, mecanismul ce sta la baza lor
avand probabil legatura cu prelungirea intervalului QT.531,532
Terapia de substitutie cu tiroxina corecteaza de obicei aceste
tulburari si previne aparitia altor aritmii, dar in
situatii de urgenta au fost folosite cu succes si
medicamente antiaritmice ca procainamida.531
8.4.3.3. Feocromocitomul
Feocromocitomul
poate produce TV/MSC, dar nu exista date care sa cuantifice
incidenta acestora, cea mai buna metoda de management, respectiv
raspunsul la tratament. Incidenta este probabil mica, si
posibil exacerbata de cardiomiopatia hipertrofica/dilatativa
reversibila indusa de catecolamine.533 Terapia
conventionala de antagonizare a excesului de catecolamine cu alfablocante,
urmata de administrarea de betablocante, nu numai ca ajuta la
controlul hipertensiunii si previn deteriorarea structurala
ulterioara,534 dar exista dovezi anecdotice ca
previne recurenta aritmiilor ventriculare.535 Tratamentul
chirurgical definitiv si precoce al feocromocitomului ar trebui sa
fie prioritar, mai ales in cazurile cu aritmii amenintatoare de
viata documentate. La cativa pacienti cu TV asociata
feocromocitomului s-a identificat un interval QT prelungit.536,537
8.4.3.4. Acromegalia
MSC este
o manifestare cunoscuta a acromegaliei, aritmiile amenintatoare
de viata fiind probabil o cauza importanta a acesteia.538
Pana la jumatate din acromegali prezinta aritmie
ventriculara complexa pe monitorizarea Holter pe 24 de ore, iar din
acestia la aproximativ doua treimi aceasta este repetitiva.539
Exista o corelatie stransa intre aceste aritmii ventriculare
si masa ventriculului stang si durata bolii, dar nu si cu
nivelurile hormonale.539 Tratamentul chirurgical adecvat al
tumorii pituitare este un decisiva pentru prognosticul bun pe termen
lung, mai ales la tineri, modificarile cardiace fiind reversibile540,541
Analogii de somatostatina, cum ar fi octreotidul si lanreotidul
reduc amandoi HVS si imbunatatesc profilul aritmic
ventricular.542-544
8.4.3.5. Aldosteronismul
primar, boala Addison, hiper- si hipoparatiroidismul
Tulburarile
electrolitice severe stau la baza aritmogenezei si TV/MSC asociate cu
endocrinopatiile mai sus mentionate. O serie de modificari ECG cum ar
fi alungirea intervalurilor QRS si QT pot acompania anomaliile
electrolitice. Dezechilibrele electrolitice necesita o corectare
imediata, inaintea tratamentului definitiv ce vizeaza cauza
subiacenta.545-549
8.4.3.6. Diabetul
Diabetul
zaharat este un factor de rise major pentru ateroscleroza precoce si
accelerata, ducand la cresterea incidentei infarctului de
miocard, accidentului vascular cerebral, decesului in comparatie cu o
populatie de varsta similara si de acelasi sex,
fara diabet.95 Managementul complicatiilor
aterosclerotice care predispun la aritmii ventriculare si MSC la
pacientii cu diabet este similar cu cel al pacientilor fara
diabet.550
In plus
fata de ateroscleroza si hiperglicemie, care predispun
pacientii cu diabet la aritmii ventriculare si MSC, neuropatia
autonoma, episoadele tranzitorii de hipoglicemie ce pot surveni in urma
terapiei medicamentoase, afectarea organelor tinta cum ar fi insuficienta
renala, in care apar hiperpotasemia si ocazional episoade de
hipopotasemie iatrogena, cresc riscul de MSC.551-557
Cardiomiopatia restrictiva poate fi o complicatie tardiva la
pacientii cu diabet.
Episoadele
de hipoglicemie cresc tonusul simpatic. Probabilitatea de aparitie a
aritmiilor ventriculare este crescuta mai ales in situalia
particulara a pacientilor cu neuropatie autonoma. Hipoglicemia
severa se asociaza cu anomalii ale repolarizarii ventriculare,
alungirea intervalului QT si aritmii ventriculare.551,552 S-a
aratat ca betablocantele reduc amploarea acestor anomalii in timpul
hipoglicemiei indusa experimental.558 Desi mascheaza
simptomatologia hipoglicemiei, betablocantele imbunatatesc
semnificativ rata de supravietuire la pacientii cu diabet, iar
indicatiile lor de utilizare sunt similare ca si in cazul
pacientilor fara diabet.559 La un subgrup de
pacienti cu diabet si HVS inrolati in trialul Losartan
Intervention for Endpoint Reduction in Hypertension, losartanul se pare
ca ofera o protectie mai buna impotriva MSC decat
atenololul.560 IECA sau blocantele de angiotensina-2 sunt
recomandati tuturor pacientilor ce prezinta complicatii
vasculare datorate diabetului, daca au contraindicatii.
8.4.4. Stadiul final al
insuficientei renale
Recomandari
Clasa I
Managementul
aritmiilor ventriculare din stadiul final al insuficientei renale ar
trebui sa se adreseze imediat corectarii statusului hemodinamic
si dezechilibrelor electrolitice (de potasiu, magneziu, calciu). (Nivel de dovezi: C)
Aritmiile
amenintatoare de viata ar trebui sa fie tratate conventional
mai ales la pacientii ce asteapta un transplant renal,
incluzand ICD si pacemaker-ul la pacientai ce primesc
medicatie cronica optima, care au o speranta de
viata rezonabila cu un status functional bun timp de cel
putin un an. (Nivel de dovezi: C)
Afectiunile
cardiovasculare sunt responsabile de cel putin 40% din decesele
pacientilor cu insuficienta renala in stadiul final,
si 20% dintre decese sunt subite. Aritmiile apar frecvent pe parcursul
hemodializei si chiar la 4-5 ore dupa aceasta. Pe parcursul acestei
perioade statusul hemodinamic si fluctuatiile electrolitice in
special ale potasiului, magneziului si calciului joaca un rol crucial
in declansarea acestor evenimente nefavorabile si ar trebui
monitorizate cu atentie. Sindromul de QT lung a fost evidentiat
ocazional, uneori fiind corelat cu terapia cu sotalol.561 Factorii
de risc ce predispun la aritmii ventriculare includ: HVS, hipertensiunea, anemia,
disfunctia cardiaca si cardiopatia ischemica subiacenta.562
Dintre acestea, s-a sugerat ca tensiunea arteriala sistolica
si disfunctia miocardica ar fi cele mai importante cauze ale
aritmiilor complexe.563 Din pacate exista putine date
in ceea ce priveste identificarea si tratamentul pacientilor cu
risc maxim. Accesul vascular restrictiv ar putea influenta alegerea
terapiei.
8.4.5. Obezitatea, dieta
si anorexia
Recomandari
Clasa I
Aritmiile
ventriculare la pacientii cu obezitate, anorexie sau care tin
dieta trebuie tratate in acelasi mod ca aritmiile ventriculare la
pacientii cu alte boli, incluzand implantarea unui ICD sau pacemaker cand
sunt necesare. Pacientii care necesita ICD trebuie sa fie pe
terapie medicamentoasa optima cronica si sa
aiba o speranta de supravietuire rezonabila, cu un
status functional bun timp de mai mult de un an. (Nivel de dovezi: C)
Clasa IIa
Scaderea
controlata in greutate la pacientii obezi realimentarea atent
controlata la pacientii cu anorexie pot sa reduca eficient
riscul de aritmii ventriculare si MSC. (Nivel de dovezi: C)
Clasa III
Dietele
prelungite, neechilibrate, cu calorii putine, de semistarvare nu sunt
recomandate, ele pot fi daunatoare si pot provoca aritmii
ventriculare amenintatoare de viata. (Nivel de dovezi: C)
Tulburarile
de alimentatie si metodele prea rapide de corectare a acestora sunt
asociate cu MSC. La indivizii supraponderali acest risc este in mod particular
evident la cei cu obezitate severa care au o incidenta de 40-60
de ori mai mare comparativ cu indivizii cu aceeasi varsta din
populatia generala.564,565 Acesta este cel mai probabil
legat de aritmii ventriculare care pun in pericol viata, dar
modificarile la nivelul sistemului de conducere la indivizi tineri obezi,
victime ale MSC, au fost deasemenea raportate.566 Anumite persoane
obeze au intevalul QTc prelungit567,568 si studiile au aratat
de asemenea o crestere a dispersiei intervalului QT la aceste persoane.569
Cardiomiopatia intalnita in obezitate (ex, cardiomegalia,VS dilatat
si hipertrofia miocitelor in absenta fibrozei interstitiale) are
cea mai frecventa asociere cu MSC92 si acesta
asociere poate sa apara si la indivizii normotensivi.570
Complexele premature ventriculare sunt de 30 de ori mai frecvente la
pacientii obezi cu HVS comparativ cu pacientii normoponderali. Complexitatea
activitatii ventriculare ectopice se coreleaza cu diametrul
diastolic al VS precum si cu masa VS.571 Apneea in somn poate
juca un rol in geneza aritmiilor si a insuficientei cardiace la
indivizii obezi.572
Riscul
de MSC la persoanele obeze poate fi redus semnificativ prin scaderea in
greutate. Cardiomiopatia intalnita la persoanele obeze este
reversibila cel putin in stadiile intiale ale bolii573,574
ca si majoritatea modificarilor ECG inclusiv alungirea intervalului
QTc.568,569,575 Strategia de reducere a greutatii trebuie
initiata la toti pacientii obezi cu risc, dar acesta
implica o dieta hipocalorica bine echilibrata. Dietele
prelungite, dezechilibrate, extrem hipocalorice, de infometare (in special
dietele proteice lichide) au fost asociate cu aritmii cardiace si MSC prin
mecanisme variate. Astfel de diete trebuie evitate in special la cei cu
anomalii cardiace subiacente.576-580
Rata
mortalitatii in anorexia nervoasa oscileza intre 5 si
20% in studiile raportate, dar rata reala este probabil in jur de 6%.581
Pana la o treime din aceste decese, inclusiv cele din perioada
reluarii alimentatiei, se presupune ca sunt de cauze cardiace
dar nu exista date precise asupra MSC. Perioadele prelungite de infometare
induc nu numai modificari anatomice cum ar fi atrofia celulelor musculare
cardiace si efuziune pericardica,582 dar si
modificari ECG cum ar fi bradicardia sinusala si alungirea
inrevalului QTc, un efect care este probabil produs si de prezenta
concomitenta a tulburarilor electrolitice.582-584 De
aceea MSC este cea mai frecventa cauza de mortalitate in aceste
situatii. Greutatea redusa, indexul de masa corporala
scazut si scaderea rapida recenta in greutate sunt cei
mai importanti factori predictori independenti pentru alungirea
intervalului QTc.582 Majoritatea manifestarilor cardiace ale
anorexiei nervoase sunt complet revesibile prin realimentare corespunzatoare.582
Sindromul de realimentare este caracterizat de complicatii cardiace,
neurologice si hematologice declansate de perturbari
hidroelectrolitice intalnite in timpul realimentarii la indivizii cronic
infometati.585 Complicatiile cardiace ale acestui sindrom
apar de obicei in prima saptamana de realimentare si sunt
tipic asociate cu grade severe de malnutritie (mai putin de 70% din
greutatea ideala),586 hipofosfatemie587 si
nutritie parenterala totala.588
8.5. Bolile pericardului
Recomandari
Clasa I
Aritmiile
ventriculare aparute la pacientii cu boala pericardica
trebuie tratate in acelasi mod in care sunt tratate aritmiile la
pacientii cu alte boli, incluzand implantarea unui ICD sau pacemaker cand
sunt necesare. Pacientii care necesita ICD trebuie sa fie pe
terapie medicamentoasa optima cronica si sa aiba
o speranta de supravietuire rezonabila, cu un status
functional bun timp de mai mult de un an. (Nivel de dovezi: C)
MSC
poate sa apara in timpul bolii pericardice datorita unor
modificari patologice variate; acestea includ atat procesele constrictive
cat si restrictive, produse de traumatisme, inflamatie, neoplazii,
infectii. Nu exista dovezi care sa arate o legatura
specifica a aritmiilor ventriculare cu aceste boli. Cazurile de MSC la
pacientii cu boli pericardice sugereaza ca procesele hemodinamice
primare (tamponada cardiaca, hernierea miocardului prin pericard) sunt
responsabile de mare majoritate a MSC la acesti pacienti.589-592
8.6. Hipertensiunea
arteriala pulmonara
Recomandari
Clasa III
Terapia
antiaritmica profilactica nu este indicata in preventia
primara a MSC la pacientii cu hipertensiune arteriala
pulmonara sau alte boli pulmonare. (Nivel de dovezi: C)
MSC este
responsabila de decesul a 30-40% din pacientii cu HTAP. Apare mult
mai frecvent la pacientii cu HTAP primara decat la cei cu HTAP
tromboembolica.593 Pacientii cu MSC au presiunea
partiala a oxigenului mai mica.594 MSC la
pacientii cu HTAP severa se pare ca se datoreaza nu numai
aritmiilor ventriculare presupuse ci si disectiei sau rupturii
arterei pulmonare.595,596 Aritmiile cardiace pot sa apara
si ca rezultat al ischemiei. Dilatarea marcata a trunchiului arterei
pulmonare poate fi cauza ischemiei miocardice datorita compresiunii pe
care o poate realiza la nivelul trunchiului arterei coronare stangi.597
Cateterismul cardiac este asociat cu o crestere a riscului de deces,
incluzand FV documentata la acesta populatie.598 In
afara pacientilor cu HTAP, aritmiile ventriculare pot sa apara
la cei cu tulburari respiratorii in timpul somnului si pot fi responsabile
de MSC la pacientii cu apnee in somn.599
Nu a
fost realizat nici un trial cu terapie antiaritmica profilactica la
pacientii cu HTAP sau alte afectiuni pulmonare. Terapia
antiaritmica nu este indicata pentru preventia MSC la
pacientii cu HTAP sau alte afectiuni pulmonare.600,601 In
managementul aritmiilor asimptomatice la acesti pacienti trebuie
folosita o buna judecata clinica pentru ca pot fi
expusi efectelor proaritmice ale medicamentelor. Acesti pacienti
pot fi expusi la un risc inalt in timpul inteventiilor chirurgicale,
cum ar fi implantarea unui ICD.
8.7. Aritmii tranzitorii
datorate unor
cauze revesibile
Recomandari
Clasa I
Revascularizarea
miocardica trebuie efectuata, cand se impune, pentru a reduce riscul
de MSC la pacientii cu stop cardiac prin FV sau TV polimorfa in
contextul ischemiei acute sau infarctului micoardic. (Nivel de dovezi: C)
Daca
dezechilibrele electrolitice nu sunt dovedite a fi cauzale,
supravietuitorii stopului cardiac prin FV sau TV polimorfa la care
sunt descoperite tulburari electrolitice trebuie evaluati si
tratati in acelasi fel ca si in cazul stopului cardiac fara
anomalii electrolitice. (Nivel de
dovezi: C)
Pacientii
care fac TV monomorfa sustinuta in prezenta unor
medicamente antiaritmice sau a unor dezechilibre electrolitice trebuie
evaluati si tratati in mod similar cu pacientii cu TV
fara dezechilibre electrolitice sau prezenta unor medicamente
antiaritmice. Medicamentele antiaritmice si
dezechilibrele electrolitice nu trebuie presupuse a fi singura cauza a
TV monomorfe sustinute. (Nivel de dovezi: B)
Pacientii
cu TV polimorfa ascociata cu alungirea intevalului QT datorita
medicamentelor antiaritmice sau altor medicamente ar trebui
sfatuiti sa evite toate medicamente asociate cu alungirea
intevalului QT. O lista cu asemenea medicamente poate fi
gasita pe pagina de internet www. qtdrugs.org
si www.torsades.org (Nivel de dovezi: B)
Mortaliatatea
supravietuitorilor unui stop cardiac este mare chiar si atunci cand
cauza initiala pare sa fi fost o anomalie tranzitorie sau
corectabila si cea mai mare mortaliatate se datoreaza stopului
cardiac recurent.33,602 Majoritatea cauzelor reversibile sunt
ischemia acuta si dezechilibrele electrolitice. Alte cauze
potential reversibile ale stopului cardiac sunt efectele proaritmice ale
medicamentelor antiaritmice.603 Pana in prezent nici un trial
nu a evaluat efectele revascularizarii miocardice asupra TV sau FV. Cu
toate acestea studiile observationale sugereaza ca:
TV
monomorfa sustinuta la pacientii cu infarct miocardic in
antecedente este putin probabil sa fie influentata de
revascularizarea miocardica.330
Revascularizarea miocardica este terapia suficienta
numai la pacientii care au supravietuit unei fibrilatii
ventriculare asociata cu ischemie miocardica atunci cand
functia ventriculara este normala si nu exista
istoric de infarct miocardic.604
Mortalitatea
pe termen scurt (in spital) la pacientii cu fibrilatie
ventriculara primara care complica faza acuta a infarctului
miocardic este inalta. Cu toate acestea pacientii care au
supravietuit spitalizarii initiale dupa un infarct miocardic cu
unda Q au o rata de supravietuire aproape identica cu a
pacientilor fara FV in faza acuta a infarctului miocardic.605
Riscul scazut pentru un stop cardiac ulterior pare sa fie valabil
numai pentru pacientii cu infarct cu unda Q; pacientii cu
infarct definit prin cresterea biomarkerilor, fara sa
dezvolte unda Q au un risc semnificativ crescut de stop cardiac tardiv.606,607
Ischemia tranzitorie determinata de spasmul coronarian poate determina TV
polimorfa sau FV.608 In asemenea cazuri tratamentul spasmului
coronarian poate fi suficient pentru a preveni aritmia recurenta.609,610
Spasmul coronarian poate creste riscul de aritmii ventriculare si
moarte subita cardiaca.
Dezechilibrele
electrolitice incluzand hipopotasemia si hipomagneziemia favorizeaza
dezvoltarea TV la pacientii predispusi care primesc medicamente
antiaritmice sau alte medicamente asociate cu SQTL. Cu toate acestea,
hipopotasemia poate fi rezultatul stopului cardiac si nu ar trebui
considerata o cauza a acestuia, cu exceptia unor
circumstante neobisnuite.611 Corectarea hipopotasemiei nu
afecteaza inductibilitatea TV monomorfa dupa infarctul
miocardic. Anomaliile electrolitice nu trebuie considerate cauza stopului
cardiac decat in prezenta SQTL indus medicamentos.
La
pacientii care dezvolta TV polimorfa in asociere alungirea
intervalului QT indusa medicamentos, renuntarea la aceste
medicamente este de obicei suficienta pentru a preveni recurenta
aritmiei. Daca functia ventriculara este normala evitarea
acestor medicamente si corectarea dezechilibrelor electrolitice este
necesara. In schimb, daca functia ventriculara este
anormala stopul cardiac si sincopa nu ar trebui atribuite exclusiv
medicamentelor antiaritmice, si evaluarea si tratamentul trebuie
sa fie similar pacientilor cu astfel de evenimente in absenta
medicamentelor antiaritmice.
Ocazional,
pacientii dezvolta TV monomorfa sustinuta numai in
prezenta unor medicamente antiaritmice fara alungirea intervalului
QT. In astfel de cazuri se pare ca aparitia TV spontane este
dependenta de medicamentele administrate. La marea majoritate a acestor
pacienti, TV monomorfa poate fi indusa in timpul studiilor
electrofiziologice in absenta medicamentelor antiaritmice.612,613
9. Aritmiile
ventriculare asociate cardiomiopatiilor
9.1.Cardiomiopatia
dilatativa (nonischemica)
Recomandari
Clasa I
Studiul
electrofiziologic este util pentru diagnosticul tahicardiei prin reintrare in
ramura si pentru a ghida ablatia la pacientii cu CMD
nonischemica. (nivel de dovezi: C
Studiul
electrofiziologic este util pentru evaluarea pacientilor cu CMD
nonischemica care prezinta palpitatii, tahicardie cu complex
QRS larg, presincopa sau sincopa. (nivel de dovezi: C)
ICD
trebuie implantat la pacientii cu CMD nonischemica si
disfunctie VS semnificativa care au TV sustinuta si
FV, primesc terpie medicala optima pe termen lung si au o
speranta de supravietuire rezonabila cu un status
functional bun mai mult de un an. (nivel
de dovezi: A
Tratamentul
cu ICD este recomandat pentru preventia primara in scopul reducerii
mortalitatii totale prin reducerea MSC la pacientii cu CMD
nonischemica care au FEVS mai mica sau egala cu 30-35%,
clasa functionala NYHA II sau III si primesc tratament
medical optim pe termen lung si au o speranta de
supravietuire rezonabila cu un status functional bun timp de
peste un an. (nivel de dovezi: B
Clasa IIa
Implantarea
unui ICD poate fi benefica la pacientii cu sincopa
inexplicabila, disfunctie VS semnificativa si CMD
nonischemica care primesc terapie medicala optima pe termen lung
si au o speranta de supravietuire rezonabila cu un
status functional bun timp de peste un an. (nivel de dovezi: C)
Implantarea
unui ICD poate fi eficienta pentru terminarea TV sustinuta la
pacientii cu functia VS normala sau aproape normala si
CMD nonischemica care primesc terapie medicala optima pe termen
lung si au o speranta de supravietuire rezonabila cu
un status functional bun timp de peste un an. (nivel de dovezi: C) (vezi sectiunea 1.2.)
Clasa IIb
Amiodarona poate fi
luata in considerare la pacientii cu TV sustinuta sau FV
care au CMD nonischemica. (nivel de
dovezi: C)
Implantarea
unui ICD poate fi luata in considerare la pacientii cu CMD nonischemica,
FEVS mai mica sau egala cu 30-35%, clasa functionala
NYHA I, care primesc terapie medicala optima pe termen lung si
au o speranta de supravietuire rezonabila cu un status functional
bun timp de peste un an. (nivel de
dovezi: C) (vezi sectiunea 1.2.)
Consideratiile
luate de Comitetul de Redactare in formularea recomandarilor pentru
aceasta sectiune sunt discutate in detaliu in introducere.
9.1.1 Stratificarea riscului
La 5 ani
mortalitatea prin CMD a fost recent estimata la 20%, MSC reprezentand
aproximativ 30% din decese.614,615 Aritmiile ventriculare simptomatice
sau asimptomatice sunt frecvente, dar sincopa sau MSC sunt rar prima
manifestare a bolii.616,617 Incidenta MSC este mare la
pacientii cu indicatori de boala cardiaca mai avansata
care au de asemenea cel mai mare risc pentru toate cauzele de mortalitate.
Desi TV si/sau FV sunt considerate cel mai comun mecanism al MSC,
bradicardia, embolia pulmonara, disociatia electromecanica
si altele reprezinta pana la 50% din cazurile de MSC la
pacientii cu insuficienta cardiaca avansata.107,618,619
Stratificarea riscului este dificil de realizat la pacientii cu CMD. MSC
apare mai putin frecvent la pacientii cu boala cardiaca
care nu este avansata dar proportia MSC din toate decesele este mare
la acest grup de pacienti.617,618,620 Predictorii
mortalitatii generale sunt si cei pentru MSC si
reflecta in general severitatea bolii (FE, volumul telediastolic, varsta
inaintata, hiponatremia, presiunea in capilarul pulmonar, hipotensiunea
arteriala, fibrilatia atriala).614 Din nefericire,
acesti factori predictori nu sunt specifici pentru moartea aritmica
si nu sunt folositori la pacientii cu boala cardiaca mai
putin severa.3,621 Chiar si fractia de
ejectie redusa (mai putin de 20%) poate sa nu aiba o
valoare predictiva pozitiva mare pentru MSC.622-624
Sincopa a fost asociata cu un risc inalt de MSC indiferent de etiologia sa
dovedita223,625 si pacientii cu ICD primesc un
numar de socuri adecvate similar cu cei din cohorte de preventie
secundara.223,625,626 Complexele ventriculare premature
si TVNS se coreleaza cu severitatea bolii cardiace si apar la
majoritatea pacientilor cu disfunctie severa de VS.619,627,628
Folosirea aritmiilor ventriculare la stratificarea riscului are astfel
utilitate limitata si se asteapta a fi sensibile dar nu
si specifice. S-a sugerat ca prezenta TVNS poate fi mai
specifica pentru stratificarea riscului la indivizii cu functie VS
mai buna.3 Inducerea TV prin studii electrofiziologice a fost
asociata cu riscul de MSC,625 dar din nefericire esecul in
inducerea TV apare la majoritatea indivizilor predispusi la moarte
subita.129,627,629,630 Microalternanta de unda T a
prezis riscul de MSC intr-un studiu cohorta care a inclus 137
pacienti cu CMD.151 Studiul a inclus 37 de pacienti cu
indicatie pentru ICD si cele mai multe endpoint-uri s-au realizat in
acest grup. Cu toate acestea, valoarea predictiv pozitiva a fost relativ
modesta (0,22) ca si FE mai mica decat 35% (0,15). CMD
idiopatica are o etiologie heterogena dar in cel putin 40% din
cazuri are transmitere familiala, de obicei autosomal dominanta cu
penetranta variabila, dar si X-linkata.631-634
Din nefericire, informatiile genetice nu sunt folositoare in acest moment
pentru stratificarea riscului.
9.1.2. Studiul
electrofiziologic
In CMD
studiul electrifiziologic ocupa un rol minor in evaluarea si
managementul tahicardiilor ventriculare. Acest lucru este in legatura
cu slaba inductibilitate si slaba reproductibilitate a TV in timpul
studiilor electrofiziologice precum si cu valoarea predictiv
redusa.203,204 Trialul multicentric CAT a inclus 104
pacienti cu CMD si FEVS mai mica de 30% fara TV
sustinuta sau FV.635 TVNS in timpul monitorizarii
Holter a fost inregistrata in 52% din cazuri. Folosind protocolul complet
al studiului electrofiziologic numai 2,9% din pacienti au avut TV
sustinuta si 9,6% au avut FV indusa. Cu toate acestea,
pacientii simptomatici pot avea tahicardii supraventriculare variate,
flutter atrial tipic sau atipic sau fibrilatie atriala fiind nevoie
de studiu electrofizilogic pentru diagnostic sau pentru realizarea
ablatiei. Reintrarea prin ramuri poate fi suspectata la
pacientii cu CMD, tulburari de conducere intraventriculara in
timpul ritmului sinusal si tahicardie cu pattern de BCRS.636
9.1.3. Management
Tratamentul
CMD este adesea bazat pe experienta medicului si situata
individuala a pacientului. Medicamentele care au redus mortalitatea la
pacientii cu insuficienta cardiaca, ca de exemplu
betablocantele si IECA, au redus de asemenea si MSC.622,637-640
Amiodarona este in general preferata pentru a trata pacientii cu
aritmii simptomatice datorita abesntei efectelor hemodinamice
negative semnificative si efectului proaritmic redus desi trialuri
comparative controlate nu sunt disponibile. S-a sugerat, in trialuri
necontrolate, ca amiodarona reduce mortalitatea.641 In studii
controlate amodarona a redus incidenta MSC in populatia de
pacienti cu CMD predominant nonischemica,637 dar nu
si intr-un studiu cu pacienti cu insuficienta cardiaca
unde majoritatea aveau boala coronariana.638 Implatarea
unui ICD s-a dovedit a fi superioara amiodaronei in preventia
secundara a TV si FV in studiile unde majoritatea pacientilor
aveau boala coronariana.266,642,643 Subgrupul de
pacienti cu CMD nonischemica a beneficiat de implantarea unui ICD mai
mult decat pacientii coronarieni.644 Rolul ICD in profilaxia
primara a fost controversat. Trialul CAT a inrolat pacienti recent
diagnosticati cu CMD si a fost intrerupt precoce datorita
inutilitatii printr-o incidenta mai mica decat era
asteptata a mortalitatii generale.635 Acesta a
fost un studiu relativ mic (50 de pacienti in bratul cu ICD si
54 pacienti in grupul de control), desi la cinci ani au fost
raportate mai putine decese in grupul cu ICD comparativ cu grupul control
(13 versus 17). In studiul AMIOVERT645 103 pacienti cu CMD care
aveau fractie de ejectie mai mica de 35% si TVNS au fost
randomizati pentru amiodarona sau ICD. Obiectivul primar a fost
mortalitatea totala si studiul a fost intrerupt prematur datorita
inutilitatii. Studiul DEFINITE646-648 a randomizat 458 de
pacienti diagnosticati cu cardiomiopatie nonischemica cu
fratie de ejectie mai mica decat 35% si frecvente BPV sau
TVNS, care au primit cea mai buna terapie medicala cu sau
fara implantarea unui ICD. S-a inregistrat o tendinta de
reducere a mortalitatii la pacientii cu ICD, dar care nu a fost
semnificativa statistic.
Pacientii
din studiul DEFINITE au fost randomizati sa primeasca cea mai
buna terapie medicala cu sau fara implantarea unui ICD si
obiectivul primar a fost mortalitatea de toate cauzele. La doi ani
mortalitatea a fost de 13,8% in grupul cu terapie standard comparativ cu 8,1%
in grupul de pacienti care au beneficiat de implantarea unui ICD, ceea ce
inseamna o reducere absoluta a riscului de 5,7% si o reducere
relativa de 35% la cei cu ICD implantat. Aceasta nu reprezinta o
reducere semnificativ statistica (p=0,06) dar rezultatele au fost
comparabile cu cele din trialuri similare.647,648 Studiul SCD-HeFT a
comparat amiodarona, ICD si cea mai buna terapie medicala la
2521 pacienti cu boala coronariana sau cardiomiopatie
nonischemica, cu insuficienta cardiaca clasa II sau III
NYHA si FE mai mica de 35%. Bratul cu amiodarona a fost
dublu-orb si versus placebo. Perioada media de urmarire a fost de
45,5 luni. Mortalitatea totala in grupul care a primit terapie
medicala a fost de 7,2% pe an dupa cinci ani cu o reducere a riscului
relativ cu 23% in grupul cu ICD comparativ cu grupul placebo (CI 0,62-0,96,
p=0,007). Reducerea riscului relativ a fost comparabila la cei cu
disfunctie de VS datorita infarctului miocardic si grupul cu
cardiomiopatie nonischemica dar mortalitatea absoluta a fost mai
redusa in grupul cu cardiomiopatie nonischemica, cu un numar
mai mare de pacienti care trebuie tratati pentru a salva o
viata. Nu a existat nici o diferenta in reducerea
mortalitatii la cei tratati cu amiodarona si grupul
placebo.8 Stratificarea suplimentara a riscului poate reduce
numarul de pacienti care trebuie tratati pentru a salva o
viata in acesta populatie.649 Cu exceptia
trialului DEFINITE (25% in grupul cu ICD) trialurile care au evaluat
implantarea ICD pentru profilaxia primara la pacientii cu CMD nu au
inclus si pacienti asimptomatici cu clasa functionala NYHA
I si de aceea eficienta ICD la acesta populatie nu este pe
deplin cunoscuta.650 Pentru ca mortalitatea este
redusa in acest subgrup beneficul terapiei cu ICD la acesti
pacienti este in cel mai bun caz moderat.
9.1.4. Analiza genetica
Aplicabilitatea
clinica a analizei genetice la pacientii cu CMD este inca
limitata, cunostintele actuale nepermitand genotiparea
majoritatii pacientilor cu afectare clinica. La
pacientii cu CMD si bloc atrioventricular si la pacientii
cu CMD si afectiuni ale muschilor scheletici exista o
probabilitate mai mare de genotipare. Cand este identificata o
mutatie patogenica devine posibila stabilirea unui diagnostic
presimptomatic al bolii printre membrii familiei existand si
posibilitatea de a fi consiliati genetic, de a monitoriza progresia bolii
si de a evalua riscul transmiterii bolii la descendenti. Pe baza
cunostintelor actuale, analiza genetica nu contribuie in plus
la stratificarea riscului in CMD.
9.2. Cardiomiopatia
hipertrofica
Recomandari
Clasa I
Terapia
cu ICD trebuie folosita la pacientii cu CMH care au TV
sustinuta si/sau FV, care primesc tratament medical optim pe
termen lung si la care ne asteptam la o supravietuire
rezonabila cu un status functional bun mai mult de un an. (nivel de dovezi: B)
Clasa IIa
Implantarea
unui ICD poate fi eficienta in profilaxia primara a MSC la
pacientii cu CMH care au unul sau mai multi factori majori de risc
pentru MSC (vezi tabelul 7), care primesc tratament medical optim pe termen
lung si la care ne asteptam la o supravituire
rezonabila cu un status functional bun mai mult de un an. (nivel de dovezi: C)
Terapia
cu amiodarona poate fi eficienta pentru tratamentul pacientilor
cu CMH si istoric de TV sustinuta si/sau FV atunci cand
terapia cu ICD nu este posibila. (nivel
de dovezi: C)
Clasa IIb
Studiul
electrofiziologic pot fi utilizat pentru evaluarea riscului de MSC la
pacientii cu CMH. (nivel de dovezi:
C)
Amiodarona
poate fi utilizata pentru profilaxia primara a MSC la pacientii
cu CMH care au unul sau mai multi factori majori de risc pentru MSC
daca implantarea ICD nu este posibila. (nivel de dovezi: C)
Tabelul 7.
Factori de risc pentru moartea subita cardiaca la pacientii cu
CMH
|
Factori
de risc majori
|
Posibili la unii pacienti
|
|
Stop cardiac (FV)
TV
spontana resuscitata
Istoric
familial de moarte subita precoce
Sincopa
neexplicata
Grosimea
peretelui VS ≥30 mm TA la efort anormala
TV nesustinute spontane
|
FA
Ischemie
miocardica
Obstructie
in tractul de ejectie VS
Mutatii
high-risk
Efort fizic intens (competitiv)
|
|
Modificat dupa Maron BJ, McKenna WJ, Danielson GK, et al.
American College of Cardiology/European Society of Cardiology clinical expert
consensus document on hypertrophic cardiomyopathy. A report of the American
College of Cardiology Foundation Task Force on Clinical Expert
Consensus Documents and the European Society of Cardiology Committee for
Practice Guidelines. J Am Coll Cardiol 2003;42:1687713.
FA, fibrilatie atriala; TA,
tensiune arteriala; VS, ventricul stang; FV, fibrilatie
ventriculara; TV, tahicardie
ventriculara.
|
9.2.1. Stratificarea
riscului
Majoritatea
pacientilor cu CMH sunt asimptomatici si prima manifestare poate fi
MSC.651-657 MSC este in general legata de aritmii ventriculare
cu o contributie variata a factorilor declansatori ca ischemia,
obstructia in calea de ejectie sau fibrilatia atriala.653-656,658
MSC este mai putin frecvent prin bradicardie.659 Mortalitatea
anuala prin CMH a fost estimata la 6% in centrele tertiare,653,660,661
dar studiile locale au sugerat o prezenta ca este o boala
mai benigna la majoritatea indivizilor, cu o mortalitate anuala de 1%
sau mai putin.622-667 Incidenta relativ redusa este
o problema pentru stratificarea riscului pentru ca rezultatele fals
pozitive ale unui marker le pot domina pe cele adevarat pozitive. Unii markeri
de MSC au fost indicati de studii observationale.98,662,669-677
Intr-un studiu, 23 din 480 de pacienti au murit subit intr-o
perioada medie de urmarire de 6,5 ani.678 Riscul de MSC a
fost in relatie directa cu grosimea peretelui VS; riscul pe 20 de ani
la pacientii cu grosime a peretelui mai mica de 20 mm a fost practic
nul, spre deosebire de cei cu grosimea mai mare sau egala cu 30 mm, la
care mortalitatea a fost aproape de 40%. Cei din acest ultim grup erau mai
tineri si frecvent asimptomatici. Cinci din cei 12 pacienti sub 18
ani au murit subit. A fost sugerat ca pacientii cu hipertrofie importanta
de sept ar avea si alti factori de risc, valoarea98,679 predictiva
independenta a hipertrofiei de sept fiind astfel neclara. Gradul
obstructiei tractului de ejectie se asociaza cu moartea de
cauza cardiovasculara674,678 dar nu cu MSC.678 Atletii
cu CMH nu ar trebui sa participe la sporturile intens solicitante, cu
posibila exceptie a celor de intensitate dinamica sau statica
joasa.680-682 Participarea la activitati atletice cu
solicitare mica sau moderata poate fi permisa la pacienti
cu risc mic.683
RMN cardiac684 si CT685 pot fi
utile in evaluarea bolii si a riscului de MSC. Antecedentele
heredocolaterale de MSC sunt asociate cu un risc mai mare.653,660,686 Acest
aspect este legat logic de sugestia ca anumite anomalii genetice specifice
au fost asociate cu riscul crescut de MSC;687-691 este de
asteptat ca rolul testelor genetice in predictia MSC sa
creasca.687 Sincopa se asociaza cu riscul de MSC.657,692-695
Severitatea altor simptome ca dispneea, durerea precordiala si
intoleranta la efort nu s-a corelat cu un risc mai mare de MSC.695,696
Un raspuns aplatizat sau hipotensiv la testul de efort la
pacientii sub 40 de ani este un factor de risc pentru MSC, dar cu valoare
predictiva pozitiva mica.658 Raspunsul normal
al tensiunii arteriale a identificat un grup cu risc mic.658,697-699 Prezenta
TV pe monitorizarile Holter665,696,700-702 se asociaza cu
un risc mai mare de MSC, desi valoarea predictiva pozitiva este
relativ mica. Absenta TV pare sa aiba o valoare
predictiva negativa buna. TV indusa in laboratorul de
electrofiziologie97 a fost de asemenea asociata cu riscul mai
mare de MSC, dar unii autori au sugerat ca inducerea TV prin tehnici
agresive de stimulare isi pierde din specificitate.703,704
Un document de consens al Colegiului American de
Cardiologie si al Societatii Europene de Cardiologie a
impartit factorii cunoscuti de risc pentru MSC in majori
si posibili la anumiti pacienti705 (vezi
Tabelul 7). Este clar ca multi din factorii de risc listati in
Tabelul 7 sunt interdependenti si ca factorii independenti
majori se pot dovedi a fi extensia bolii si anomaliile genetice.
Absenta factorilor de risc a identificat un grup cu risc mic, dar valoarea
predictiva pozitiva a oricarui marker luat singur este
limitata. Stratificarea riscului bazata pe mai multi markeri
probabil va imbunatati acuratetea predictiei.693
9.2.2. Studiul
electrofiziologic
Valoarea
testului electrofiziologic in CMH este controversata.7 In
1989, Fananapazir et al. au aratat folosind 2 stimuli prematuri ca
numai 16% din pacientii cu CMH si sincopa sau stop cardiac
resuscitat au TV sustinuta inductibila. Intr-un studiu ulterior,
aceiasi autori au publicat date despre 230 de pacienti, incluzandu-i
pe cei 155 de pacienti raportati anterior.97,707 Pacientii
cu TV inductibila au avut un prognostic mai sever; TV indusa a fost
frecvent polimorfa. Testul electrofiziologic pozitiv a fost considerat un
factor de prognostic important, alaturi de istoricul de sincopa sau
stop cardiac. Intr-un studiu prospectiv la 29 de pacienti cu CMH, dintre
care 8 cu sincopa, studiul electrofiziologic cu pana la 3
extrastimuli la 3 lungimi ale ciclului, inclusiv cu stimulare in VS, nu a putut
deosebi pacientii cu sincopa in antecedente de ceilalti.224
La pacientii care au primit un ICD pentru preventie primara rata
de descarcare adecvata a fost de 5% pe an.708
9.2.3. Management
Principalele
mijloace terapeutice medicamentoase la pacientul simptomatic au fost betablocantele
si verapamilul, care probabil isi exercita efectul prin
reducerea frecventei cardiace si a contractilitatii,653,660
Disopiramida a fost folosita datorita presupusului efect inotrop
negativ.709 Fibrilatia atriala poate fi o problema,710,711
prin deteriorarea clinica brusca rezultata din frecventa
ventriculara rapida si pierderea umplerii atriale. In plus, este
asociata cu risc mare de embolii, insuficienta cardiaca
sau moarte. Riscul mare de embolii justifica anticoagularea cu
warfarina desi eficienta nu a fost validata la acest grup
de pacienti printr-un trial randomizat mare. Amiodarona este larg
folosita si este considerata cel mai eficient antiaritmic,
desi nu exista trialuri controlate comparative mari.710,712
Terapia medicamentoasa nu s-a dovedit a preveni progresia bolii la
pacientii asimptomatici si in general nu este indicata.
Totusi, tratamentul cu betablocante si/sau blocanti de calciu
este tentanta chiar la asimptomatici, daca sunt tineri si au
hipertrofie severa sau gradiente semnificative.660 Este
rezonabil sa credem ca terapia medicamentoasa optima
si controlul comorbiditatilor vor reduce riscul de MSC,
desi acest lucru nu a fost demonstrat riguros.
Desi
nu exista studii randomizate, implantarea de ICD a fost folosita la
pacientii cu istoric de stop cardiac, TV sustinuta sau
fibrilatie ventriculara, un procent mare de pacienti primind
descarcari adecvate in perioada de urmarire, la o rata de
11% pe an.708 Implantarea de defibrilator pentru profilaxie
primara la un grup de pacienti pe baza riscului perceput mare de MSC
(sincopa, istoric familial de MSC, TVNS, TV inductibila, grosime a
septului mai mare sau egala cu 30 mm) au dus la o rata mai mica
de descarcare adecvata, de 5% pe an.708 Amiodarona s-a
dovedit folositoare in preventia MSC in studii nerandomizate,712,713
in timp ce alte studii au aratat imbunatatiri ale
simptomatologiei fara o preventie completa a MSC. Studii
versus placebo sau studii care sa compare ICD cu amiodarona nu sunt
disponibile si rolul amiodaronei in preventia MSC este neclar. Este
putin probabil ca amiodarona sa fie superioara ICD si este
posibil ca un studiu comparativ sa nu fie niciodata realizat.716
ICD nu este indicat la majoritatea pacientilor asimptomatici cu CMH care
vor avea o evolutie relativ benigna. Rolul ICD trebuie individualizat
la pacientii considerati a avea risc mare de MSC.3,717,718 Desi
o stratificare exacta a riscului nu a fost validata, pacientii
cu multipli factori de risc (mai ales hipertrofia septala severa, mai
mare sau egala cu 30 mm) si cei cu MSC (mai ales multiple cazuri) la
rudele apropiate par a avea un risc suficient de mare pentru a lua in
considerare terapia cu ICD.
9.2.4. Analiza genetica
Analiza
genetica este utila la familiile cu CMH, pentru ca daca se
identifica o mutatie patogena devine posibil diagnosticul
presimptomatic existand si posibilitatea de a fi consiliati
genetic, de a monitoriza progresia bolii si de a evalua riscul
transmiterii bolii la descendenti. Analiza genetica poate contribui
la stratificarea riscului in anumite circumstante.
9.3. Cardiomiopatia
aritmogena de ventricul drept
Recomandari
Clasa I
ICD
este recomandat pentru preventia mortii subite la pacientii cu
CAVD cu TV sustinuta sau FV documentate ce primesc tratament farmacologic
optim si au o speranta de viata rezonabila cu un
bun status functional mai mult de 1 an. (Nivel de dovezi: B)
Clasa IIa
ICD poate fi eficient
pentru preventia MSC la pacientii cu CAVD cu boala extinsa,
inclusiv cei cu afectare de VS, cu MSC la unul sau mai multi membrii din
familie afectati de boala, sincopa neexplicata cand TV sau
FV nu au putut fi excluse ca fiind cauze ale sincopei, daca primesc
tratament farmacologic optim si au o speranta de viata
rezonabila cu un bun status functional mai mult de un an. (Nivel de dovezi: C)
Amiodarona
sau sotalolul pot fi eficiente pentru tratamentul TV sustinute si FV
la pacientii cu CAVD cind implantarea ICD nu este realizabila. (Nivel de dovezi: C)
Ablatia
poate fi utila ca terapie aditionala la pacientii cu CAVD
si TV recurente in ciuda terapiei medicamentoase antiaritmice optime. (Nivel de dovezi: C)
Clasa IIb
Studiul
EF poate fi util pentru evaluarea riscului de MSC la pacientii cu CAVD. (Nivel de dovezi: C)
9.3.1. Stratificarea
riscului
CAVD
(displazia) este suspectata de obicei la barbatii tineri, cu
aritmii cu originea in VD sau la rudele indivizilor cu CAVD cunoscuta.
Sincopa, presincopa si mai putin frecvent insuficienta
biventriculara sunt de asemeni observate.719,720 Aritmiile
ventriculare au morfologie de BRS si pot fi reprezentate de ectopia
ventriculara simpla, TV nesustinute sau sustinute, FV.
CAVD trebuie sa fie luata in considerata alaturi de TV
idiopatica din tractul de ejectie al VD la pacientii cu extrasistole
ventriculare si TV cu originea in tractul de ejectie al VD. In
comparatie cu CAVD, TV idiopatica din tractul de ejectie al VD nu
este asociata de obicei cu modificarile ECG vazute in CAVD, este
mai frecventa la femei si este initiata de perfuzia cu
isoproterenol si nu prin SEF.721,722 Pe electrocardiograma
pacientilor cu CAVD se observa frecvent inversarea undelor T in
derivatiile precordiale, de obicei de la V1 la V3,
si durata QRS mai mare de 110 ms.721 Undele epsilon
(potentiale de voltaj redus ce urmeaza complexului QRS) sunt
caracteristice dar sunt relativ rare si potentialele tardive sunt
pozitive la mai mult de 50% din cazuri.721,723,724
Din
nefericire moartea subita cardiaca este frecvent prima manifestare a
bolii.96,725,726 O schema de diagnostic standardizata a fost
realizata pentru stabilirea diagnosticului clinic pe baza unor scoruri.727
Incidenta anuala a MSC a variat de la 0,08% la 9%. Dintr-un
numar de 27 de autopsii, s-a determinat ca 24 de pacienti au decedat
subit si 3 au decedat datorita IC congestive.731 Moartea
subita cardiaca apare relativ frecvent in timpul efortului sau
stresului, dar moartea subita fara o provocatoare nu este
neobisnuita.732 Intr-un studiu italian, pana la 25%
din MSC au fost legate de CAVD.733 Chiar daca moartea
subita este intilnita de obicei la pacientii cu anomalii
evidente ale VD, ea poate apare si la cei cu anomalii microscopice si
fara dilatare de VD.734 Dilatarea VD, anomaliile de
repolarizare din derivatiile precordiale si afectarea VS au fost
asociate cu riscul de moarte subita.730,735,736 Anumite tipuri
genetice pot fi asociate cu un risc mai mare de MSC.737 MSC la unul
sau mai multi membri ai familiei poate sugera un risc mai mare la un
individ cu CAVD, dar acesta nu a fost bine cuantificat.170
9.3.2. Studiul
electrofiziologic
Manifestarile
aritmice ale bolii sunt variabile.96 Rolul prognostic al SEF la
pacientii cu extrasistole ventriculare izolate sau TVNS este necunoscut.
Raspunsul la studiul electrofiziologic poate fi influenjat de severitatea
bolii. Progresia boli trebuie sa fie luata in considerare. Studiul
electrofiziologic pentru stratificarea risculuzi a fost evaluat la un
numar limitat de pacienti. Di Biase si colab.738 au
utilizat studiul electrofiziologic la 17 pacienti cu displazie
moderata si s-a indus TV numai la pacientii cu TV
sustinuta spontana. TV a fost indusa la 90% din cei 12
pacienti cu TV sustinuta spontana.739 Valoarea
predictiva pozitiva pentru TV recurenta a fost de numai 55%. TV
sustinuta nu a putut fi indusa la 20 de pacienti care aveau
TVNS.736 In acest studiu, inductibilitatea a fost de 88% la 24 de
pacienti din 27 care aveau TV sustinute. Studiul electrofiziologic in
general este utilizat pentru reproducerea TV clinice si ghidarea
ablatiei.740,741
9.3.3. Management
Tratamentul
CAVD este adesea in functie de prezentarea fiecarui pacient si
de experienta medicului. ICD a fost utilizat la pacientii cu sincope
neexplicate, TV sustinute sau FV, cu o incidenta made de
socuri adecvate.742 Desi nu exista trialuri
randomizate mari care sa sprijine aceasta abordare, situatia
este destul de asemanatoare cu alte situatii, cum ar fi
cazurile de IM vechi, unde aceste indicatii sunt bine stabilite.266,718,
741,743 ICD la pacienti cu istoric familial de MSC sau sincope
neexplicate este intuitiv necesar dar nu este dovedit. Impactul terapei
farmacologice pe mortalitate nu este stabilit. Ablatia prin RF a fost
utilizata la pacienti cu TV refractare la tratamentul medical.744
Eliminarea uneia sau mai multor tahicardii cliniceprin ablatie cu RF
este un tratament simptomatic util, dar este posibil sa nu fie
suficienta pentru preventia MSC. Interventia chirurgicala
de deconectare electrica totala a VD s-a dovedit eficienta la
pacientii refractari la tratamentul medicamentos, cu functie
normala de VS dar are un risc postoperator mare de IC dreapta.745
Transplantul cardiac si dispozitivele de asistare ventriculara sunt o
optiune la pacientii cu insuficienta biventriculara.
9.3.4. Testele genetice
Sunt utile in familiile cu CAVD deoarece cand este identificata o
mutatie patogenica devine posibila stabilirea unui diagnostic
presimptomatic al bolii printre membrii familiei, existand si
posibilitatea de a fi consiliati genetic, de a monitoriza progresia bolii
si de a evalua riscul transmiterii bolii la descendenti. Pe baza
cunostintelor actuale, analiza genetica nu contribuie la stratificarea
riscului in CAVD.
9.4. Bolile neuromusculare
Recomandari
Clasa I
Pacientii
cu boli neuromusculare care au aritmii ventriculare trebuie tratati in
general in acelasi mod ca pacientii fara boli
neuromusculare. (Nivel de dovezi: A)
Clasa IIb
Cardiostimularea
permanenta poate fi considerata pentru boli neuromusculare cum ar
fi: distrofia musculara miotonica, sindromul Kearns-Sayre, distrofia
Erb, atrofia musculara peroneala, cu orice grad de bloc AV (inclusiv
blocul de gradul I) cu sau fara simptome, deoarece progresia
afectarii sistemului de conducere poate fi imprevizibila. (Nivel de dovezi: B)
Bolile neuromusculare
mostenite pot predispune la aritmii atriale, tulburari de conducere,
blocuri AV de grad inalt, TV monomorfe, TV polimorfe si MSC.746-755
O lista exhaustiva a bolilor neuromusculare mostenite depaseste
scopul acestui ghid. Tabelul 8 prezinta cele mai comune boli asociate cu
manifestari cardiovasculare, produse in anumite cazuri de degenerarea
sistemului specializat de conducere si in alte cazuri prin modificari
degenerative ale miocardului atrial si ventricular ce favorizeaza
aparitia cardiomiopatiilor si aritmiilor ventriculare. In multe
cazuri electrocardiograma de repaus este anormala, cu bloc AV de gradul
I, bloc de ramura, unde Q, anomalii ale fazei de repolarizare (ST-T) sau
BPV.753,754
Prezentarea
clinica, indicind substratul potential de MSC, este foarte variabil,
mergand de la asimptomatic la simptome cum ar fi sincopa, senzatia de cap
gol si palpitatii. Nu exista serii mari de pacienti
asimptomatici tratati cu dispozitive si momentul implantarii unui
pacemaker/defibrilator nu este clar bazindu-ne pe datele din literatura
actuala. In general cu cat afectarea cardiaca (structurala sau a
sistemului de conducere) este mai avansata cu atat probabilitatea de
aparitie a unei aritmii importante este mai mare. MSC este o
complicatie bine cunoscuta a unor boli neuromusculare si
progresia anomaliilor de conducere poate fi imprevizibila.756-762
Odata ce implicarea cardiaca apare, in special la pacientii cu
distrofii musculare, medicul trebuie sa foloseasca un prag jos in
evaluarea simptomelor si a modificarilor ECG care indica
necesitatea implantarii unui pacemaker, defibrilator sau efectuarea unui
studiu electrofiziologic. Indiferent de simptomatologie trebuie realizat un
screening al implicarii cardiace cu ajutorul ECG de repaus si a
ecocardiografiei. Probabilitatea relativa a unui pacient cu boala
neuromusculara mostenita sa dezvolte o tulburare de
conducere, aritmie ventriculara sau cardiomiopatie este prezentata in
Tabelul 8. In general, indicatiile dispozitive implantabile la pacientii
cu boala Duchenne, Becker, cardiomiopatii cu transmitere X-linkata,
membru-centura 2C-2F si ataxie Friedreich trebuie sa ghidurile
standard pentru cei cu cardiomiopatie dilatativa. Lista completa a
indicatiilor se gaseste in ACC/AHA/NASPE 2002 Guidelines
Update for Implantation of Cardiac Pacemakers and Antiarrhythmic Devices.1
Implantarea unui pacemaker sau defibrilator la pacientii asimptomatici cu
ECG normal si fara manifestari cardiovasculare nu este de
obicei indicata.
Indicatiile
pentru tratament farmacologic sau dispozitiv implantabil la pacientii cu
miastenia gravis, sindrom. Guillaiin-Barre sau evenimente vasculare cerebrale
acute sunt destul de diferite de cele intilnite la pacientii cu boli
neuromusculare mostenite. Tratamentul este adesea temporar pentru
abordarea evenimentelor acute si nu este necesar pe termen lung.
Tabelul 8.
Frecventa evenimentelor in bolile neuromusculare associate cu afectare
cardiaca
|
Transmitere
|
Bloc
|
AV
|
CM
|
|
Distrofii musculare
|
|
|
|
|
|
Duchenne
|
X-linkat
|
|
|
|
|
Becker
|
X-linkat
|
|
|
|
|
CMD X-linkata
|
X-linkat
|
|
|
|
|
Membru-centura 1B
|
AD
|
|
|
|
|
Membru-centura 2C-2F
|
AR
|
|
|
|
|
DM miotonica
|
AD
|
|
|
|
|
DM Emery-Dreifuss asociata cu alte tulburari
|
X-linkat, AD, AR
|
|
|
|
|
Altele
|
|
|
|
|
|
Ataxia Friedreich
|
AR
|
|
|
|
|
Sindromul Kearns-Sayre
|
|
|
|
|
|
+ la +++ reprezinta o comparatie
intre tipul de afectare si frecventa relativa.
AD, autosomal dominant; AR, autosomal recesiv; CM, cardiomiopatie; DM, distrofie
musculara; AV, aritmii ventriculare; +, frecventa redusa;
++, frecventa intermediara; +++, frecventa mare.
|
10.
Insuficienta cardiaca
Recomandari
Clasa I
ICD
este recomandat pentru preventia secundara a MSC la pacientii
ce au supravietuit FV sau unei TV instabile hemodinamic, sau unei TV cu
sincopa si care au FE a VS mai mica sau egala cu 40%, ce
primesc tratament farmacologic optim si care au o speranta de
viata rezonabila cu un status functional bun mai mult de un
an. (Nivel de dovezi: A)
ICD
este recomandat in preventia primara pentru reducerea
mortalitatii totale prin reducerea MSC la pacientii cu
disfunctie de VS datorata unui IM ce au cel putin 40 de zile
post-infarct, au FE <30-40%, sunt in clasa functionala NYHA II
sau III, primesc tratament farmacologic optim si au o speranta
de viata rezonabila cu un status functional bun mai mult de
1 an. (Nivel de dovezi: A) (vezi
sectiunea 1.2.)
ICD
este recomandat in preventia primara pentru reducerea
mortalitatii totale prin reducerea MSC la pacientii cu boli
cardiace neischemice ce au FE <30-35%, sunt in clasa functionala
NYHA II sau III, ce primesc tratament farmacologic optim, si care au o
speranta de viata rezonabila cu un status functional
bun mai mult de 1 an. (Nivel de dovezi: B)
(vezi sectiunea 1.2.)
Amiodarona,
sotalolul si/sau alte betablocante sunt recomandate ca terapie complementara
la ICD pentru supresia tahicardiilor ventriculare simptomatice
(sustinute sau nesustinute), la pacienti cu tratament optim. (Nivel de dovezi: C)
Amiodarona
este indicata pentru supresia tahicardiilor supraventriculare sau ventriculare
cu compromitere hemodinamica unde cardioversia si/sau corectia
cauzelor nu au reusit sa opreasca aritmia sau sa
previna recurenta precoce. (Nivel
de dovezi: B)
Clasa IIa
ICD
combinat cu cardiostimularea biventriculara poate fi eficient in
preventia primara pentru reducerea mortalitatii totale prin
reducerea MSC la pacientii cu clasa functionala NYHA III
sau IV, ce primesc tratament farmacologic optim, in ritm sinusal cu o durata
a QRS de cel putin 120 ms si care au o speranta de
viata rezonabila cu un status functional bun mai mult de un
an. (Nivel de dovezi: B)
ICD
este rezonabil in preventia primara pentru reducerea
mortalitatii totale prin reducerea MSC la pacientii cu disfunctie
de VS datorata unui IM vechi de cel putin 40 de zile, care au FE
30-35%, sunt in clasa functionala NYHA I, primesc tratament farmacologic
optim si au o speranta de viata rezonabila cu un
status functional bun mai mult de un an. (Nivel de dovezi: B)
ICD
este rezonabil pentru pacientii cu TV recurente stabile, cu FE
normala sau aproape normala, cu tratament optim al IC, care au o
speranta de viata rezonabila cu un bun status
functional mai mult de un an. (Nivel
de dovezi: C)
Cardiostimularea
biventriculara in absenta ICD este rezonabila pentru
preventia MSC la pacientii cu clasa functionala III
sau IV NYHA, FE <35% si durata QRS mai mare sau egala de 160 ms
(sau cel putin 120 ms in prezenta altor date de asincronism ventricular)
ce primesc tratament farmacologic optim si care au o speranta
de viata rezonabila cu un bun status functional mai mult de
un an. (Nivel de dovezi: B)
Clasa IIb
Amiodarona,
sotalolul si/sau betablocantele pot fi considerate ca o alternativa
la ICD pentru oprirea TV simptomatice (sustinute sau nesustinute) la
pacientii cu tratament optim al IC la care implantarea unui defibrilator
nu poate fi realizata. (Nivel
de dovezi: C)
ICD
poate fi considerat pentru preventia primara pentru reducerea
mortalitatii totale prin reducerea MSC la pacientii cu boli
cardiace nonischemice care au FE <30-35%, sunt in clasa
functionala NYHA I, primesc tratament farmacologic optim si au
o speranta de viata rezonabila cu un bun status
functional mai mult de un an. (Nivel
de dovezi: B) (vezi sectiunea 1.2.)
Consideratii
asupra modului de formulare a recomandarilor sunt prezentate in
Introducere.
Aritmiile
ventriculare si moartea subita cardiaca sunt comune la
pacientii cu IC simptomatica acuta sau cronica si la
cei cu disfunctie sistolica de VS. Cauza IC probabil
influenteaza mecanismele si tipurile de aritmii ventriculare.
Recomandarile din aceasta sectiune se refera la
pacientii cu IC simptomatica; nu doar cei cu FEVS alterata (vezi
ACC/AHA Guideline Update for the Diagnosis and Management of Chronic Heart
Failure in the Adult6 pentru definitii).
Tratamentul
aritmilor in cazul IC acute trebuie sa se faca in acelasi timp
cu stabilizarea hemodinamica. Evaluarea aritmiilor in cazul IC acute
necesita evaluarea problemelor mecanice corectabile care produc aritmii
supraventriculare sau ventriculare folosind cateterele pentru monitorizarea
hemodinamica. O atentie deosebita trebuie avuta la factori
ca medicamentele utilizate in tratamentul IC acute, ionograma si
saturatia in oxigen. Avind in vedere debutul relativ rapid al
actiunii si profilul superior de siguranta, amiodarona i.v.
pentru tratamentul aritmiilor amenintatoare de viata la
pacientii cu IC acuta a fost larg acceptata.
La
pacientii cu IC acuta, TSV si fibrilatia atriala sau
flutterul atrial pot produce decompensare hemodinamica si terapia
agresiva poate fi necesara. Tahicardia supraventriculara prost
tolerata poate fi tratata prin cardioversie electrica
utillizand energii joase (50 100 J bifazic). Verapamilul poate fi eficient
pentru supresia tahicardiilor supraventriculare reintrante dependente de
nodul atrioventricular. Trebuie evitata supresia excesiva a
contractilitatii miocardice prin efectul inotrop negativ al
verapamilului. Amiodarona iv poate fi mai eficienta pentru controlul
frecventei ventricular in fibrilatia atriala sau flutter atrial
si poate restabili ritmul sinusal. La pacientii cu IC, amiodarona
singura sau impreuna cu cardioversia electrica este
eficienta pentru scaderea frecventei si realizarea
cardioversiei.763,764
In
cazurile de IC acuta, aritmiile ventriculare pot fi prost tolerate si
cardioversia precoce trebuie realizata, mai degraba decat sa
incercam cardioversia farmacologica. Pacientii cu boli
miocardice avansate adesea au tulburari de conducere intraventriculare
care fac dificil diagnosticul diferential al tahicardiile
supraventriculare si ventriculare. Indiferent de origine aritmiile cu
instabilitate hemodinamica necesita cardioversie. Amiodarona este
preferata pentru administrarea pe termen lung si este in general bine
tolerata hemodinamic.765 Ablatia poate fi potrivita
la anumiti pacienti.
TVNS
asimptomatica poate fi documentata prin utilizarea
monitorizarii Holter la 30-80% din pacientii cu IC cronica.25,766,767
Desi TV nesustinuta este asociata cu cresterea
riscului de deces, nu exista o legatura specifica intre
TVNS si MSC,25,766,768 desi un trial a sugerat
aceasta legatura.767 Nu exista dovezi ca
supresia TV nesustinute are un efect favorabil pe prognosticul pacientilor
cu IC.638 Deci, TVNS asimptomatice nu trebuie tratate cu
medicatie antiaritmica. Daca TVNS este simptomatica si
necesita terapie, amiodarona este probabil cel mai sigur medicament,
desi amiodarona la pacientii cu clasa functionala III
NYHA in trialul SCD-HeFT a fost asociata cu cresterea
mortalitatii.8,248
TV
polimorfa asociata sau nu cu prelungirea QT poate fi intalnita
in timpul exacerbarilor IC. Aceste aritmii pot fi intrerupte prin
tratamentul IC.
Moartea
subita cardiaca reprezinta aproximativ 50% din decesele la
pacientii cu IC. Totusi, exista putine date ca tratamentul
antiaritmic empiric poate reduce riscul de moarte subita. Trialurile mai
vechi in care s-a utilizat tratamentul empiric cu amiodarona au furnizat
date contradictorii, unele demonstrand reducerea mortalitatii altele
nesustinand imbunatatirea supravietuirii.637,638
Trialul SCD-HeFT nu a demonstrat ameliorarea supravietuirii la
pacientii cu IC (clasa functionala II si III NYHA) si
FEVS mai mica sau egala cu 35% tratati empiric cu amiodarona.8
ICD nu a
crescut supravietuirea la pacientii cu IC datorata bolilor
cardiace nonischemice in 2 trialuri mici.635,645 Totusi,
trialul SCD-HeFT a demonstrat o reducere cu 23% a mortalitatii
totale prin utilizarea ICD in comparatie cu placebo.8 Aceste
rezultate sunt concordante cu rezultatele DEFINITE si trialurilor mai
vechi la pacientii cu boala coronariana si disfunctie
de VS, unii dintre ei avand IC simptomatica.192,267,268 ICD in
combinatie cu cardiostimularea biventriculara poate imbunatati
supravietuirea si simptomele pacientilor cu IC avansata
(clasa functionala NYHA III si IV) pe termen scurt (1-2 ani).
Pacingul
biventricular poate fi folosit pentru sincronizarea contractiei VS la
pacientii cu activare ventriculara anormala. Terapia de resincronizare
cardiaca a imbunatatit hemodinamica, a crescut FEVS, a
crescut toleranta la efort si a imbunatatit calitatea
vietii.769,770 La pacientii cu status functional
prost ( clasa NYHA III sau IV), cu fractie de ejectie redusa
(FEVS mai mica sau egala cu 35%) si complex QRS larg (cel
putin 120 ms) pacingul biventricular fara ICD a condus
sistematic la reducerea mortalitatii si a spitalizarilor
pentru tratamentul IC.771,772 Prin urmare a fost puternic
recomandat6 ca pacingul biventricular sa fie luat in
considerare la acesti pacienti. Acets ghid se refera la
managementul aritmiilor ventriculare si al MSC. Intr-un studiu recent772
care a recrutat pacienti cu IC de clasa NYHA III-IV, cu FE mai
mica sau egala cu 35%, durata QRS mai mare sau egala cu 160 ms
(sau cel pautin 120 ms in prezenta altor dovezi de
dissincronism ventricular), moartea subita a fost semnificativ
redusa prin pacing biventricular. Cu toate acestea, in alt studiu771
care a recrutat pacienti asemanatori, doar ca durata
QRS a trebuit sa fie mai mare sau egala de 120 ms, moartea
subita nu a fost prevenita numai prin resincronizare. Valoarea
pacingului biventricular fara ICD aditional pentru reducerea
mortii subite ramane controversata.773,774
11. Sindroame
aritmice genetice
11.1. Concepte generale
pentru
stratificarea riscului
LQTS,
sindromul Brugada si tahicardia polimorfa catecolaminergica (Online
Mendelian Inheritance in Man [OMIM] Nr. 192500, 152427, 603830, 600919,
176261, 603796, 601144 si 604772)775 sunt boli aritmogene mostenite.
Ele predispun la TV si MSC in absenta anomaliilor structurale ale
inimii. Aceste sindroame sunt prin definitie boli rare deoarece ele au o
prevalenta estimata de 5 la 10000 (definitia 1295/1999/EC
a Parlamentului European770).
Datorita
numarului mic de indivizi afectati de aceste boli, trebuie luate in
considerare cateva aspecte inainte de a propune recomandari de management
si stratificare a riscului.
Cele
mai multe date disponibile deriva din registre care au urmarit
pacientii in timp, inregistrand rezultatele. Nu sunt disponibile studii randomizate si cel mai probabil ele nu vor
putea fi realizate. Prin urmare, nivelul de dovezi pentru recomandari in
aceste conditii este B sau C depinzand de marimea registrelor
disponibile si de durata urmaririi pacientilor. (Acest comitet
a decis sa considere nivelul de dovezi B pentru datele din registrele de
LQTS, care contin un numar mare de pacienti urmariti
perioade lungi si nivelul de dovezi C pentru sindromul Brugada si
CPVT care perioadede follow-up mai mai scurte).
Datele despre istoria naturala sunt potential
alterate prin includerea mai probabila a pacientilor inalt
simptomatici in registre. Acest bias este
probabil mai pronuntat in registrele recente (CAVD, sindrom Brugada, CPVT)
decat in cele care au strans informatii timp de decenii (LQTS).
Unele concepte aplicate pentru stratificarea riscului
sunt comune diferitelor boli aritmogene mostenite. De exemplu severitatea fenotipului ECG este un marker general al
cresterii riscului de MSC in majoritatea bolilor. In LQTS, fenotipul
sever a fost reprezentat de prezenta intervalului QTc peste 500 ms,103,776
in sindromul Brugada prin prezenta spontana a supradenivelarii ST
in derivaltiile precordiale drepte104,777 si in CPVT prin
TV induse prin test de efort.105,778
Deoarece aceste boli sunt caracterizate prin anomalii
electrice aparute pe cord cu structura normala utilizarea ICD a
fost recomandata cu indicatie de clasa I in preventia
secundara a stopului cardiac. Utilizarea ICD in preventia
primara este controversata, tinand cont de varsta
tanara in momentul diagnosticarii. In LQTS si in CPVT
terapia farmacologica cu betablocante este eficienta in reducerea
riscului de evenimente cardiace. In aceste boli betablocantele au fost recomandate
ca prima linie de tratament la toti pacientii afectati,
clasa I de indicatie si utilizarea ICD a fost recomandata
pentru subgrupul cu risc mai inalt.104,105,777,779 In sindromul
Brugada nu este cunoscut un tratament farmacologic eficient si de aceea
utilizarea profilactica a ICD trebuie folosita tintit la
pacientii cu risc mare.104,777
Testele genetice intra progresiv in practica clinica
si se integreaza in schemele de stratificare a riscului.103,780
In general istoricul familial de MSC nu si-a dovedit
utilitatea in stratificarea riscului la pacientii afectati.
Evitarea sporturilor competitive este recomandata
de unii, la toti pacientii cu boli aritmogene mostenite, chiar
cand efortul fizic nu este considerat un trigger al aritmiilor, ca la
pacientii cu sindrom Brugada sau LQTS3 (vezi sectiunea 13.1).
O
privire generala asupra manifestarilor clinice, recomandarilor
de stratificare a riscului si management este eprezentata in
sectiunile urmatoare.
11.1.1. Sindromul de QT lung
Recomandari
Clasa I
Modificarea stilului de
viata este recomandata pentru pacientii cu diagnosticul de
LQTS (clinic si/sau molecular). (Nivel
de dovezi: B)
Betablocantele
sunt recomandate pentru pacientii cu diagnostic clinic de LQTS (ex, in
prezenta unui interval QT lung). (Nivel
de dovezi: B)
Implantarea
unui defibrilator impreuna cu betablocantele este recomandata pentru
pacientii cu LQTS care au stop cardiac in antecedente si au o
speranta de viata rezonabila cu un status functional
bun mai mult de un an. (Nivel de dovezi:
A)
Clasa IIa
Betablocantele
pot fi eficiente pentru reducerea MSC la pacientii cu diagnostic
molecular de LQTS si interval QT normal. (Nivel de dovezi: B)
Implantarea
unui defibrilator cu continuarea tratamentului cu betablocante poate fi eficienta
pentru reducerea MSC la pacientii cu LQTS care prezinta sincope
si/sau TV in timp ce primeau betablocante si care au o speranta
de viata rezonabila cu un status functional bun mai mult de 1
an. (Nivel
de dovezi: B)
Clasa IIb
Denervarea
simpatica stanga poate fi considerata pentru pacientii cu
LQTS si sincope, torsada de varfuri sau stop cardiac in timp ce
primeau tratament cu betablocante. (Nivel
de dovezi: B)
Implantarea
unui defibrilator impreuna cu utilizarea betablocantelor poate fi considerata
pentru profilaxia MSC la pacientii cu un risc mai mare de stop cardiac
(LQT2 si LQT3) si care au o speranta de viata
rezonabila cu un status functional bun mai mult de 1 an. (Nivel de dovezi: B)
11.1.1.1. Cauze si
factori de risc.
LQTS
este o boala mostenita caracterizata prin prelungirea
repolarizarii ventriculare (intervalul QT) si prin tahiaritmii
ventriculare care se pot manifesta prin evenimente sincopale. Aritmiile sunt
adesea declansate de stress si emotii, desi in unele cazuri
ele pot surveni in repaus sau in timpul somnului.781 Doua
tipuri de transmitere au fost identificate: cea mai comuna autozomal dominanta
in cazul sindromului Romano-Ward si Timothy782,783 si una
mult mai rara autozomal recesiva. Ultima este in mod obisnuit
mai severa, implicand adesea dar nu intotdeauna casatorii
consangvine, si sunt adesea asociate cu surditate congenitala
(sindromul Jervell Lange-Nielsen784). Au fost identificate
mutatii in 8 gene: 7 din ele codifica subunitat ale
canalelor ionice si 1 codifica o proteina de ancorare care a
fost implicata in controlul canalelor ionice cu localizare membranara
specifica.791 Trasaturile caracteristice ale unor
variante genetice de boala au fost identificate si incluse in algoritmul
de stratificare a riscului.
11.1.1.2. Stratificarea
riscului
Chiar
inaintea identificarii subtipurilor genetice, durata intervalului QT a
fost identificata ca cel mai puternic factor predictiv de risc pentru
evenimente cardiace (sincopa, moartea subita) in LQTS,776 si
inca a ramas. Un interval QT normal la un membru al unei familii
negenotipate are un prognostic bun.792 Un QTc peste 500 ms
identifica (corespunzator cuartilei superioare la pacientii
afectati genotipati) identifica pacientii cu cel mai mare
risc de a deveni simptomatici pana la varsta de 40 ani.103
Pacientii cu sindrom Jervell LangeNielsen si alte sindroame
homozigote si pacientii cu LQTS asociat cu sindactilie790,793
au un risc mai mare. Un istoric familial de MSC nu a fost dovedit a fi un
factor de risc pentru moartea subita cardiaca.779,794
Testele
genetice sunt adesea utile la pacientii suspecti cu un diagnostic
clinic de LQTS pentru a realiza o stratificare mai exacta a riscului si a
ghida tratamentul.
Simptomele
LQTS variaza de la MSC la sincopa sau presincopa. Pacientii
resuscitati dupa un episod de MSC au in mod special prognostic
nefavorabil, cu un risc relativ de 12,9 de a repeta stopul cardiac.779
Pacientii afectati pot fi identificati datorita
descoperirii intamplatoare a prelungirii intervalului QT sau
datorita faptului ca sunt rude ale pacientilor afectati si
sunt descoperiti purtatori ai mutatiei prin efectuarea unui
screening genetic; prognosticul la acestia tinde sa fie mai bun
decat la cei cu suspiciune clinica. Riscul creste in perioada imediat
postpartum.795
S-a
dovedit ca relatia intre defectul genetic, durata QT si sex
poate furniza un algoritm pentru stratificarea riscului.103
Pacientii cu cel mai mare risc de a deveni simptomatici sunt cei cu LQT1
si LQT2 cu un QTc mai mare de 500ms si barbatii cu LQT3
indiferent de durata QT.103 Pacientii cu LQT3 pot reprezenta un
grup cu risc mai inalt.780 Printre pacientii cu LQT2, cei cu o
mutatie determinind o modificare in regiunea porului proteinei,796
par sa aiba un risc mai mare de evenimente decat cei cu mutatii
in alte regiuni ale genei. Betablocantele sunt foarte eficiente in LQT1, in
timp ce ele ofera protectie incompleta in LQT2 si LQT3.797
Aritmiile ventriculare
Sincopa
la pacieniti cu LQTS este obisnuit atribuita aritmiilor
ventriculare severe (desi alte cauze pot fi intalnite). Sincopele sunt
obisnuit asociate cu stresul, emotiile sau efortul; totusi
triggeri genic-specifici pentru evenimentele cardiace au fost identificati
in cazul celor 3 variante genetice mai comune de boala. Pacientii cu
tipul LQT1 de boala (mutatii in KCNQ1 sau KvLQT1 ale genei ce
codifica canalele ionice ale curentului Iks), sunt mai
susceptibili la evenimente cardiace in timpul efortului798 si
in special in timpul inotului.799,800 Pacientii cu LQT2 ce
prezinta mutatii in KCNH2 (sau HERG), gena ce codifica
canalele Ikr, sunt susceptibili la evenimente in repaus sau la
emotii, si caracteristic la stimuli acustici.800,801 Tipul
LQT3 ce prezinta mutatii in gena SCN5A ce codifica canalele de
Na di cord sunt susceptibili la evenimente cardiace in repaus si in
timpul somnului.798 O descriere a subtipurilor de LQT este
realizata in Tabelul 9.
Tabelul 9.
Subtipuri de sindroame de QT lung
|
Varianta
|
Gena
|
Cromozom
|
Functie
|
|
LQT1
|
KCNQ1
|
11p15.5
|
IKs subunitatea alfa
|
|
LQT2
|
KCNH2
|
7q35-35
|
IKr subunitatea alfa
|
|
LQT3
|
SCN5A
|
3p21-23
|
INa subunitatea alfa
|
|
LQT4
|
ANK2
|
4q25-2
|
Targeting protein
|
|
LQT5
|
KCNE1
|
21p22.1-22-2
|
IKs subunitatea beta
|
|
LQT6
|
KCNE2
|
21p22.1-22-2
|
IKr subunitatea beta
|
|
LQT7
|
KCNJ2
|
17p23.1-24.2
|
IK1
|
|
LQT8
|
CACNA1C
|
12p13.3
|
ICa subunitatea alfa
|
|
JLN1
|
KCNQ1
|
11p15.5
|
IKs subunitatea alfa
|
|
JLN2
|
KCNE1
|
21p22.1-22-2
|
IKr subunitatea beta
|
Varsta
medie la care apar primele manifestari ale bolii este de 12 ani, dar exista
o categorie considerabila de pacienti la care s-au raportat
manifestari atat in primul an de viata, cat si in decadele
5-6. Evidentierea aritmiilor in timpul evenimentelor cardiace nu este
frecventa in sindromul QT lung: atunci cand se inregistreaza
aritmii, acestea sunt tahicardia ventriculara polimorfa, torsada
varfurilor;781,802 moartea cardiaca subita poate fi prima
manifestare a bolii.
11.1.1.4 Schimbarea stilului de viata
Se
recomanda ca toti pacientii afectati de LQTS sa evite
sportul de performanta.682 Pentru cei diagnosticati
cu varianta LTQ1 practicarea inotului trebuie sa fie in mod specific
limitata sau executata sub supraveghere. Pentru cei
diagnosticati cu varianta LTQ2 este interzisa expunerea la stimuli
acustici pe perioada somnului (ex, telefonul sau alarma ceasului in timpul
noptii). Tuturor pacientilor diagnosticati cu LTQS le este
interzis consumul de medicamente care prelungesc intervalul QT si
consumul de medicamente care duc la depletia K si Mg.
11.1.1.5. Sindromul Andersen
In 1971
Andersen si colab.803 au raportat cazul unui copil in varsta de
8 ani, de statura mica, cu hipertelorism, radacina nasului
largita si defect al palatului dur si moale. Definitia lui
Andersen a fost utilizata prima data in 1994 de Tawil si colab.804
pentru a descrie o tulburare clinica caracterizata prin asocierea a
trei conditii majore: paralizia periodica sensibila la potasiu,
aritmii ventriculare si dismorfia fetei (similara celei descrise
de Andersen in 1971). Prezenta unui grad variabil al alungirii
intervalului QT a fost subliniata inca din prima descriere
sistematica a bolii. Ulterior, Sansone si colab.805 au
confirmat importanta diagnostica a acestei alungiri a intervalului
QT. In afara de QT lung, pacientii cu sindrom Andersen pot avea
anomalii ale repolarizarii constand dintr-o componenta a
repolarizarii tardive asemanatoare unei unde U largite. TV
bidirectionala a fost de asemenea mentionata ca pattern
distinctiv al sindromului Andersen. Sindromul Andersen mai este cunoscut
si ca LTQ7, desi este discutabil faptul ca ar putea fi parte a
spectrului LTQS.806 In ciuda faptului ca a fost raportata
MSC,807 aritmia nu pare a fi o cauza majora de deces in
sindromul Andersen, boala avand adesea un prognostic benign.805,808
Substratul
genetic al sindromului Andersen a fost recent elucidat prin studiul larg al
genomului de catre Plaster si colab.;804 intr-o familie
numeroasa afectata de sindromul Andersen, ei au demonstrat cu succes
legitura intre prezenta afectiunii respective si locusul 17q23. A
fost cautata candidata in regiunea critica si o
mutatie mis-sense a fost identificata pe gena KCJN2. Mutatii
suplimentare au fost identificate ulterior la 8 persoane neinrudite, ceea ce
reprezinta o dovada in plus ca KCJN2 este cauza macar a
catorva persoane afectate de sindromul Andersen. KCJN2 codifica un canal
rectificator inward al K, Kir2.1, cu larga raspandire la nivelul
cordului, unde pare sa contribuie determinant la faza a 4-a a
repolarizarii si la potentialul de repaus. Mutatii la
nivelul genei KCJN2 se intalnesc la aproximativ 40% din cei afectati de
sindromul Andersen.
Se
cunosc putine lucruri despre stratificarea riscului si managementul
pacientilor cu sindrom Andersen. Pacientii par sa aiba aritmii
ventriculare, dar nu s-a raportat incidenta crescuta a stopului
cardiac. Desi cei mai multi dintre acesti pacienti cu QT
lung sunt tratati in mod empiric cu betablocante, rolul profilactic al
acestora nu a fost demonstrat. Rolul benefic al blocantelor canalelor de Ca se
bazeaza de asemenea pe observarea supresiei aritmiei la un singur pacient.809
11.1.1.6. Analiza genetica
Analiza
genetica este foarte importanta pentru identificarea tuturor
purtatorilor de mutatii intr-o familie afectata de LQTS.
Odata identificati, purtatorii asimptomatici ai defectelor
genetice responsabile de LQTS pot fi tratati cu beta-blocante pentru
profilaxia aritmiilor ce pun in pericol viata. Mai mult, purtatorii
asimptomatici ar trebui sa primeasca sfaturi genetice in ceea ce priveste
riscul transmiterii LTQS la urmasi.
La
pacientii afectati de LTQS analiza genetica este folosita
pentru stratificarea riscului103 si pentru luarea unor decizii
terapeutice.810 Chiar daca analiza genetica e greu
disponibila, este de dorit ca ea sa fie accesibila tuturor
pacientilor cu LTQS.
11.1.2. Sindromul de QT
scurt
Primul
raport al acestei conditii clinice caracterizata prin scurtarea
anormala a repolarizarii, a fost facut de Gussak si colab
in 2000.140 Acesti autori au descris la o mama si 2
fii, in absenta unei boli cardiace structurale, un interval QT scurt
persitent (260-275 msec) cu unde T inguste si ascutite. Astfel, ei au
propus ca un interval QT mai mic de 300 msec sa fie diagnostic pentru
SQTS. In 2003 Gaita si colab.811 au raportat
existenta a 2 familii cu SQTS si au aratat ca cei
afectati aveau un interval QTc mai mic de 300 ms, cu un interval QT mai
mic de 280 ms. La scurt timp dupa aceea, o noua forma a SQTS a
fost identificata la pacientii cu un interval QTc de pana la 320
ms.812 In prezent nu se stie clar daca diagnosticul SQTS
ar trebui sa se bazeze pe valorile intervalului QT sau QTc si nici
care este sensibilitatea si specificitatea valorilor QT/QTc.
Anomaliile
morfologice ale undei T acompaniaza scurtarea repolarizarii in SQTS.
Multi pacienti au unde T inalte si ascutite sau unde T
asimetrice cu o panta ascendenta normala si o panta
descendenta foarte rapida. Parametrii clinici de diagnostic sunt
inca necunoscuti, deci analiza genetica pare sa fie
folositoare in confirmarea diagnosticului la pacientii suspecti de
SQTS.
Pana
acum doar 23 de cazuri de SQTS din 6 familii diferite au fost raportate813
si experienta actuala sugereaza ca boala are
mortalitate ridicata. Trebuie avut in vedere faptul ca atunci cand
o cohorta limitata de pacienti este disponibila, severitatea
bolii tinde sa fie supraestimata, pentru ca pacientii
simptomatici sunt identificati datorita aritmiilor
amenintatoare de viata, in timp ce pacientii
asimptomatici raman nediagnosticati. Nu exista nici un fel de
informatie asupra faptului ca ar exista un anumit factor
declansator al evenimentelor cardiace,
iar MSC poate aparea atat in conditii de repaus cat si in
conditii de stres. SQTS ar putea fi cauzat de mutatii dispuse la
nivelul a trei gene ce codifica anumite canale ionice de la nivelul
miocardului.
Prima
gena identificata in SQTS este KCNH2814 care ar
contine mutatia responsabila de o remarcabila crestere
a curentului Ikr. Bellocq si colab.815 au raportat o
alta mutatie dispusa la nivelul genei KCNQ1 la un barbat de
70 ani prezentand FV idiopatica si interval QT scurt pe ECG.
Dupa Priori si colab.816 a treia gena
identificata ca si cauza a repolarizarii scurte anormale,
este KCNJ2, caracteristica fiind morfologia specifica a undei T
(partea terminala extrem de scurta, iar segmentul ST si faza
ascendenta a undei T cvasinormale).
Este
interesant de notat faptul ca toate cele trei gene implicate in SQTS
(KCNH2, KCNQ1, KCNJ2) pot produce deasemenea LQTS. Fenotipurile ECG depind de
consecintele mutatiilor de baza, mutatiile cu pierdere de
functie fiind asociate cu STQS, iar cele cu castig de functie
fiind asociate cu LQTS.
Studiile
electrofiziologice au aratat ca perioada refractara efectiva,
atat atriala cat si cea ventriculara, este scurta in SQTS,
iar stimularea electrica programata de obicei induce tahiaritmii
ventriculare. Ramane neclar daca inductibilitatea aritmiilor
ventriculare este predictor de evenimente cardiace fatale (Tabel 10).
Tabelul 10.
Variante genetice ale sindromului QT scurt
|
Locus
|
Cromozom
|
Transmitere
|
Gena
|
Proteina
|
Autori
|
|
SQTS1
|
7q3p2135-q36
|
Autozomal dominanat
|
KCNH2
|
Canalul de K Ikr
subunitatea α (HERG)
|
Brugada si colab.813
|
|
SQTS2
|
11p15.5
|
Autozomal dominanat
|
KCNQ1
|
Canalul de K Iks
subunitatea α (KvLQT1)
|
Belloq si colab.814
|
|
SQTS3
|
17q23.1-q24.2
|
Autozomal dominanat
|
KCNJ2
|
Canalul de K Ik1 (Kir2.1)
|
Priori si colab.815
|
Managementul
pacientilor cu SQTS nu este inca bine definit.817 La
pacientii care prezinta mutatii la nivelul genei KCNH2 este
sugerat faptul ca utilizarea chinidinei ar putea scadea inductibilitatea
aritmiilor prin stimulare electrica programata; nu se stie
insa daca ea confera preventie pe termen lung in ceea ce
priveste aparitia stopului cardiac. Pentru celelalte forme genetice
ale SQTS eficacitatea chinidinei este mai putin inteleasa; utilizarea
ICD poate fi considerata chiar daca exista riscul
cresterii numarului de socuri inadecvate (prin oversensing al
undei T).817
11.1.2.1
Analiza genetica
Analiza
genetica este utila in identificarea purtatorilor
asimptomatici ai mutatiilor responsabile de SQTS; riscul de evenimente
cardiace la indivizii afectati, dar cu aspect ECG normal, este necunoscut.
Datorita numarului mic de indivizi depistati cu SQTS, analiza
genetica nu poate contribui la stratificarea riscului.
11.1.3. Sindromul Brugada
Recomandari
Clasa I
Implantarea
defibrilatorului cardiac este recomandata la pacientii cu sindrom
Brugada cu stop cardiac resuscitat in antecedente, care primesc terapie
medicamentoasa optima si la care se asteapta
supravietuire la un standard bun pentru o perioada mai mare de 1 an. (nivel de dovezi C)
Clasa IIa
ICD
este recomandat la pacientii cu sindrom Brudaga cu supradenivelare
spontana de segment ST in V1, V2 sau V3, care au avut o sincopa, cu
sau fara mutatii demonstrate la nivelul genei SCN5A si la
care speranta de viata este rezonabila cu un status
functional bun pentru o perioada mai mare de 1 an. (nivel de dovezi C)
Urmarirea
clinica pentru eventuala dezvoltare spontana a supradenivelarii de
segment ST este recomandata la pacientii cu supradenivelare de
segment ST indusa doar prin metode farmacologice, cu sau fara
simptome. (nivel de dovezi C)
ICD
este recomandat la pacientii cu sindrom Brugada cu TV documentata,
care nu a fost urmata de stop cardiac si la care se
asteapta o supravietuire rezonabila la un status
functional bun pe o perioada mai mare de 1 an. (nivel de dovezi C)
Isoproterenolul
poate fi folosit pentru tratarea furtunii electrice din sindromul Brugada. (nivel de dovezi C)
Clasa IIb
Studiul
electrofiziologic poate fi recomandat pentru stratificarea riscului la
pacientii cu sindrom Brugada asimptomatici, cu supradenivelare
spontana de segment ST, cu/fara mutatii la nivelul genei
SCN5A. (nivel de
dovezi C)
Chinidina
poate fi rezonabil folosita pentru tratamentul furtunii electrice la
pacientii cu sindrom Brugada. (nivel
de dovezi C)
11.1.3.1 Cauze si
factori de risc
Sindromul
Brugada se asociaza cu aspect anormal caracteristic al ECG si cu un
risc inalt de MCS, la indivizi structura cardiaca normala.818
Aspectul ECG in sindromul Brugada implica supradenivelarea punctului
J in derivatiile V1-V3 si BRD la unii pacienti; acest aspect ECG
poate fi prezent permanent sau intermitent. Ocazional, supradenivelarea
punctului J a fost raportata si in alte derivatii (ex,
derivatiile inferioare). Boala este transmisa autozomal dominant.
Expresia clinica a acestei afectiuni variaza in functie de
sex, astfel incat 90% din pacientii cu aspect ECG diagnostic pentru
sindromul Brugada sunt barbati. Doar o singura gena responsabila
de sindromul Brugada a fost identificata pana acum, gena ce
codifica canalul de Na (SCN5A);819 alte locusuri non SCN5A au
fost deasemenea raportate, dar genele responsabile de aceasta boala
raman inca de identificat. Evenimentele cardiace (sincopa sau stopul
cardiac) predomina la barbatii de 30-40 ani, desi stopul
cardiac a fost raportat si la nou-nascut sau copil.104,777,820
Febra este factor predispozant pentru stopul cardiac in cadrul sindromului
Brugada.800,818,821-824
11.1.3.2 Stratificarea riscului
Deoarece
implantarea ICD este singura masura profilactica capabila
sa previna MSC, stratificarea riscului la acesti pacienti
are mare importanta.
11.1.3.3. Antecedente
heredocolaterale
Ca
si in cazul LQTS, nu exista date suficiente care sa arate daca
istoricul familial poate prezice eventualele evenimentele cardiace printre
membrii unei familii. Mai mult, nu ar trebui sa presupunem ca
indivizii asimptomatici cu aspect ECG caracteristic dar care nu au antecedente
heredocolaterale ar putea avea risc scazut de MSC, sau ca membrii
unei familii in care a existat un caz de MSC ar putea avea risc mai mare.104
11.1.3.4
Date electrocardiografice
Supradenivelarea
de segment ST poate exista spontan sau poate fi indusa de administrare de
blocante ale canalelor de Na (flecainida, procainamida sau ajmalina).825
Exista un consens, cum ca pacientii cu supradenivelare
spontana de segment ST au un prognostic mai prost decat cei la care
aspectul ECG tipic se observa doar dupa administrarea medicamentelor
mai sus mentionate.104,777
11.1.3.5. Simptome
Pacientii
cu istoric de sincopa si aspect ECG specific sindromului Brugada
(supradenivelare spontana de segment ST) au un risc de stop cardiac de 6
ori mai mare decat pacientii fara sincopa si cu aspect
ECG specific.104
11.1.3.6. Studiul
electrofiziologic
Rolul
studiului electrofiziologic in stratificarea riscului este inca
dezbatut. Brugada si colab.206,207 sugereaza ca
studiul electrofiziologic are un rol important in stratificarea riscului: in
cadrul analizei facuta de acestia, studiul electrofiziologic a
avut o valoare predictiva pozitiva scazuta (23%), dar la
urmarirea pe o perioada mai mare de 3 ani a avut valoare
predictiva negativa inalta (93%). In opozitie, Priori
si colab.104,208 au raportat faptul ca studiul
electrofiziologic a avut acuratete scazuta in prezicerea
stopului cardiac. Ei au propus ca alternativa pentru stratificarea
riscului acestor pacienti, metode non-invazive (ECG si
simptomatologia)
11.1.3.7. Defectul genetic
Deoarece
o singura gena a fost asociata cu sindromul Brugada, nu
exista inca suficienta informatie despre contributia
defectelor genetice la prezicerea prognosticului. Mutatiile la nivelul
genei SCN5A nu identifica subsetul de pacienti aflati la risc
inalt pentru evenimente cardiace.104
11.1.3.8. Aritmile
ventriculare
MSC e
cauzata de TV polimorfa sau FV, frecvent aparute in timpul
repausului sau chiar in timpul somnului. Pacientii cu sindrom Brugada de
obicei nu au extrasistole ventriculare sau episoade de TVNS la inregistrarile
Holter. In consecinta, tinta terapeutica pentru acesti
pacienti este preventia stopului cardiac. Studiile
stiintifice de baza si studiile clinice au sugerat rolul
blocarii curentului de potasiu outward tranzitor de catre chinidina,
cu rol in scaderea frecventei aritmiilor.827,828 Chinidina
si isoproterenolul pot fi utile la pacientii cu furtuna
aritmica chiar si in prezenta ICD.139,395,829
11.1.3.9. Analiza
genetica
Analiza
genetica poate fi utila pentru identificarea purtatorilor
asimptomatici ai mutatiilor legate de sindromul Brugada, astfel incat ei
sa ramana sub supraveghere clinica pentru depistarea
manifestarilor clinice tardive ale sindromului. Odata
identificati, purtatorii asimptomatici trebuie sa
primeasca sfaturi genetice in ceea ce priveste riscul transmiterii
bolii la urmasi. Bazata numai pe datele actuale, analiza
genetica nu contribuie la stratificarea riscului.
11.1.4 Tahicardia
ventriculara polimorfa catecolaminergica
Recomandari
Clasa I
Betablocantele
sunt indicate la pacientii diagnosticati clinic cu CPVT pe baza
prezentei aritmiilor ventriculare spontane sau induse la testul de efort. (nivel de dovezi C)
Implantarea
ICD impreuna cu betablocantele se utilizeaza la pacientii cu
CPVT cu stop cardiac resuscitat in antecedente, la care se asteapta
supravietuire rezonabila la un status functional bun pentru o
perioada mai mare de 1 an. (nivel de
dovezi C)
Clasa IIa
Beta-blocantele pot fi
eficiente la pacientii fara manifestari clinice, la care
diagnosticul de CPVT a fost stabilit in copilarie pe baza analizei
genetice. (nivel de dovezi C)
Implantarea
ICD si utilizarea de betablocante poate fi eficienta la
pacientii diagnosticati cu CPVT, cu sincopa si/sau TV
sustinuta documentata in timpul tratamentului cu betablocante
si la care se asteapta supravietuire rezonabila cu
status functional bun pe o perioada mai mare de 1 an. (nivel de dovezi C)
Clasa IIb
Beta-blocantele
sunt de considerat la pacientii cu CPVT care au fost diagnosticati
prin analiza genetica la maturitate si care nu au avut niciodata
manifestari clinice ale tahiartimiilor. (nivel de dovezi C)
11.1.4.1. Cauze si
factori de risc
CPVT
reprezinta tahiaritmii ventriculare aparute in timpul
activitatii fizice sau emotiilor acute, in prezenta unui
aspect ECG de repaus necaracteristic.778 Primul episod apare adesea
in perioada copilariei, desi au fost descrise si cazuri in care
primele manifestari au aparut mai tarziu in cursul vietii.830
Boala
poate fi transmisa autozomal dominant, dar si autozomal recesiv.
Jumatate din cazurile transmise autosomal dominant sunt cauzate de
mutatii la nivelul genei ce codifica receptorul cardiac al ryanodinei
(RyR2), responsabila de eliberarea Ca din depozitele reticulului
sarcoplasmatic.831,832 Forma recesiva este cauzata de
mutatii la nivelul genei care codifica calsequestrina (CASQ2),
proteina ce leaga Ca la nivelul reticulului sarcoplasmatic.833
11.1.4.2. Stratificarea
riscului
Au fost
raportati prea putini pacienti cu CPVT pentru a putea defini
clar stratificarea a riscului. Betablocantele par a fi eficiente.
Pacientii care au avut un episod de FV sunt considerati a avea risc
inalt si alaturi de terapia cu betablocante, acestora le este
recomandata implantarea defribrilatorului cardiac. Daca in timpul terapiei
cu betablocante apar TV sustinuta recurenta sau TV cu
deteriorare hemodinamica, acestea sunt considerate markeri de risc inalt
si pentru pacientii respectivi se recomanda ICD. Studiul
electrofiziologic nu este folosit pentru managementul si stratificarea
riscului la pacienti cu CPVT pentru ca de obicei aceasta aritmie nu este
inductibila.105,778
11.1.4.3 Aritmiile
ventriculare
Aritmiile
supraventriculare si ventriculare sunt frecvent induse la testul de
efort, cand frecventa cardiaca depaseste pragul de
120-130 bpm. Prima data apar de obicei BPV izolate si sunt urmate de
pase scurte de TVNS. Daca pacientul continua efortul, durata TV
creste progresiv si se poate transforma in TV sustinuta.
Aspectul tipic al CPVT este tahicardia bidirectionala, cu alternanta
axului QRS de la un complex la altul. Pacientii cu CPVT pot prezenta
si TV polimorfa neregulata sau fibrilatie
ventriculara.105,778
Betablocantele
pot preveni recurenta sincopei la majoritatea pacientilor,105,778
chiar daca TV si TSV pot fi provocate in timpul tesului de efort.
Daca apare sincopa la pacientii care primesc betablocante, atunci se
recomanda implantarea de ICD.105 Oricum, implantarea de ICD
necesita programari minutioase ale dispozitivului, astfel incat
sa fie prevenite terapiile medicamentoase inutile pentru episoadele de
TVNS.
11.1.4.4. Analiza
genetica
Analiza
genetica poate sa permita identificarea purtatorilor
asimptomatici ai mutatiilor responsabile de TV catecolaminergica.
Odata identificati, acesti purtatori pot fi tratati cu
beta-blocante pentru scaderea riscului de evenimente cardiace si pot
primi sfaturi genetice in ceea ce priveste riscul transmiterii bolii la
urmasi. Bazata pe datele actuale, analiza genetica nu contribuie
la stratificarea riscului.
12. Aritmiile
la cei cu cord
structural normal
12.1 Tahicardia
ventriculara idiopatica
Recomandari
Clasa I
Se
recomanda ablatia la pacientii cu structura cardiaca
normala care prezinta TV simptomatice, refractare la tratament, cu
punct de plecare din VS sau VD, sau la pacientii cu intoleranta medicamentoasa,
sau la cei care nu prezinta complianta pentru terapia
medicamanetoasa pe termen lung. (nivel
de dovezi C)
Clasa IIa
Studiul
electrofiziologic se recomanda pentru evaluarea diagnostica la
pacientii cu structura normala a cordului si cu istoric de
palpitatii sau suspectati de tahicardie ventriculara cu
originea in tractul de ejectie al ventriculului. (nivel de dovezi B)
Terapia
medicamentoasa cu betablocante si/sau blocante ale canalelor de Ca
(si/sau agenti antiaritmici din clasa IC in TV din tractul de
ejectie al VD) poate fi utilizata la pacientii cu TV
simptomatica cu origine la nivelul VD pe cord indemn. (nivel de dovezi C)
Implantarea
ICD poate fi eficienta pentru oprirea TV la pacientii cu functie
ventriculara normala sau aproape de normala si fara
boli cardiace structurale, care primesc un tratament medical permanent optim
si la care se asteapta supravietuire rezonabila, cu un
status functional bun pe o perioada mai mare de 1 an. (nivel de dovezi: C)
12.1.1. Date demografice
si mod de prezentare al tahicardiilor cu origine in tractul de
ejectie al ventriculului
TV cu
origine la nivelul VD este forma cea mai comuna de TV la persoane aparent
sanatoase si se asociaza cu un prognostic bun la cei
fara boli cardiace structurale.291,294,297,377,834-844
Aceste TV au adesea morfologie de BRS cu ax orientat inferior. Sunt adesea
induse prin testul de efort nonischemic si/sau ca TV repetitive
monomorfe. Simptomatologia este blanda, iar sincopa este rara.722
Tahicardia ventriculara cu origine in tractul de ejectie al VS poate
apare in absenta unor boli cardiace structurale si reprezinta un
procent mic din toate cazurile de TV . ECG inregistrat in timpul ritmului
sinusal la pacientii cu tahicardie din tractul de ejectie al VD ne
ajuta sa o diferentiem de displazia aritmogena de VD, unde
ECG este adesea modificat.722 Tahicardia ventriculara cu
origine in tractul de ejectie al VD a fost considerata de mult timp
ca fiind idiopatica, dar ulterior aceasta caracteristica a fost
subliniata de teste diagnostice ca testul de efort, ecocardiografia,
coronarografia.297,834,835,843,845-847 Mai recent RMN a fost
folosita pentru evaluarea pacientilor cu TV cu origine in VD, in
absenta anomaliilordefinite conventional pentru excluderea CAVD.210,262
Tahicardiile ventriculare cu origine in tractul de ejectie al VS pot fi
clasificate dupa locul de origine (la nivelul endocardului, origine la
nivelul cuspelor coronariene, la nivelul epicardului).232 TV cu origine
in tractul de ejectie al VS si sept sunt prezente in mod
caracteristic in a treia sau a patra decada a vietii.694 TV din
LVOT este mai comuna la barbati decat la femei. Aceasta
tahicardie poate fi incesanta si poate fi indusa de efort.
12.1.2 Mecanisme
Mai
multe mecanisme electrofiziologice au fost asociate cu TV din RVOT incluzand
automatismul anormal si activitatea declansata. Cea mai
comuna forma de TV din RVOT este legata de activitatea
declansata prin postdepolarizare tardiva si se
considera ca este dependenta de incarcarea excesiva a
celulei cu Ca si AMPc.377,840,841 TV din RVOT este adesea
sensibila la adenozina, poate fi oprita prin manevre vagale
si e facilitata de catecolamine. Adesea nu e usor de indus la
studiul electrofiziologic, putand necesita rapid burst pacing sau
stimulare cu isoproterenol.210,722 Tahicardia ventriculara cu
origine in tractul de ejectie al VS (LVOT) poate apare prin reintrare sau
prin automatism anormal. TV incesante din VS au fost asociate cu postdepolarizarea
tardiva.4,694 Tahicardia idiopatica cu origine in VS poate
fi sensibila la verapamil, adenozina si propranolol.697-702
12.1.3 Studiul
electrofiziologic
Efectuarea
studiului electrofiziologic este motivata de nevoia de a stabili un
diagnostic precis pentru ghidarea ablatiei curative.209,210
Desi poate apare sincopa, tahicardiile ventriculare cu origine in tractul
de ejectie al ventriculului, in absenta unor boli cardiace concomitente,
nu au un prognostic sever.848 Valoarea prognostica a
inductibilitatii aritmiilor ventriculare nu a fost evaluata in
mod sistematic. O inductibilitate de 80% a fost raportata la 35
pacienti cu TV din RVOT la care s-au efectuat studii electrofiziologice cu
pana la 3 extrastimuli si administrare de isoproterenol daca a
fost necesar.300 Intr-un alt studiu rata inductiei a fost de
numai 3%, dar acesta a crescut pana la 80% dupa administrare de
isoproterenol singur.210 A fost de asemenea folositoare si
inductia prin burst pacing.297
A fost
descrisa TV cu origine in tractul de ejectie al VS (LVOT) sau la
nivelul cuspelor aortice; mecanismul si prognosticul acesteia par sa
fie similare TV din RVOT. Inductia TV din LVOT prin studiu electrofiziologic
nu este deplin consolidata, desi aceasta aritmie poate fi
provocata. Poate fi provocata in timpul administrarii de
isoproterenol.378
12.1.4. Management
Tratamentul
clinic al TV din RVOT sau LVOT adesea implica betablocante sau Ca
blocante. Antiaritmicele din clasa IC par a fi utile in TV din RVOT.297,837,849-852
La pacientii care raman simptomatici sau la cei care terapia nu are
rezultate, trebuie recomandata ablatia.
Rata
succesului ablatiei in RVOT este de peste 90%.210,722 Succesul
pe termen lung al ablatiei variaza si el depinde de
prezenta si gradul altor anomalii.
11.1.5. Date demografice
si modul de prezentare al altor tahicardii ventriculare idiopatice cu
originea la nivelul VS
Asa
numitele TV idiopatice cu originea in VS pot lua nastere din tractul de
ejectie al VS sau din fasciculele sistemului de conducere. TV
fasciculara poate fi impartita in 3 categorii, functie
de originea si de morfologia QRS in timpul tahicardiei. TV cu originea in
fasciculul stang posterior are in mod caracteristic aspect de BRD si axul
QRS orientat superior si este cea mai comuna forma de tahicardie
fasciculara. TV cu originea in fasciculul stang anterior are aspect de BRD
si deviatie axiala dreapta; este mai putin
comuna. Mai rar, TV fasciculara ia nastere in portiunea
inalta a septului interventricular, prezinta QRS ingust, iar axul este in
limite normale. Aceste TV sunt caracteristice decadelor 4-5 ale vietii695
si au distributie egala pe sexe.
12.1.6. Mecanisme si
tratament
Mecanismul
caracteristic al TV cu origine in fasciculul stang este reintrarea si
poate raspunde la betablocante sau blocante ale canalelor de Ca. Oricum,
la pacientii care nu tolereaza tratamentul medicamentos sau cei la
care tratamentul medicamentos nu are succes, se recomanda ablatia.
Ablatia fasciculului stang posterior este ghidata de inregistrarea
facuta in timpul ritmului sinusal sau in timpul TV, prezentand un
potential discret care precede cea mai precoce electrocardiograma
ventriculara.703,704,709,853 Dispozitivele noi de mapping
tridimensional care nu necesita prezenta TV sustinute pot
facilita ablatia la acesti pacienti.710
12.2. Tulburari
electrolitice
Recomandari
Clasa I
Sarurile
de K (sau Mg) sunt folosite in tratamentul aritmiilor ventriculare secundare
hipopotasemiei (sau hipomagneziemiei) rezultate din consumul de diuretice la
pacientii cu structura cardiaca normala. (nivel de dovezi B)
Clasa IIa
Este
recomandata mentinerea unui nivel seric al K de 4 mM/L la
pacientii care prezinta aritmii ventriculare amenintatoare
de viata documentate si care au structura normala cardiaca.
(nivel de dovezi C)
Este
recomandata mentinerea unui nivel seric al K mai mare de 4 mM/L la
pacientii cu infarct miocardic acut. (nivel
de dovezi B)
Sarurile
de Mg pot fi benefice in managementul TV secundare toxicitatii
digoxinului la pacientii cu cord indemn. (nivel de dovezi B)
Desi
modificarile nivelului de K extracelular, Mg intra- si extracelular
(in special in asociere cu hipopotasemia) si ale Ca intracelular sunt
asociate cu modificari electrofiziologice aritmogene, aritmiile
ventriculare ce pun in pericol viata la pacientii cu cord indemn nu
ar trebui sa fie atribuite numai modificarilor concentratiei
acestor ioni. Modificari ale nivelului K pot apare dupa stopul
cardiac sau pot acompania anumite boli ca paralizia periodica.
O
crestere rapida a nivelului de K extracelular, hipopotasemia (mai
putin de 3.5 mM/L) si hipomagneziemia sunt asociate cu aritmii
ventriculare si MSC la pacienti cu cord indemn (unii dintre
acestia putand anumite disfunctii ale canalelor ionice) si la
pacientii cu IMA.591,854-867 Hipomagneziemia este clasic
asociata cu TV polimorfa sau torsada varfurilor, care impreuna
cu aritmiile ventriculare din cadrul infarctului miocardic acut pot
raspunde la administrarea de Mg intravenos.868-871 Hipopotasemia
cu/fara hipomagneziemie, poate fi responsabila de aritmii
ventriculare la pacientii cu hipertensiune sau insuficienta
cardiaca congestiva (precipitate de utilizarea de diuretice tiazidice
si de ansa),855,856,872 la cei cu inanitie
acuta,873 intoxicatie acuta cu alcool sau sevraj
alcoolic, si cei ce utilizeaza digoxin sau antiaritmice de clasa I
Vaughan Williams.865,874,875 Hipocalcemia severa poate duce
la cresterea intervalului QT.
Schimbarile
concentratiei extracelulare a Ca pot produce tulburari
electrofiziologice care la randul lor duc la aritmii ventriculare, pe care
insa nu le intalnim in practica. Ocazional, hiperparatiroidismul
poate cauza cresteri importante ale nivelului de Ca. Fluctuatiile Ca
intracelular influentate de medicamente (ex, digitala), efort fizic (prin
catecolamine) si reperfuzia dupa ischemia miocardica, pot fi
factori declansatori ai unor modificari electrofiziologice ce pun
viata in pericol. Efectul protectiv al betablocantelor la acest ultim
caz, poate fi in parte datorat inhibitiei influxului de Ca in miocite.
12.3. Agentii fizici
si toxici
Recomandari
Clasa I
Abstinenta
completa de la alcool este recomandata in cazurile in care se
banuieste o corelatie intre ingestia de alcool si aritmiile
ventriculare. (nivel de
dovezi C)
Aritmiile
ventriculare ce pun viata in pericol, persistente in ciuda
abstinentei de la alcool, ar trebui tratate in aceeasi maniera
in care sunt tratate aritmiile la pacientii cu alte boli, incluzand
implantarea unui defibrilator la pacientii ce primesc terapie
medicala optima cronica si la care speranta de
supravietuire la standard bun este pentru o perioada mai mare de a 1
an. (nivel de dovezi: C)
Relatia
dintre ingestia de alcool si TV/MSC este indisputabila; ceea ce este
controversat este natura acestei relatii.876 Un numar de studii
sustin o relatie cu aspect de litera J, cu riscul cel mai mic la
pacientii cu ingestie scazuta de alcool (ex, de la 2 la 6
bauturi pe saptamana) comparativ cu cei care nu consuma sau
consuma foarte rar alcool,877 si cei care au o rata
crescuta a ingestiei de alcool (ex, mai mult de 3-5 bauturi pe zi)878,879
si obisnuinta de a consuma cantitati mari de alcool la
petreceri sindromul inimii de vacanta.880-883 Explicatia
acestei legaturi este probabil efectul protectiv al ingestiei unor
cantitati mici-moderate de alcool in ceea ce priveste boala
cardiaca ischemica.884 Acest lucru este contestat
insa de o metaanaliza unde au fost gasite eficacitate scazuta
si chiar efecte daunatoare ale alcoolului, la femei si la
barbati locuitori in afara ariei mediteraneene si de studiile
care au folosit evenimentele fatale ca obiectiv. Mai mult, spre deosebire de
pacientii cu risc scazut (fara boala cardiaca
ischemica), la barbatii de varsta medie cu boala
cardiaca ischemica, ingestia de alcool in cantitati mici pana
la moderate (de la 1 la 14 bauturi pe saptamana) nu a fost
asociata cu un beneficiu semnificativ.885
Ingestia
de alcool poate deci reduce incidenta TV/ MSC datorate evenimentelor
coronariene, dar efectul pe aritmiile amenintatoare de
viata se coreleaza direct cu cantitatea si durata ingestiei de
alcool si chiar o cantitate mica poate fi semnificativa la
pacienti susceptibili.
Mecanismele asociate cu TV/MSC induse de alcool sunt
complexe si nu sunt in intregime legate de prezenta cardiomiopatiei
induse de alcool. Alcoolul are efect inotrop negativ, mediat de
interactiunea directa cu celulele musculare cardiace, desi
aceasta actiune este adesea mascata de efectele indirecte prin
cresterea eliberarii de catecolamine.886 Studiile EF au
aratat ca alcoolul induce diferite aritmii incluzand TV la
pacienti cu si fari cardiomiopatie.887,888 HVS
si remodelarea sunt un raspuns precoce la marii bautori;889
la o treime din alcoolici s-a demonstrat disfunctie diastolica
corelata cu consumul890 si 20-26% dezvolta CMD in 5
ani.891 La acesti pacienti, hipertrofia miocitelor si
a nucleilor, fibroza interstitiala si necroza miocitelor
reprezinta substratul pentru aritmogeneza.892 QTc este
alungit la pacientii cu boala hepatica alcoolica
dovedita in absenaa diselectrolitemiilor si poate fi triggerul
aritmiilor maligne.893
12.3.2. Fumatul
Recomandari
Clasa I
Fumatul
trebuie puternic descurajat la toti pacentii cu aritmii ventriculare
suspectate si documentate si/sau MSC resuscitata. (nivel de dovezi : B)
Fumatul
tigaretelor este un factor de risc independent pentru MSC indiferent de
boala coronariana subiacenta.58,894-897 Majoritatea
acestor decese sunt determinate de aritmii. La femeile care
fumeaza mai mult de 25 tigari pe zi, riscul de aritmii ventriculare
si MSC este crescut de 4 ori, similar post-IM.62 Este un factor de risc pe termen
lung898 si continua sa fie la supravietuitorii
stopului cardiac din afara spitalului care nu renunta la fumat.74
Incetarea fumatului reduce semnificativ riscul de MSC. Nu exista date care
sa permita identificarea indivizilor cu riscul cel mai mare.
12.3.3. Lipidele
Recomandari
Clasa I
Tratamentul cu statine este eficient la pacientii cu
boala coronariana pentru reducerea riscului de evenimente vasculare,
posibil de aritmii ventriculare si MSC. (nivel de dovezi: A)
Clasa IIb
Suplimentarea
cu acizi grasi polinesaturati n3 poate fi considerata la
pacientii cu aritmii ventriculare si boala coronariana
subiacenta. (nivel de dovezi: B)
Asocierea
nivelului crescut de colesterol total, lipoproteine cu densitate mica
si foarte mica, cu HDL scazut, impreuna cu cresterea
trigliceridelor si apolipoproteinei B cu cresterea riscului de
TV/MSC este aproape in totalitate datorata BCI concomitente. Managementul
corespunzator, in special prin utilizarea statinelor, reduce riscul de MSC
prin prevenirea IM recurent fatal si aritmiilor ventriculare.899-901
Efectul hipolipemiantelor in prevenirea primara a MSC nu a fost studiat, dar o
reducere a riscului relativ de 30-40% poate fi asteptata in paralel
cu reducerea riscului de moarte prin BCI.902,903
Acizii
grasi liberi sau acizii grasi neesterificati sunt de asemenea un
factor de risc independent pentru MSC dar nu pentru IM.94 Totusi,
ideea larg raspandita ca dieta bogata in n-3 PUFA poate
conferi protectie pentru moartea aritmica la subiectii cu sau
fara BCI subiacenta documentata,904,905 la
pacientii care au avut manifestari anterioare,904-911 a
fost pusa la indoiala de un trial multicentric mic, dublu-orb,
randomizat versus placebo, cu n-3 PUFA la 200 pacienti cu ICD si
episod recent de aritmie ventriculara.262 Acest studiu a
aratat o tendinta catre o incidenta mai
crescuta a TV/FV la pacientii tratati cu ulei de peste,
corelat cu nivelul de n-3 PUFA. O analiza a timpului pana la
recurenta evenimentului a constatat semnificativ mai multe evenimente la
pacientii tratati cu ulei de peste.
13. Aritmiile
ventriculare si moartea subita cardiaca la populatii
specifice
13.1 Atletii
Recomandari
Clasa I
Anamneza
si examenul fizic, incluzand istoricul familial de MSC prematura
si dovezile de boli cardiovasculare specifice cum sunt cardiomiopatiile
si anormalitatile canalelor ionice, sunt recomandate la
atleti. (nivel de
dovezi: C)
Atletii
prezentand tulburari de ritm, boli structurale sau orice semne sau
simptome de boala cardiovasculara trebuie evaluati ca orice
pacient dar cu recunoasterea situatiei particulare a activitatii
lor. (nivel de dovezi: C)
Atletii
cu sincopa trebuie evaluati atent pentru descoperirea bolilor
cardiovasculare subiacente sau tulburarilor de ritm (nivel de dovezi: B)
Atletii
cu simptome semnificative trebuie sa opreasca activitatea
competitionala pana la evaluarea completa. (nivel de dovezi: C)
Clasa II b
ECG
pe 12 derivatii si ecocardiografia pot fi considerate pentru
screening la atletii cu boala cardiaca. (nivel de dovezi: C)
Este
general acceptat ca screeningul inainte de competitie trebuie
sa fie obligatoriu, dar nu exista standarde uniform acceptate.
Pentru ca riscul de MSC la atleti pare sa il
depaseasca pe cel din populatia corespunzatoare ca
varsta,912 screeningul cardiovascular este de
importanta majora.
Sportul
de performanta a fost definit ca participare la un sport individual
sau de echipa organizat, care presupune competitia regulata cu
alte echipe, care pune la mare pret excelenta si cere
antrenament sistematic.913,914 Screeningul precompetitional a
fost dezbatut in numeroase conferinte si declaratii de
politica, desi802,915,916 programele de screening variaza
mult intre tari. Cauzele majore ale MSC la atleti sunt CHM
(36%), anomaliile arterelor coronare (19%), CAVD si miocardita. In
Italia, incidenta miocarditei ca si cauza de MSC s-a redus
considerabil dupa introducerea programului de screening ECG si
ecocardiografic.917
13.1.1. Screening si
management
13.1.1.1. Screening
Screeningul
cardiovascular se concentreaza in special asupra grupului de tineri
(varsta sub 30 ani), in randul carora majoritatea anomaliilor sunt
congenitale, chiar daca pot exista si afectiuni dobandite.680,915,918
Multiplele mecanisme si boli implicate in moartea subita la tinerii
atleti au fost prezentate.919 Diverse substante pot avea
multiple efecte asupra sistemului cardiovascular si pot duce la spasm
coronarian (cocaina), modificari de repolarizare la pacientii
susceptibili (ex, antibiotice, antiaritmice, antidepresive) si la
modificarea raspunsului la efort (ex, betablocante).920 O
atentie deosebita trebuie acordata atletilor de varsta
mijlocie sau mai varstnici.914
Screeningul
atletilor este o sarcina dificila. Incidenta
scazuta a anomaliilor face ca acesta sa nu fie cost-eficient,
desi un studiu a sugerat ca screeningul ECG este mai eficient din punct de
vedere al costului decat cel prin ecocardiografie.921,922 Examinarea
fizica de rutina poate sa nu releve anomalii clinice
semnificative iar antecedentele personale si heredocolaterale au o valoare
limitata. ECG de repaus poate dezvalui tulburari de ritm,
sindroame de repolarizare anormala cum ar fi LQTS, sindromul Brugada, sindromul
WPW precum si tulburarile de depolarizare si repolarizare
asociate cu CMH. Totusi variatiile nespecifice observate frecvent pe
ECG la adolescentilor si ale tinerilor atleti pot induce in
eroare. Ecocardiografia poate arata anomaliile structurale dar nu si
anomaliile arterelor coronare.
Cu toate
acestea, se recomanda ca, pe langa anamneza si examenul
fizic, toti candidatii sa fie supusi testelor screening prin
ECG si, cand este cazul, ecocardiografie (ex, ECG anormal, antecedente
heredocolaterale). Impactul unor teste aditionale de screening trebuie
clarificat; povara financiara a altor investigatii suplimentare in
cazul suspectarii unor anomalii poate fi considerabila.
13.1.1.2. Managementul
aritmiilor, stopului cardiac si sincopei la atleti
La
atleti factorii de risc pot fi agravati sau atenuati dar nu
eliminati de activitatea fizica regulata. Din motive etice
si legale, atletii care primesc medicatie cardiovasculara
si care poarta aparate cum sunt pacemakerul si ICD, nu pot participa
in general la competitii la nivel inalt. Exceptiile, cum ar fi
medicatia betablocanta, sunt prevazute in ghiduri. Conform
Codului Mondial Anti-Doping elaborat de Agentia Mondiala Anti-Doping
(WADA), una din organizatiile Comitetului Olimpic International,
si acceptat de toate federatiile sportive internationale,
betablocantele si diureticele sunt interzise in unele sporturi. Lista
acestora poate fi gasita pe site-ul WADA www.wada-ama.org si poate fi
downloadata.
Atletii
care prezinta sincopa sau presincopa nu ar trebui sa
participe la competitii pana cand nu se stabileste daca
acestea au o cauza benigna si tratabila. Cresterea
numarului BPV in timpul efortului necesita o evaluare atenta.
Aceasta poate fi determinata de anomalii structurale, cum ar fi anomalii
ale arterelor coronare, origine anormala a arterelor coronare, prolaps de
valva mitrala, CAVD, CMH sau CMD. Antrenamentul de anduranta
este frecvent acompaniat de bradicardie sinusala, ritm jonctional
si conducere atrioventriculara cu perioade Wenckebach pe ECG. In
general, acestea sunt raspunsuri de adaptare la indivizi aparent normali.
Diferenta dintre hipertrofia adaptativa a VS si o forma
usoara de cardiomiopatie poate fi dificil de sesizat. Atletii care
prezinta aritmii ventriculare nesustinute si asimptomatice induse de
efort, pot participa la competitii care nu necesita efort fizic
intens, daca nu exista nici o anomalie cardiaca structurala
dovedita.924 Recomandarile de interzicere a participarii
la sporturile ce necesita efort fizic intens au fost prezentate intr-un
document de consiliere914 precum si la o Conferinta
Bethesda.682,802
Atletii
care prezinta tulburari de ritm, anomalii cardiace sau sincope
trebuie tratati ca orice alti pacienti. Trebuie totusi avut
in vedere ca activitatea fizica intensa poate agrava aceste
anomalii.
13.2. Sexul si sarcina
Recomandari
Clasa I
La
femeile gravide care dezvolta tahicardie ventriculara instabila
hemodinamic sau fibrilatie ventriculara trebuie realizata
cardioversia electrica sau defibrilarea. (nivel de dovezi : B) (vezi sectiunea 7).
La
femeile gravide cu LQST simptomatic este indicat sa se continue tratamentul cu
beta blocante pe parcursul sarcinii si dupa, daca nu sunt
contraindicate absolut. (nivel de
dovezi: C)
13.2.1. Intervalul QT
Tipic,
femeile au interval QT mai lung decat barbatii si aceasta
diferenta este mai pronuntata la frecvente cardiace
mai mici. Intervalul QT corectat la barbati se reduce la pubertate
si apoi creste treptat cand nivelurile de androgeni scad. In jurul
varstei de 50 ani, difereniele dintre sexe in ceea ce priveste intervalul
QT dispar.925 O scurtare similara a intervalului QT la
pubertate a fost observata la barbatii cu genotip de LQTS.926
Aceste observatii sustin ipoteza unor efecte hormonale asupra
intervalului QT deci a susceptibilitatii la aritmii. La femeile cu
LQTS congenital, riscul de stop cardiac este mai mare in perioada postpartum
decat in timpul sau inainte de sarcina.795 Tahicardia
relativa observata in timpul sarcinii poate servi la scurtarea
intervalului QT, jucand astfel un rol protector. Betablocantele aduc
un beneficiu major in timpul perioadei de postpartum, atunci cand
frecventa cardiaca scade natural. Betablocantele pot fi folosite in
general in siguranta in timpul sarcinii. Majoritatea se excreta in laptele
matern. Sunt bine tolerate atat de mama cat si de fat, desi
se poate observa o scadere a frecventei cardiace a fatului.
Cateva studii au demonstrat o susceptibilitate crescuta la femei pentru
torsada varfurilor, cel mai probabil legata de intervalul QT bazal mai
lung si posibil de diferentele de farmacodinamica a
medicamentelor.927 Incidenta formelor de interval QT lung atat
dobandite cat si congenitale precum si a torsadei varfurilor este mai
mare la femei decat la barbati.776,928
In
Registrul Intervalului QT lung, 70% dintre subiecti si 58% din
membrii de familie afectati sunt femei.929 Pana la pubertate,
barbatii au fost mai predispusi la stop cardiac si sincope,
dar apoi incidenta acestor evenimente potential fatale a predominat
la femei.926
Cateva
studii au aratat ca torsada varfurilor indusa medicamentos este
mai frecventa la femei decat la barbati.930-933 ICD
ar trebui recomandata la pacienti cu sindroam de QT lung care
prezinta rezistenta la medicamente si la cei cu risc
crescut de aritmii potential fatale.1
13.2.2. Sarcina si
perioada postpartum
Recomandarile
privind managementul bolilor cardiovasculare, inclusiv al aritmiilor
ventriculare, in timpul sarcinii au fost prezentate.934
Palpitatiile sunt extrem de frecvente in timpul sarcinii si unele
studii au aratat cresterea TSV.935-937 In timp ce
majoritatea palpitatiilor care apar in timpul sarcinii sunt benigne,
tahicardia ventriculara nou aparuta pune probleme deosebite.938,939
Desi prezenta unor anomalii cardiace structurale trebuie
cautata la aceste femei, adesea tahicardia ventriculara apare
fara o modificare structurala subiacenta si poate fi
legata de nivelul crescut de catecolamine.938 In acest caz,
aceste aritmii pot raspunde la terapia cu betablocante. La femeile la care
tahicardia ventriculara debuteaza in ultimele 6 saptamani de sarcina
sau devreme postpartum, trebuie exclusa cardiomiopatia postpartum.940
La femeile cu TV sustinuta nelegata de QT lung survenita in
timpul sarcinii, terapia antiaritmica indicata cuprinde lidocaina
intravenos in situatiile acute sau procainamida pe termen lung. Amiodarona
poate avea un efect negativ asupra fatului incluzand hipotiroidism,
incetinirea cresterii si nastere prematura. Terapia
profilactica cu un betablocant cardioselectiv poate fi eficienta. In
caz ca aceasta nu este eficienta, poate fi folosit sotalolul.941
Pentru femeile cunoscute cu anomalii structurale cardiace, sarcina poate
reprezenta un risc. Edemul pulmonar, accidentul vascular cerebral sau moartea
de cauza cardiaca pot surveni in pana la 13% din aceste cazuri.942
Factori de risc independenti la femeile cu boli cardiovasculare
sunt istoricul de aritmii, cianoza, disfunctia sistolica a
VS, obstructia tractului de ejectie al VS.942 Aritmiile
ventriculare potential letale ar trebui rezolvate prin cardioversie
electrica. Pot fi folosite si betablocantele 1-selective si
amiodarona (cu precautiile prezentate anterior) singure sau in
combinatie, ICD poate fi necesar; prezenta lui nu contraindica
sarcinile viitoare.
13.2.3.
Probleme speciale privind anumite aritmii specifice
Sindromul
WPW si tahicardia ortodromica atrioventriculara
reciprocanta sunt mai frecvente la barbati decat la femei.943,944
In plus, la pacientii cu sindrom WPW caile manifeste sunt mai comune
la barbati. Invers, tahicardia antidromica
atrioventriculara reciprocanta este mai frecventa la femei.
Totusi FA care degenereaza in FV este mai frecventa la
barbati.100 Pentru sindromul WPW simptomatic tratamentul
de electie este ablatia cu RF. Rezultatele sunt similare pentru
ambele sexe.945-947 Managementul sindromului WPW simptomatic in
timpul sarcinii necesita initierea unui tratament cu antiaritmice
pentru a bloca calea accesorie si, la unele paciente, monitorizarea pe
termen lung.
Incidenta
MSC la orice varsta este mai mare la barbati decat la femei.948
In parte, aceasta poate fi legata de frecventa mai mare a bolii
coronariene la barbati. Totusi, chiar in cazul cohortelor
selectionate fara BCI se observa o preponderenta
a barbatilor. Predictorii clasici cum ar fi obezitatea, HVS,
hiperlipemia si fumatul se asociaza cu BCI si TV mai frecvent la
barbati decat la femei.898 La femei, hiperglicemia,
cresterea hematocritului si scaderea capacitatii
vitale sunt predictori mai importanti pentru BCI si TV.898
Impactul diabetului, observat la ambele sexe, este mai pronuntat la femei.
In timp ce TVNS si BPV au fost asociate cu un risc crescut de moarte
subita la barbatii cu sau fara BCI, nu s-a demonstrat
o astfel de asociere la femei.898 Similar, in timp ce BPV post
infarct miocardic la barbati au fost asociate cu o crestere a
mortalitatii, acest lucru nu s-a dovedit adevarat in cazul
femeilor.949
13.3. Pacientii
varstnici
Recomandari
Clasa I
Pacientii
varstnici cu aritmii ventriculare in general trebuie tratati la fel ca
cei tineri. (nivel de dovezi : A)
Dozele
si titrarea antiaritmicelor in cazul pacientilor varstnici trebuie
ajustate conform particularitatilor de alterare a farmacocineticii
la acesti pacienti. (nivel de dovezi : C)
Clasa III
Pacientii
varstinici cu o speranta de viata sub 1 an prin comorbiditati majore, nu
ar trebui sa primeasca ICD.
(nivel de dovezi : C)
13.3.1. Epidemiologie
Aritmiile
ventriculare sunt comune la pacientii varstnici si incidenta
acestora creste in prezenta bolilor structurale cardiace.404,950-952
De notat ca varstnicii sunt un grup heterogen. In diferite studii,
pacientii varstnici sunt definiti ca avand varste de la peste 60 la
peste 85 ani. Aceasta lipsa de uniformitate ridica probleme in
ceea ce priveste aplicabilitatea rezultatelor studiilor la intreaga
populatie varstnica.
Aritmiile
ventriculare pot fi gasite la 70% - 80% din persoanele peste 60 ani,
ectopia ventriculara complexa este comuna la acest grup de
varsta, desi multi dintre pacienti sunt frecvent
asimptomatici.953-956 Aritmiile ventriculare complexe adesea
preced evenimente coronariene majore si MSC la pacienti cu BCI
si alte tipuri de boli cardiace structurale.957,958
Incidenta MSC creste cu avansarea in varsta.959,960
La pacientii varstnici cu BCI, proportia de morti subite
cardiace scade,36,961 in timp ce proportia de MSC din afara
spitalului creste progresiv cu avansarea in varsta.36,414
Desi
mai mult de 80% din pacientii cu MSC au BCI, pacientii varstnici cu
CMD si boli valvulare sunt de asemenea cu risc.957,961 MSC a
fost de asemenea documentata la pacientii varstnici cu CMH,662
CAVD962 si Tetralogie Fallot corectata chirurgical,963
in mod particular la pacientii cu disfunctie de VS. Sindromul Brugada
si LQTS congenital sunt cauze neobisnuite de MSC la pacientii
varstnici.929,964
In
perioada peri-infarct, stopul cardiac (folosit ca surogat de MSC) este mai
comun la pacientii varstnici. Datele din Al Doilea Registru National
de Infarct Miocardic (NRMI-2) arata ca varsta mai are de 75 ani a
fost asociata cu probabilitatea mai mare de stop cardiac in spital, cu
raport de risc de 1,6 (CI 1,5-1,7).965
13.3.2. Tratamentul
farmacologic
Managementul
aritmiilor ventriculare si preventiei MSC la pacientii varstnici
nu difera apreciabil de cele recomandate pentru populatia
generala. Totusi, cand se prescriu medicamente antiaritmice la
pacientii varstnici, trebuie luate in calcul modificarile fiziologice
care apar cu varsta inaintata si trebuie ajustata schema de
tratament in mod corespunzator. Astfel de modificari includ
clearance renal si hepatic scazut si volumul alterat al
distributiei agentilor farmacologici. Trebuie luate in considerare
si schimbarile in compozitia organismului si prezenta
de comorbiditati. Prin urmare, terapia medicamentoasa trebuie
initiata la doze mai joase decat cele uzuale si titrarea dozelor
trebuie sa aiba loc la intervale lungi si cu doze mai mici.
Folosirea
empirica a majoritatii antiaritmicelor in tratarea TVNS si
a altor ectopii ventriculare complexe s-a demonstrat a fi ineficienta in
prevenirea MSC si chiar daunatoare in anumite circumstante.966-970
Varsta avansata creste susceptibilitatea la efectele adverse ale
antiaritmicelor de clasa IC.969 Amiodarona este singurul antiaritmic
demonstrat ca imbunatateste prognosticul supravietuitorilor
stopului cardiac, bazat pe o metaanaliza a 15 trialuri randomizate971
(vezi sectiunea 6.3.1 pentru discutii suplimentare).
Amiodarona
este un drog asociat cu numeroase efecte secundare la pacientii varstnici,
care sunt predispusi sa dezvolte efecte secundare, si care in
mod frecvent urmeaza tratament cu mai multe medicamente, crescand riscul
interactiunilor.404,972 De aceea cand se ia in calcul terapia
cu amiodarona pentru preventia MSC la pacientii varstnici care
primesc terapie multipla pentru conditii comorbide, medicul curant
trebuie sa cantareasca beneficiul potential al unei astfel de
terapii contra potentialelor sale efecte secundare si sa
decida daca amiodarona este cea mai buna terapie pentru acest
pacient.
S-a
demonstrat in multe studii ca betablocantele, alaturi de alti
agenti care nu poseda proprietati antiaritmice clasice
(IECA, blocantii receptorilor de angiotensina, statine) reduc
mortalitatea totala si MSC post-IM la toate grupele de varsta,
inclusiv la varstnici.110,973-976 In trialul Beta Blocker Heart
Attack analiza pe subgrupuri a demonstrat ca cel mai mare beneficiu al
betablocantelor apare in grupul de varsta 60-69 ani.973
Combinatia de betablocant si amiodarona poate sa
reduca mortalitatea totala si MSC mai mult decat amiodarona
singura,404,405 si intr-o analiza post-hoc a datelor
din CAST pacientii tratati cu un antiaritmic care primeau de asemenea
un betablocant au avut o rata mai joasa a MSC decat aceia
tratati doar cu antiaritmic.977 Betablocantele s-a demonstrat
ca reduc mortalitatea totala si MSC la pacientii cu IC
severa.978,979 In aceste studii analiza pe subgrupuri a aratat
beneficiul echivalent al terapiei cu betablocante la pacientii tineri
si varstnici.
In ciuda
eficacitatii demonstrate in reducerea mortalitatii totale
si MSC, betablocantele sunt sub-folosite la varstnici. O analiza
retrospectiva a folosirii betablocantelor dupa IM la pacientii
cu varste mai mari de 65 ani, a aratat ca doar 21% din 3737
pacienti fara contraindicatii au fost tratati.
Pacientii care au primit acesti agenti au avut o mortalitate la
2 ani cu 43% mai mica.980 Similar, un studiu al practicilor
clinice si al surselor de variatie terapeutica a demonstrat o
asociere negativa puternica, independenta intre varstp si
sansele tratamentului cu betablocante dupa IM.981 Aceste
informatii sunt un subiect de mare preocupare pentru sanatatea
publica.
13.3.3. Terapia cu
dispozitive
Cateva
trialuri randomizate prospective au demonstrat eficienta ICD in reducerea
MSC la pacientii cu BCI cu risc inalt pentru MSC (preventie
primara) si la pacientii cu MSC resuscitata
(preventie secundara) comparativ cu terapia antiaritmica medicamentoasa.192,
266-268,642,643
Toate aceste
studii au inclus un numar substantial de pacienti cu varsta
peste 65 ani. Analiza subgrupurilor in AVID si MADIT II a demonstrat
beneficii echivalente ale implantarii ICD la pacientii tineri si
varstnici.266,268 In trialul Cardiac Arrest Study Hamburg (CASH)
pacientii cu varsta peste 65 aniau avut un beneficiu mai mare decat cei
maitineri.643 Se poate presupune ca aceste rezultate sunt
aplicabile la toti pacientii varstnici.
Date
care sa compare eficienta si complicatiile terapiei ICD la
pacientii varstnici fata de cei mai tineri sunt putine.
Intr-un studiu retrospectiv care a comparat eficacitatea terapiei ICD la
pacientii >65 ani fata de cei <65 ani982 nu s-a
notat nici o diferenta semnificativa a morbiditatii
chirurgicale sau de durata a spitalizarii dupa implantarea ICD,
intre cele doua grupuri. In plus, rate similare de supravietuire au
fost calculate la cele 2 grupe la 1, 2 si 3 ani dupa implantare.
In mod
similar intr-un studiu observational983 al unui numar de
450 de pacienti care au primit ICD epicardic (46%) sau transvenos (54%),
supravietuirea la 3, 5 si 7 ani pentru mortalitatea aritmica a
fost similara la pacientii tineri si varstnici. Morbiditatea
perioperatorie a fost de asemenea similara la toate grupurile de
pacienti.
In ciuda
acestor beneficii documentate ale ICD, multi medici au ezitat sa
supuna pacientii varstnici la asemenea interventii si
rolul dispozitivelor implantate la acest grup de varsta a fost
controversat. Totusi, cateva studii observationale au aratat ca
abordarea invaziva in managementul pacientilor cu aritmii
ventriculare amenintatoare de viata este benefica in
mod egal la tineri si varstnici.984-986 Din 1985 pana in
1995, folosirea ICD la pacientii varstnici a crescut de la 1% la 13%;
acest lucru a fost asociat cu imbunatatirea supravietuirii
pe termen mediu.987
Pacientii
foarte varstnici cu multiple comorbiditati si speranta
de viata limitata pot sa nu fie candidati
potriviti pentru terapia cu ICD, chiar daca au criteriile standard.
In aceste circumstante, gandirea clinica a medicului curant si
dorintele pacientului si/sau ale familiei sale sunt prioritare
fata de recomandarile generale de terapie. Exista dovezi
dintr-un studiu988 ca octogenarii care mor subit pot fi chiar
bine echilibrati in luna dinaintea decesului. Aceasta
informatie sustine conceptul ca MSC loveste adesea
pacientii varstnici echilibrati, cu status functional bun, care
ar putea beneficia de ICD daca ar indeplini criteriile.
13.4. Copiii
Recomandari
Clasa I
ICD
trebuie implantat la copiii supravietuitori ai unui stop cardiac atunci
cand o cautare profunda a unei cauze corectabile este negativa iar pacientii
primesc terapie medicala optima si o speranta de
viata rezonabila cu un status functional bun mai mult de 1
an. (nivel de
dovezi: C)
Evaluarea
hemodinamica si EF trebuie realizata la pacientii tineri cu
tahicardie ventriculara sustinuta simptomatica. (nivel de dovezi: C)
Terapia
ICD conjugata cu terapia medicamentoasa este indicata la
pacientii copii cu risc inalt cu fond genetic de boala (defecte de
canale ionice sau cardiomiopatie) pentru MSC cat si pentru aritmiile
ventriculare sustinute. Decizia de a implanta un ICD la un copil trebuie
sa tina cont de riscul MSC asociat cu boala, beneficiul potential
echivalent al terapiei medicale, ca si de riscul malfunctiei
dispozitivului, infectiei sau rupturii de sonda, si daca
exista o speranta de viata rezonabila cu un
status functional bun mai mult de 1 an.
(nivel de dovezi: C)
Clasa IIa
ICD
este rezonabil pentru pacientii copii cu aritmii ventriculare spontane
sustinute asociate cu functie ventriculara diminuata
(FEVS de 35% sau mai putin) care primesc terapie medicala
optima si o speranta de viata rezonabila
cu un status functional bun mai mult de 1 an. (nivel de dovezi: B)
Ablatia
poate fi folositoare la copiii cu conducere aberanta simptomatica
sau tahicardie ventriculara cu origine in tractul de ejectie sau in
sept, care este rezistenta la medicatie, cand pacientul nu tolereaza
drogul sau nu doreste ss ia medicamente. (nivel de dovezi: C)
Clasa III
Tratamentul farmacologic
al BPV izolate la pacientii copii nu este recomandat. (nivel de dovezi: C)
Digoxinul
sau verapamilul nu ar trebui folosite pentru tratamentul tahicardiei
sustinute la copii cand TV nu a fost exclusa ca diagnostic potential.
(nivel de dovezi: C)
Ablatia
nu este indicata la pacientii tineri cu TVNS asimptomatica
si functie ventriculara normala. (nivel de dovezi: C)
Incidenta
MSC datorata bolii cardiovasculare este semnificativ mai mica la
copii decat la adulti. Estimarile curente arata ca decesele
prin bolile cardiovasculare la indivizii mai tineri de 25 ani reprezinta
mai putin de 1% din intreaga mortalitate cardiaca.36
Conform cu aceasta rata joasa studiile populationale
epidemiologice a trebuit sa defineasca incidenta mortii
subite, neasteptate la pacientii copii. Aceste studii au fost relativ
consistente, cu o rata a evenimentelor intre 1,3 si 4 decese la
100000 pe an.49,989-991 O cauza definita sau probabil
cardiaca a fost estimata la 70% din victimele tinere ale mortii
subite neasteptate.433 Aceasta este comparata cu rata estimativa
a MSC de 100 la 100000 pe an la pacientii adulti.992
Data fiind incidenta joasa a evenimentelor nici un trial randomizat
nu a reusit sa defineasca nici stratificarea riscului pentru
MSC la tineri nici rolul terapiei de preventie primara. Deci, nivelul
de dovezi pentru majoritatea recomandarilor la pacientii tineri este
de clasa C.
In ciuda
acestor limitari, cateva grupuri de pacienti tineri au fost
identificate ca avand un risc mai mare de MSC comparativ cu populatia
generala. Ele includ pacientii cu boli congenitale cardiace, anomalii
ale arterelor coronare, cardiomiopatii si aritmii primare ca LQTS.993
Riscul MSC si semnificatia aritmiilor ventriculare la ace.ti
pacienti sunt discutate in sectiuni separate. Acest capitol trateaza
aritmiile ventriculare in populatia pediatrica generala
si semnificatia lor ca factor de risc pentru MSC.
MSC la
copiii cu sindrom WPW este neobisnuita si survine la
pacientii cu sincopa anterioara, cu multiple cai accesorii
sau perioade refractare scurte. De aceea, la pacientii selectati, un
studiu EF poate fi indicat si ablatia efectuata daca pacientul
este simptomatic sau perioada refractara a fasciculului accesor este
egala sau mai mica de 240 ms.279
BPV
izolate sunt comune la copii, 15% din nou-nascuti avand ectopii
ventriculare la monitorizarea ECG pe 24 ore. Prevalenta ectopiei
ventriculare scade la mai putin de 5% la copii, dar apoi creste
la 10% la varsta de 10 ani si la 25% in adolescenta tarzie
si perioada de adult tanar.994-996 Pentru majoritatea
pacientilor tineri cu ectopie ventriculara, obiectivul primar este
sa se excluda orice boala cardiaca functionala
sau structurala; in aceste cazuri BPV pot avea semnificatie prognostica.434,997
Ectopia ventriculara simpla in absenta bolilor cardiace nu s-a
demonstrat ca are semnificatie prognostica.
Aritmiile
ventriculare sustinute poate apare la copii, fiind cel mai frecvent un
ritm accelerat idioventricular. Prin definitie acesta este un ritm
ventricular cu frecventa mai mare de cea sinusala cu maximum 20%
si care apare in absenta altor boli cardiace.998 Aceasta
aritmie dispare tipic spontan in timpul primelor luni de viata. Aceasta
este in contrast cu TV incesanta, rara la copii, care se
datoreaza tumorilor miocardice sau cardiomiopatiei.999,1000 FV
si MSC au fost raportate la acesti copii cel mai adesea dupa
administrarea de digoxin sau verapamil iv pentru un diagnostic prezumtiv de
TSV.1001,1002 Aceste aritmii ventriculare pot raspunde la
tratament antiaritmic sau la rezectie chirurgicala. TV sustinute
la copii poate fi cauzate de hiperpotasemie sau asociate cu una dintre formele
de LQTS, in mod particular acele forme cu bloc AV sau sindactilie.790,1003,1004
Are loc
o dezbatere considerabila privind sindromul mortii subite la copil
(SIDS) si rolul potential al LQST in declansarea unora dintre decese.1005,1006
Totusi, studiile populationale au demonstrat un declin de 40% in incidenta
SIDS asociata cu evitarea dormitului cu fata in jos, sustinand apneea
sau disfunctii de reglare respiratorie drept cauza primara a
SIDS in majoritatea cazurilor.1007 Definitia cauzelor de SIDS
ramane o arie de continua investigatie si include disfunctia
autonoma si arimiile ventriculare datorate cauzelor genetice.
Dincolo
de primul an de viata, majoritatea copiilor cu ectopie complexa
sau TV tolerata hemodinamic par sa aiba prognostic bun.233,1008
Cauza acestor aritmii ramane necunoscuta si adesea se
rezolva spontan. Supresia farmacologica a acestor aritmii
ventriculare este in general ineficace si mareste riscul
evenimentelor adverse ulterioare. Tahicardia cu origine in tractul de
ejectie si cea cu origine in septul VS pot fi diagnosticate in timpul
copilariei si adolescentei. Criteriile de diagnostic pentru
aceste aritmii specifice sunt discutate in sectiunea 12. Prognosticul
general pentru aceste aritmii este benign, tratamentul cu ablatie pentru
pacientii simptomatici avand o rata mare de succes. Ca si in
alte aritmii pediatrice, un obiectiv primar este de a exclude orice boala
cardiovasculara asociata. TV polimorfa catecolaminergica
sau indusa de efort este o exceptie de la prognosticul benign al TV
tolerata hemodinamic la pacientii cu cord normal. Desi pacientii
cu o astfel de forma de TV pot sa nu fie simptomatici, ei au risc de
MSC.105 De asemenea, aritmiile ventriculare simptomatice pot fi
modalitatea initiala de prezentare a cardiomiopatiei la
pacientii tineri.834,1009
Rolul
si beneficiul implantarii de ICD pentru prevenirea MSC la copiii
mici cu disfunctie ventriculara avansata nu a fost definit. La
copiii mai mari si la adolescenti, implantarea profilactica a
ICD poate fi luata in considerare, bazata pe date provenite din trialuri
clinice randomizate de la pacienti similari.8,248
Tratamentul
aritmiilor potential amenintatoare de viata la copii
este specific in functie de boala (betablocante pentru LQTS,
ablatie pe cateter sau chirurgicala pentru TV focale si
transplantul cardiac pentru cardiomiopatia in stadiul final). Cand au
indicatie, implantarea ICD transvenos este in general realizabila la
copii mai mari de 10 ani.1 Totusi, exista o ingrijorare in
ceea ce priveste longevitatea sistemelor intravasculare cand sunt folosite
pentru zeci de ani de viata.1010 Folosirea ICD la copii
mici si aceia cu boli cardiace congenitale complexe ramane o
provocare si adesea necesita folosirea sistemelor epicardice sau
subcutanate. Cea mai mare incidenta a esecului sistemului
si infectiei sau erodarii la acesti pacienti mandateaza
folosirea judicioasa a acestor dispozitive la pacientii tineri.1011
13.5. Pacienti cu
cardioverter-defibrilator implantabil
Recomandari
Clasa I
Pacientii
cu ICD ar trebui regulat evaluati si sa li se faca analiza
statusului dispozitivului. (nivel de dovezi: C)
ICD
implantate ar trebui sa fie programate astfel incat sa se obtina
sensibilitate si specificitate optime. (nivel de dovezi: C)
Trebuie
luate masuri de minimizarea riscului terapiei inadecvate ICD. (nivel de
dovezi: C)
Pacientii
cu ICD implantat care se prezinta cu TV incesanta ar trebui
spitalizati pentru evaluare. (nivel de dovezi: C)
Clasa IIa
Ablatia pe cateter
poate fi utila la pacientii cu ICD care au TV incesanta sau
frecvent recurenta. (nivel de
dovezi: B)
La
pacienti cu descarcari inadecvate ale ICD, evaluarea EF poate fi
de folos pentru diagnosticul si tratament. (nivel de dovezi: C)
Implantarea
unui ICD nu scade incidenta aritmiilor, desi pacientul este protejat
de consecintele acestora.
13.5.1. Tahiaritmii
supraventriculare
TSV
poate declansa activarea ICD datorita indeplinirii criteriilor
programate de detectie a tahicardiilor ventriculare sau supraventriculare.
Efectul tahiaritmiilor atriale pe frecventa ventriculara este
crucial. Atata timp cat frecventa ventriculara se potriveste cu
fereastra de detectie a tahicardiei, programarea algoritmului de detectare
poate preveni activarea dispozitivului pentru TV. Daca frecventa
ventriculara este mai mica decat fereastra de detectare a FV, terapia
adecvata nu ar trebui sa fie intrerupta (vezi sectiunea
7.6). Algoritmuri sofisticate cresc specificitatea terapiei TV si
ajuta la evitarea terapiei bazate doar pe criteriul frecventei.1012-1014
Betablocantele sunt de asemenea o terapie pretioasa care va preveni
multe interventii nedorite cauzate de aritmiile supraventriculare.
Investigatii suplimentare cum ar fi inregistrarea Holter si studii EF
pot fi necesare in a ghida managementul acestor aritmii.
13.5.2. Tahicardia supraventriculara
la pacienti cu ICD ventricular
Analiza
episoadelor se bazeaza in principal pe informatia primita de la
sonda ventriculara a ICD desi in unele cazuri activitatea
atriala este de asemenea simtita (vezi mai departe).1015
Analiza atenta a episoadelor detectate, efectele pacing-ului
antitahicardic pe lungimea intervalelor de ciclu si modul de terminare
sau accelerare este important in clasificarea tahicardiei detectate.
Algoritmuri discriminatorii potentate ajuta la reducerea terapiei
inadecvate a TV bazata numai pe criteriul frecventei. FA este cel mai
frecvent implicata. Frecventa ventriculara rapida in timpul
TSV poate provoca pacingul ventricular antitahicardic. Actiunea dispozitivului
poate fi proaritmica, pacingul antitahicardic neadecvat care poate cauza
TV sau FV.1016
13.5.3. ICD dual cameral
ICD dual
cameral furnizeaza caracteristici atriale de diagnostic
imbunatatite cu privire la electrocardiogramele atriale
locale, regularitatea semnalelor atriale si lungimea ciclului. Acesta
poate furniza caracteristici aditionale pentru a evita terapii inadecvate
ale TV/FV dar detectarea inadecvata inca apare in 10-15% din cazuri.1017
Oversensingul unor semnale indepartate de electrozii atriali ar produce
descarcarea inadecvata pentru TSV, cum sunt pacingul antitahicardic
sau cardioversia automata. In cazul terapiei de cardioversie atriala
interna programata, chiar socurile de energie joasa pot fi
dureroase si pot compromite calitatea vietii.1018 Pacingul
antitahicardic atrial cu rata inalta poate induce (tranzitoriu)
fibrilatia atriala. Eficacitatea pacingului atrial avansat sau a
cardioversiei variaza mult in functie de durata episodului, de
lungimea ciclului atrial si mecanismul tahicardiei atriale.1013,1019,1020
Eficacitatea acuta a pacingului antitahicardic atrial poate fi mai mare
de 40%.1013
13.5.4. Furtuna aritmica
la pacientii cu ICD
Termenul
de furtuna aritmica se refera la o situatie in care
numeroase descarcari apar datorita episoadelor aritmice
repetitive recurente. Un cerc vicios intre actiunea dispozitivului
si disfunctia cardiaca poate conduce la o deteriorare
ulterioara. Managementul trebuie sa se adreseze tuturor aspectelor
pentru a corecta aceasta situatie (vezi sectiunea 7.6).
13.6. Aritmii induse de
medicamente
13.6.1. Indroducere
Datorita
faptului ca problema aritmiilor induse de medicamente este sporadica,
trialuri clinice randomizate dublu-orb, cu foarte putine exceptii, nu
au fost realizate. Sindroame specifice de aritmii induse de medicamente, cu
mecanisme si strategii de management diverse, sunt descrise in
sectiunile urmatoare. Ghidurile de tratament se concentreaza pe
evitarea tratamentului la pacientii cu risc crescut, recunoasterea
sindroamelor de aritmii induse de medicamente si retragerea
agentilor implicati. Eficacitatea terapiilor specifice este adesea
dedusa din date anamnestice sau preclinice, din studii de macanisme.
Concentratii
inalte de medicamente datorate supradozajului sau interactiunii
medicamentoase cresc in general riscul de aritmii induse de medicamente. Cea
mai mare crestere a concentratiei apare atunci cand un drog este
eliminat printr-o singura cale si aceasta este susceptibila la
inhibitie prin administrarea unui al doilea medicament. Tabelul 11
enumera exemple de interactiuni medicamentoase care pot cauza
aritmii prin acest mecanism. Interactiunile pot de asemenea reduce concentratia
plasmatica a medicamentelor antiaritmice si in consecinta
exacerbeaza aritmia tratata. Efecte farmacologice aditionale
pot de asemenea rezulta in aritmii.
Toxicitatea digitalica
Recomandari
Clasa I
Anticorpi
antidigitalici sunt recomandati pentru pacientii care se
prezinta cu aritmii ventriculare sustinute, BAV avansat si/sau
asistola care se considera ca sunt determinat de toxicitatea
digitalica. (nivel de
dovezi: A)
Clasa IIa
Pacientii
care iau digitala si care se prezinta cu toxicitate
cardiaca usoara (doar batai premature izolate) pot fi
tratati eficient prin recunoasterea, monitorizarea continua a
ritmului cardiac, scoaterea digitalei, restabilirea nivelurilor electrolitice
normale (incluzand potasiul seric mai mare de 4 mM/l) si oxigenoterapie. (nivel de dovezi: C)
Magneziul
sau pacingul sunt rezonabile la pacientii sub tratament digitalic care se
prezinta cu toxicitate severa (arimii ventriculare sustinute,
BAV avansat si/sau asistola). (nivel
de dovezi: C)
Clasa IIb
Dializa
pentru tratamentul hiperpotasemiei poate fi considerata la pacientii
care iau digitala si se prezinta cu toxicitate severa (aritmii
ventriculare sustinute, BAV avansat si/sau asistola). (nivel de dovezi: C)
Clasa III
Tratamentul
cu lidocaina sau fenitoina nu este recomandat la pacientii care
iau digitala si care se prezinta cu toxicitate severa
(aritmii ventriculare severe, BAV avansat si/sau asistola). (nivel de dovezi: C)
13.6.2.1. Prezentare
clinica
Anumite
aritmii sunt tipice: cresterea automatismului atrial, jonctional
sau ventricular (cu batai ectopice sau tahicardie), adesea combinate
cu BAV. Supradozajul digitalic cauzeaza hiperpotasemie severa si
oprire cardiaca. Diagnosticul se stabileste prin combinarea tulburarilor
de ritm cardiac, simptomelor auxiliare (tulburari de vedere,
greata, tulburari in mentatie), si cresterea
concentratiei serice. Factori contributori pot include hipotiroidismul,
hipopotasemia sau disfunctia renala.
13.6.2.2 Tratamentul specific
In
cazurile usoare, tratamentul include intreruperea administrarii
medicamentului, monitorizarea ritmului si mentinerea potasiului seric
normal. Ocazional, pacingul temporar poate fi necesar. Pentru intoxicatii
mai severe (concentratia serica a digoxinei mai mare de 4-5 ng/ml,
si cu aritmii severe), tratamentul de ales este cu anticorpi Fab digoxin
specifici.1022 Intr-o serie de 150 de pacienti cu intoxicatie
severa, raspunsul a fost rapid (30 minute pana la 4 ore),
si 54% din pacientii care s-au prezentat cu oprire cardiaca au
supravietuit. Efectele adverse includ agravarea bolii subiacente
(cresterea ratei ventriculare in timpul FA) si hipopotasemia. Monitorizarea
concentratiei de digoxin este nerelevanta dupa anticorpi
antidigoxina. Terapii folosite anterior cum ar fi lidocaina sau fenitoina
au un rol minor.
13.6.3. Sindromul de QT lung
indus de medicamente
Recomandari
Clasa I
La
pacientii cu sindrom de QT lung indus de medicamente, indepartarea
agentilor implicati este indicata. (nivel de dovezi: A)
Clasa IIa
Tratamentul
cu sulfat de magnesiu intravenos este recomandat pacientilor care iau
medicamente care alungesc intervalul QT si prezinta cateva episoade
de torsada de varfuri in care intervalul QT ramane lung. (nivel de dovezi: B)
Pacingul
atrial sau ventricular sau isoproterenolul este recomandat pentru
pacientii care iau medicamente care alungesc intervalul QT si se
prezinta cu torsade de varf recurente. (nivel
de dovezi: B)
Clasa IIb
Repletia
potasiului la 4,5-5 mmol/l, poate fi recomandata la pacientii care iau
medicamente care alungesc QT si prezinta cateva episoade de torsada
de varfuri in care intervalul QT ramane lung. (nivel de dovezi: C)
13.6.3.1. Caracteristici
clinice
Alungirea
marcata a intervalului QT, adesea acompaniata de morfologii
distinctive de TV sau torsada de varfuri, apare in 1 pana la 10% din
pacientii care primesc medicamente antiaritmice care alungesc QT si
mult mai rar la pacientii care primesc medicamente non-cardiovasculare cu
potential de alungire a QT. In timp ce multe medicamente au fost asociate
cu cazuri izolate de torsada de varfuri, tabelul 12 cuprinde acele medicamente
in general recunoscute ca avand potential de alungire a QT. O lista
cu asemenea medicamente poate fi gasita pe pagina de internet www.qtdrugs.org si www. torsades.org.
Majoritatea
cazurilor de torsada de varfuri induse de medicamente prezinta o
serie scurt-lung-scurt de modificaari de lungime a ciclului anterior
initierii tahicardiei. Intervalele QT, necorectate in functie de
frecventa, sunt in general mai mari decat 500 ms, o proeminenta
unda U este comuna, si alungirea marcata a QTU poate fi
evidenta numai dupa batai postpauza. Factori de risc majori
pentru torsada de varfuri indusa de medicamente sunt inclusi in
Tabelul 13; adesea este prezent mai mult decat unul. Medicamentele pot expune
sindroame de QT lung subclinice; in plus unele studii au implicat variante mai
comune de ADN (polimorfisme, cu frecventa de pana la 15% in unele
populatii).70,1023
Prezentarea
alungirii QT indusa de medicamente include detectia incidentala
la un pacient asimptomatic, palpitatii datorita extrasistolelor
frecvente si aritmiilor ventriculare nesustinute, sincope datorita
episoadelor prelungite de torsade de varfuri sau MSC. Masura in care MSC,
la pacientii care primesc medicamente care alungesc QT, reprezinta
torsada de varfuri este nesigura. Agent care alungeste QT,
d-sotalolul a crescut mortalitatea intr-un trial clinic randomizat (SWORD Survival
With Oral D-sotalol), un efect care poate fi datorat torsadei de varfuri.970
In trialul DIAMOND (Danish Investigators of Arrhytmia and Mortality on
Dofetilide), 3,3% din pacientii cu insuficienta
cardiaca severa au avut torsada varfurilor in timpul primelor 72 ore
de terapie cu dofetilid.1024 Concentratii crescute de
eritromicina obtinute prin terapie intravenoasa au fost asociate cu
torsada de varfuri, si un studiu al MSC in baza de date Medicaid a
implicat combinarea dintre eritromicina pe cale orala si medicamente ce
blocheaza metabolismul in cresterea MSC.603
Tabelul 11.
Interactiuni medicamentoase care produc aritmii
|
Medicament
|
Medicament cu care interactioneaza
|
Efect
|
|
Cresterea concentratiei
medicamentului aritmogen
|
|
Digoxin
|
Antibiotice
|
Prin
distrugerea florei care metabolizeaza digoxinul, unele antibiotice pot creste
biodisponibilitatea digoxinului. Nota: unele antibiotice de asemenea
interfera cu glicoproteina P( exprimata in intestine si in alta parte), alt
efect care poate creste concentratia digoxinului
|
|
Digoxin
|
Amiodarona
|
Creste
disponibilitatea digoxinului, scade excretia biliara prin inhibarea
glicoproteinei
|
|
Chinidina
|
|
|
Verapamil
|
|
|
Ciclosporina
Itraconazole
|
Toxicitate digitalica
|
|
Eritromicina
|
|
|
Chinidina
|
Ketoconazol
|
Creste nivelul
|
|
Cisaprid
|
Itraconazol
|
|
|
Terfenadina, astemizol
|
Eritromicina
*
Claritromicina
Unele blocante ale canalelor de Ca*
|
|
|
Unii inhibitori de proteaza
|
|
|
(especially ritanovir)
|
|
|
Betablocante propafenona
|
Chinidina
(chiar doze foarte mici)
|
Creste betablocarea
|
|
Fluoxetina
|
Creste betablocarea
|
|
Flecainida
|
Unele antidepresive
triciclica
|
Cresc efectele adverse
|
|
Scade
analgesia (scaderea transformarii in metabolitul activ-morfina)
|
|
Dofetilid
|
Verapamil
Cimetidina
|
Cresc
concentratia plasmatica a dofetilidului prin inhibarea
excretiei renale
|
|
Trimethoprim
Ketoconazol
|
|
Megestrol
|
|
|
Scaderea concentratiei
medicamentului antiaritmic
|
|
Digoxin
|
Antiacide
|
Scade absorbtia
|
|
Rifampin
|
Creste activitatea
glicoproteinei P
|
|
Chinidina, mexiletina
|
Rifampin, barbiturice
|
Induce metabolizarea
|
|
Efect synergic provocand aritmii
|
|
Antiaritmice care prelungesc QT
|
Diuretice
|
Risc mare de torsada prin
hipokaliemie
|
|
Betablocante
|
Amiodarona, clonidina, digoxin,
|
Bradicardia
|
|
diltiazem, verapamil
|
|
|
Digoxin
|
Amiodarona, betablocantes,
|
|
|
clonidina, diltiazem,
|
|
|
verapamil
|
|
|
Verapamil
|
Amiodarona, betablocante,
|
|
|
clonidina, digoxin, diltiazem
|
|
|
Diltiazem
|
Amiodarona, betablocante,
|
|
|
clonidina, digoxin, verapamil
|
|
|
Clonidina
|
Amiodarona, betablocante,
|
|
|
digoxin, diltiazem, verapamil
|
|
|
Amiodarona
|
Betablocante, clonidina,
|
|
|
digoxin, diltiazem, verapamil
|
|
|
Sildenafil
|
Nitrati
|
Vasodilatatie
accentuata si persistenta; risc de ischemie miocardica.
|
|
*Se
pot acumula la niveluri toxice si la asocierea cu inhibitori precum
Ketoconazol. Dupa Roden DM, Anderson ME. Proarrhythmia. In: Kass RS,
Clancey CE, ed. Handbook of
Experimental Pharmacology: vol. 171. Basis and Treatment of Cardiac
Arrhythmias. Boston: Springer Verlag, 2006:288 304 (1021).
|
| | | | | |
Tabelul 12. Exemple
de medicamente ce produc torsada de varfuria
|
Frecvent (mai mare de 1%)
(ex, spitalizare pentru monitorizare recomandata in timpul
initierii medicamentului in cateva circumstante)
Disopiramida
Dofetilid
Ibutilid
Procainamida
Chinidina
Sotalol
Ajmalina
Mai putin frecvent
Amiodarona
Trioxid arsenic
Bepridil
Cisaprid
Anti-infectioase:
claritromicina, eritromicina, halofantrin, pentamidin, sparfloxacin
Antiemetice: domperidona,
droperidol
Antipsihotice:
clorpromazina, haloperidol, mesoridazin, tioridazin, pimozid
Agenti opioizi: metadona
|
|
a Vezi www.qtdrugs.org
si www.torsades.org
pentru lista la zi. Adaptat dupa Roden
DM. Drug-induced
prolongation of the QT interval. N Engl J Med 2004;350:101322. Copyright ©
2004 Massachusetts Medical Society.1025
|
Tabelul 13. Factori de risc pentru torsada de varfuri
indusa de medicamente
|
Sexul feminin
Hipopotasemia
Bradicardia
Conversia recenta
din fibrilatia atriala
Insuficienta
cardiaca congestiva
Terapia digitalica
Concentratii inalte
ale medicamentelor (exceptie: chinidina), adesea datorita
interactiunilor medicamentoase
Administrare
intravenoasa rapida a medicamnentului
Alungirea de baza a
QT
Aritmii ventriculare
Hipertrofia
ventriculara stanga
Sindromul de QT lung
congenital
Polimorfism ADN
Hipomagneziemie
severa
Folosirea
concomitenta a 2 sau mai multe medicamente ce alungesc intervalul QT
Combinarea de medicamente
ce alungesc QT cu inhibitorul sau metabolic
|
|
Adaptat dupa Roden
DM. Drug-induced prolongation of the QT interval. N Engl J Med
2004;350:101322. Copyright © 2004 Massachusetts Medical Society.1025
ADN, acid dezoxiribonucleic
|
13.6.3.2. Tratament
Monitorizarea
pacientilor aflati la risc inalt in timpul initierii
medicamentelor antiaritmice ce alungesc QT si recunoasterea sindromului
cand apare este primul pas. Mentinerea potasiului seric intre 4,5-5mEq/l
scurteaza QT;1026,1027 nu sunt date specifice disponibile pentru
eficacitatea repletiei potasiului in prevenirea torsadei de varfuri.
Magneziul intravenos poate supresa
episoadele de TORV fara a scurtarea obligatorie a QT, chiar in
conditiile in care magneziul seric este normal.1028 Toxicitatea
magneziului (areflexia mergind pana la depresie respiratorie) poate apare
cand concentratia atinge 6-8 mEq/l dar este un foarte mic risc cu
dozele uzuale folosite in torsada de varf, 1 pana la 2 g intravenos.
Pacingul temporar este superior in tratamentul torsadei de varfuri care este
recurenta dupa repletia potasiului si suplimentarea cu
magneziu. Isoproterenolul poate fi de asemenea folosit pentru a creste
frecventa cardiaca si a aboli pauzele postectopice. S-a raportat
ca lidocaina,1029 verapamilul,1030 si ocazional
amiodarona1031 au fost eficiente. Oricum, amiodarona
insasi poate determina TORV, desi mai rar decat alte
antiaritmice care alungesc QT.1032
13.6.4. Toxicitatea
determinata de blocantii de canale de sodiu
Recomandari
Clasa I
La
pacientii cu toxicitate determinata de blocantii de canale de sodiu,
intreruperea agentului implicat este indicata. (Nivel de dovezi: A)
Clasa IIa
Oprirea
medicamentului, reprogramarea pacemakerului sau repozitionarea sondei
poate fi de ajutor la pacientii care iau blocanti de canale de sodiu
si care se prezinta cu cresterea pragului de defibrilare sau de
stimulare. (Nivel de
dovezi: C)
La
pacientii care iau blocanti de canale de sodiu si care se
prezinta cu flutter atrial cu conducere 1:1, retragerea agentului implicat
este recomandata. Daca medicamentul trebuie continuat, o
blocada aditionala a nodului AV cu diltiazem, verapamil, sau
betablocante sau ablatia flutterului atrial poate fi eficienta. (Nivel de dovezi: C)
Clasa IIb
Administrarea
unui betablocant si unui bolus de sodiu poate fi considerata la
pacientii ce iau blocanti de canale de sodiu daca tahicardia
devine mai frecventa sau mai dificil de convertit. (Nivel de dovezi: C)
13.6.4.1. Caracteristici
clinice
Aritmiile
produse de blocanti de canale de sodiu sunt incluse in tabelul 14.
Medicamentele antiaritmice sunt cele mai comune precipitante, desi
alti agenti, an special antidepresivele triciclice si
cocaina, pot produce unele din toxicitatile lor prin aceste
mecanisme. Medicamentele blocante de canale de sodiu cu rata scazuta de
disociatie tind sa genereze aceste efecte adverse mai frecvent;
acestea includ agenti cum ar fi flecainida, propafenona si chinidina
care (ca o consecinta a ratei scazute de disociatie) tind
sa prelungeasca durata QRS chiar la o frecventa
cardiaca normala si dozaj terapeutic.1033
In
trialuri clinice mari, medicamentele blocante de canal de sodiu cresc
mortalitatea in randul pacientilor aflati in convalescenta
dupa IM. Acest efect a fost cel mai bine demonstrat in CAST,967
dar directii similare au fost de asemenea vazute la mexiletina1034
si disopiramida.1035 Analiza bazei de date CAST a
indicat ca pacientii aflati la risc de ischemie
miocardica recurenta sunt susceptibili la MSC in timpul tratamentului
cu medicamente blocante de canal de sodiu.1036
Tabelul 14. Sindroame de aritmii induse de medicamente
si tratamentul lor
|
Medicamente
|
Clinic
|
Tratament
|
|
Digitala
|
Toxicitate cardiaca medie
(numai aritmii izolate)
Toxicitate severa:
aritmii ventriculare sustinute; bloc AV avansat; asistola
|
Anticorpi
antidigitala
Pacing
Dializa pentru
hiperpotasemie
|
|
Medicamente care
prelungesc QT
|
Torsada de varf: cateva
episoade, QT lung
Torsada de varf
recurenta
|
Sulfat de magneziu iv
Repletia potasiului
la 4.5-5mEq/l
Pacing ventricular
Isoproterenol
|
|
Blocanti de canale
de sodiu
|
Necesitati
crescute pentru defibrilare sau pacing
Flutter atrial cu
conducere 1:1
Tahicardia
ventriculara ( mai frecvent; dificil de cardiovertit)
Sindrom Brugada
|
Oprirea medicamentului;
repozitionarea sondei
Diltiazem, verapamil,
betablocante
Betablocante; sodiu
Oprirea medicamentului;
tratamentul aritmiei
|
|
*Include intotdeauna recunoasterea
situatiei, monitorizarea continua, oprirea medicamentului,
restabilirea nivelurilor electrolitice normale (incluzand potasiul seric mai
mare de 4 mM/l) si oxigenoterapie. Ordinea nu este cea a secventei
preferate cand mai mult de un tratament este mentionat.
AV, atrioventricular; iv, intravenos.
|
La
pacientii tratati pentru TV sustinuta, acesti agenti
pot provoca episoade mai frecvente, si adesea mai dificil de convertit,
de TV sustinuta. In timp ce medicamentele in general incetinesc
frecventa TV, ocazional aritmia devine dezorganizata si poate
deveni rezistenta la cardioversie; decesul poate surveni. Se pare ca
cel putin o parte din excesul de mortalitate in CAST si alte trialuri
sunt reflectate de provocarea sau exacerbarea aritmiei ventriculare
sustinute. Medicamentele blocante de canale de sodiu cresc energia de defibrilare
si pragul pacingului,1037,1038 ca o consecinta,
pacientii pot necesita reprogramarea sau revizuirea pacingului sau
sistemelor ICD sau schimbari in regimul medicamentos. Blocantii de
canale de sodiu pot converti FA la flutter atrial cu frecventa scazuta,
care poate avea conducere AV 1:1 cu complex QRS larg. Aceasta aritmie
indusa de medicamente poate fi confundata cu TV.1039
Blocantii
de canale de sodiu pot ocazional precipita sindromul Brugada cu ECG tipic.1040
Acesta a fost raportat nu numai cu medicamente antiaritmice dar de asemenea
si cu antidepresivele triciclice1041 si cocaina.1042
Daca aceasta reprezinta demascarea indivizilor cu sindrom Brugada
inaparent clinic sau un aspect al spectrului larg de raspuns la
medicamentele blocante de canal de sodiu nu este cunoscut (vezi sectiunea
11.1.3.). Extinderea cu care sindromul Brugada latent a putut juca un rol in
rezultatele CAST este de asemenea necunoscut.
13.6.4.2. Tratament
Medicamentele
blocante de canale de sodiu nu ar trebui folosite la pacientii cu IM sau
TV sustinuta datorita bolilor cardiace structurale. Extinderea
cu care aceasta interzicere a blocantilor canalelor de sodiu la
pacientii cu boli cardiace structurale se refera si la
antidepresivele triciclice care sunt de asemenea blocanti de canale de
sodiu este necunoscuta.1043
Indicatia
majora pentru aceste medicamente sunt aritmiile atriale la pacientii
fara boli cardiace structurale; acestea exclud cel putin pe cei
studiati in CAST si pe considerente mecanice se extinde la cei cu
alte forme de disfunctii ventriculare. Cand sunt folositi pentru FA,
medicamente ce blocheaza nodul AV ar trebui considerate pentru a preveni
frecventa ventriculara rapida daca apare flutterul atrial;
amiodarona poate fi o exceptie. Pacientii care se prezinta cu
flutter atrial si frecventa rapida (si la care TV nu
se ia an considerare) ar trebui tratati prin incetinirea conducerii
AV cu medicamente cum ar fi diltiazemul intravenos. Ablatia flutterului
atrial si continuarea medicatiei antiaritmice poate fi o optiune
de terapie pe termen lung.1044
Observatii
clinice si pe animale sugereaza ca administrarea de sodiu, ca sodiu
clorid sau sodiu bicarbonat, poate fi eficienta in inversarea conducerii
incetinite si in TV frecventa sau rezistenta la cardioversie.1045,1046
Betablocantele au fost de asemenea folosite cu succes.1047
13.6.5. Supradozajul cu
antidepresive triciclice
13.6.5.1. Caracteristici
clinice
Antidepresivele
triciclice sunt dupa analgezice cea mai importanta cauza de
toxicitate prin supradozaj. Manifestarile tipice cardiace includ
tahicardia sinusala, alungirea PR si QRS, si ocazional un
sindrom ECG Brugada-like.1041 Hipotensiunea, febra, si coma
sunt alte manifestari comune de toxicitate. Torsada de varf a fost
asociata cu folosirea antidepresivelor triciclice, dar aceasta pare a fi
foarte rara.
13.6.5.2. Tratament
Durata
QRS poate fi scurtata in experimente pe animale si la oameni prin
administrarea de NaHCO3, sau NaCl bolus.1048 Medicamentele
antiaritmice, incluzand betablocantele, sunt in general evitate. Masurile
suportive, cum ar fi agentii presori, circulatia extracorporeala pot
fi necesare.
13.6.6. Moartea
cardiaca subita si bolile psihiatrice sau neurologice
Incidenta
MSC este crescuta la pacientii cu convulsii1049 si
schizofrenie. Nu este sigur daca acestea reflecta anomalii specifice,
cum ar fi disfunctii autonome sau o prevalenta neobisnuit de
mare a bolilor cardiovasculare, sau terapiile folosite in tratarea acestor
boli.1049-1052
Interactiunile
medicamentoase pot de asemenea contribui.1053 Agentii
antipsihotici cunoscuti a produce alungirea QT si torsada de varfuri
includ tioridazina si haloperidolul. Alt grup de medicamente antipsihotice
noi de asemenea alungesc intervalul QT, dar putine cazuri de torsada
au fost raportate. Nu se cunoaste daca acestea reflecta
diferente intrinseci intre medicamentele care produc o alungire
pronuntata a QT si cele care induc intr-un grad mai mic
alungirea QT sau reflecta diferente in expunerea pacientului la
medicamente noi fata de cele vechi.238,1054
13.6.7. Alte toxicitati
medicamentoase
Recomandari
Clasa I
Dozele
mari intermitente si dozele cumulative care depasesc nivelurile
recomandate ar trebui evitate la pacientii care primesc antracicline ca
doxorubicina. (Nivel de dovezi: B)
Toti
pacientii care primesc 5-fluorouracil trebuie supravegheati
indeaproape si administrarea trebuie intrerupta la primul semn sau
simptom de ischemie miocardica. La acesti pacienti administrarea
ulterioara de 5-fluorouracil trebuie evitata. (Nivel de dovezi: C)
Pacientii
cu boala cardiaca trebuie evaluati complet, inclusiv
ecocardiografic, inainte de administrarea antraciclinelor ca doxorubicina,
si ar trebui urmariti periodic pe termen lung. (Nivel de dovezi:
C)
Cardiotoxicitatea
antraciclinelor este dependenta de doza, dozele mari intermitente
si dozele cumulative mari cresc riscul de cardiomiopatie si aritmii
letale.1055,1056 Factorii de risc includ varstele tinere, sexul
femeiesc si folosirea trastuzimabului.1055,1057-1059
Aceasta forma de cardiomiopatie poate aparea acut, imediat
dupa tratament, la cateva luni (asa-numita forma
subacuta), sau dupa mai multi ani.1056,1060-1066 Exista
o crestere a ectopiei ventriculare la pacientii care primesc
doxorubicina, in timpul infuziei, dar aceasta este foarte rar semnificativa.1067-1068
Unele studii au sugerat ca reducerea HRV, anomaliile SAECG, si
cresterea QTc pot fi indicatori ai cardiomiopatiei iminente si ai
instabilitatii electrice, dar acestea nu au fost dovedite.1066,1069,1070
Este necesara evaluarea intermitenta pe termen lung a
pacientilor si decompensarile cardiace trebuie tratate conventional.
Exista putine dovezi de reversibilitate a proceselor miopatice induse
de antraciclina.
Indiferent
de boala coronariana subiacenta, 5-fluorouracilul produce aritmii
letale si potential fatale in timpul infuziei, marea majoritate
producandu-se la prima administrare.1071 Monitorizarea
cardiaca in perioada de infuzie, mai ales la prima, este recomandata
la toti pacientii care primesc 5-fluorouracil. La aparitia
simptomelor de ischemie miocardica, cu sau fara semne ECG,
administrarea trebuie oprita imediat. Ischemia trebuie tratata
conventional cu anticoagulante, nitrati, calciu-blocante si
beta-blocante in functie de situatie.1071 Desi
cardiotoxicitatea sa este reversibila, 5-fluorouracilul
sensibilizeaza pacientii si ar trebui evitat.1071
Cesiul, cunoscut a produce torsada varfurilor la modele animale, a asociat o
frecventa mai mare a acesteia atunci cand a fost folosit ca terapie
antineoplazica alternativa.1072
Veninul
de broasca, un ingredient al unor medicamente traditionale
chinezesti, are o toxicitate asemanatoare clinic cu cea a
digoxinului, si la modele animale anticorpii digoxin-specifici sunt
eficienti in antagonizarea toxicitatii.1073 Alte
produse vegetale, inclusiv ceaiul de degetarita (Digitalis sp.), pot
produce efecte similare.1074,1075 Cocaina are atat
proprietati de blocare a canalelor lente de sodiu cat si de
prelungire a QT (prin blocarea Ikr). Aritmiile asociate cu ingestia
de cocaina includ tahicardii cu complex QRS larg, care sugereaza
blocarea canalelor de sodiu si raspund la perfuzia de sodiu, precum
si torsada varfurilor. Cocaina produce si alte complicatii
cardiovasculare care pot da aritmii, mai ales miocardita si spasmul
coronarian.
Suplimentele
de dieta care contin alcaloizi de secara (inclusiv ma huang)
nu mai sunt comercializate deoarece s-au asociat in unele cazuri cu o
toxicitate cardiovasculara severa si MSC.1076-1078 Mecanismul
nu este cunoscut dar poate implica stimularea simpatomimetica
directa, spamul coronarian, si/sau hipertensiunea severa la
pacientii susceptibili. Efedrina, componenta activa, este
prezenta si in unele droguri ilicite. Spasmul coronarian este
asociat cu multe alte medicamente si se poate manifesta prin
fibrilatie ventriculara: anumite medicamente antineoplazice
(5-fluorouracil1079-1082), capecitabina,1083 triptani
folositi in terapia migrenelor,1084 agenti
recreationali (ecstasy1085, cocaina), administrarea
intempestiva de catecolamine vasopresoare, anafilaxia datorata unei
mari varietati de medicamente (vezi Sectiunea 7.5 pentru alte
discutii).
Bradiaritmiile
sunt efecte farmacologice comune (si dorite) ale digoxinului,
verapamilului, diltiazemului si beta-blocantelor. Bradiaritmiile severe
pot apare la doze obisnuite la pacientii sensibilizati, mai ales
daca primesc combinatii, sau in cazul supradozajului accidental ori
in scop suicidal. Bradicardia sinusala severa este un efect frecvent al
clonidinei.
14. Concluzii
MSC continua
sa fie o cauza majora de mortalitate in tarile
dezvoltate. Folosind o abordare bazata pe dovezi, acest document
incearca sa sumarizeze cele mai noi informatii referitoare la
acest subiect, cu scopul de a furniza recomandari consecvente precedentelor
versiuni. Este important sa subliniem ca domeniul evolueaza
continuu si ca recomandarile se vor schimba cu
siguranta, in functie de datele aflate. Lista bibliografica
lunga este si un indicator al vastei cercetari care abordeaza
MSC, si este indubitabil ca aceasta lista va creste in
viitor. Aducerea la zi periodica a acestor informatii este
vitala pentru medicii care ingrijesc pacienti cu risc de MSC.1021,1025
Acronime si abrevieri
IECA, inhibitori ai enzimei de
conversie a
angiotensinei
ACLS, advanced cardiac life support
suport vital avansat
SCA, sindroame coronariene acute
DAE, defobrilator automat extern
FA, fibrilatie atriala
IMA, infarct miocardic acut
AMIOVERT, Amiodarone Versus Implantable
Cardioverter-Defibrillator
CAVD, arrhythmogenic right ventricular
cardiomyopathy cardiomiopatia aritmogena de ventricul drept
AV, atrioventricular -
atrioventricular
AVID, Antiarrhythmics Versus Implantable
Defibrillators
BEST-ICD, Beta-Blocker Strategy plus
Implantable Cardioverter Defibrillator
CABG Patch Trial, Coronary Artery Bypass Graft
Patch Trial
CASH, Cardiac Arrest Study Hamburg
CAST, Cardiac Arrhythmia Suppression Trial
CAT, Cardiomyopathy Trial
BCI, coronary heart disease,
boala cardiac ischemica
CPVT, catecholaminergic polymorphic
ventricular tachycardia tahicardia ventriculara polimorfa
catecolaminergica
CT, computed tomography tomografie
computerizata
CMD, cardiomiopatie dilatativa
DEFINITE, Defibrillators in Nonischemic
Cardiomyopathy Treatment Evaluation
DIAMOND, Danish Investigators of Arrhythmia
and Mortality on Dofetilide
FE, fractia de ejectie
EF, electrofiziologic
CMH, cardiomiopatia hipertrofica
IC, insuficienta cardiaca
HRV, heart rate variability
variabilitatea ritmului cardiac
ICD, implantable
cardioverter-defibrillator defibrilator-cardioverter implantabil
LIFE, Losartan Intervention for Endpoint
Reduction in Hypertension
VS, ventricular ventricul stang
FEVS, fractia de ejectie a
ventriculului stang
LVOT, left ventricular outflow tract
tractul de ejectie al ventriculului stang
LQTS, long QT syndrome sindrom de QT
lung
MADIT II, Multicenter Automatic Defibrillator
Implantation Trial II MI , myocardial infarction infarct miocardic
RMN, rezonanta magnetica
nucleara
MUSTT, Multicenter UnSustained Tachycardia
Trial
NRMI-2, Second National Registry of
Myocardial Infarction
NSTEMI, non, ST-elevation myocardial
infarction infarct miocardic fara supradenivelare de ST
TVNS, tahicardie ventriculara
nesustinuta
NYHA, New York Heart Association
HTAP, hipertensiune arteriala
pulmonara
BPV, premature ventricular complex
bataie prematura ventriculara
BRD, right bundle-branch block bloc
de ramura dreapta
RF, radiofrequency -
radiofrecventa
RV, ventricular ventricul drept
RVOT, right ventricular outflow tract
tract de ejectie al ventriculului drept
SAECG, signal-averaged electrocardiography
electrocardiografie de inalta rezolutie
MSC, moarte subita cardiaca
SCD-HeFT, Sudden Cardiac Death in Heart Failure
Trial
SCN5A, cardiac sodium channel gene
gena canalului de sodiu din cord
SIDS, sudden infant death syndrome
sindromul de moarte subita a nou-nascutului
SNP, single nucleotide polymorphism
polimorfism mono-nucleotid
SOLVD, Studies Of Left Ventricular
Dysfunction
SPECT, single-photon emission computed
tomography tomografie prin emisie de pozitroni SVT, supraventricular
tachycardia tahicardie supraventriculara
SWORD, Survival With Oral D-sotalol
TWA, T-wave altemans
alternanta de unda T
FV, fibrilatie ventriculara
TV, tahicardie ventriculara
TSV, tahicardie supraventriculara
TORV, torsada varfurilor
WADA, World antidoping agency
WPW, Wolff-Parkinson-White




