DEFINITII BAC
ANORGANICA
ELEMENT CHIMIC - specia de atomi cu acelasi numar atomic Z
deci cu aceeasi sarcina nucleara.
IZOTOP - specia de atomi cu acelasi numar atomic Z dar cu A diferit
(numar de neutroni diferit).
izotopii hidrogenului : protiu (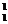 H) , deuteriu (
H) , deuteriu (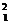 H) si tritiu (
H) si tritiu (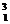 H)
H)
M element = %iz1 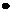 Aiz 1 + %iz2
Aiz 1 + %iz2
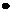 Aiz2 + . . . .
Aiz2 + . . . .
MOL DE ATOMI - cantitatea in grame dintr-un
element numeric egala cu masa atomica.
In A (masa atomica) grame din
orice element se gasesc un numar fix de atomi egal cu numarul
lui Avogadro 6,022 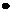
A g element . . . . . . . ..6,022 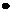 1023 atomi . . . . . . ..1 mol de atomi
1023 atomi . . . . . . ..1 mol de atomi
NUMAR DE MASA (A) - este suma dintre
numarul de protoni (Z) si numarul de neutroni (n) pe care ii
contine in nucleu. A = Z + n
NUMAR ATOMIC (Z) - numarul protonilor din nucleu.
Z = numar atomic = nr p+ = nr. e- = sarcina
nucleara = numar de ordine
ORDINEA COMPLETARII CU ELECTRONI
1s22s22p63s23p64s23d104p65s24d105p66s24f145d106p67s25f146d107p6
Fiecare orbital
atomic poate fi acupat cu max. 2 electroni de spin
opus.
SOLUTIE
SATURATA - solutia care contine o cantitate
maxima de substanta dizolvata
SOLUTIE NESATURATA - solutia care mai poate dizolva noi
cantitati de substanta
pana la saturatie.
SOLUTIE
DILUATA - solutia care contine o cantitate
mica de substanta dizolvata.
SOLUTIE CONCENTRATA - solutia care contine o
cantitate mare de substanta dizolvata.
SOLUTIA - amestecul omogen de doua sau mai
multe substante obtinut in urma procesului de dizolvare
CRISTALOHIDRATI - cristalele care inglobeaza in
structura lor apa.
DIZOLVAT
- substanta care se dizolva (solvat, dizolvat)
DIZOLVANT
- substanta in care are loc dizolvarea (solvent)
SOLUBILITATE - proprietatea unei substante de a se dizolva in alta
substanta
CONCENTRATIA SOLUTIEI - cantitatea de substanta
dizolvata intr-o anumita cantitate de solutie
CONCENTRATIA PROCENTUALA- cantitatea de substanta
dizolvata intr-o 100 g de solutie
C
= 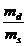
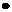 100 ms = md + mapa
100 ms = md + mapa
CONCENTRATIA MOLARA - numarul de moli de
substanta dizolvata intr-un litru de solutie.
CM = 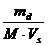 =
= 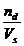
VOLUM MOLAR - Volumul unui mol
de gaz masurat in conditii normate de temperatura si presiune (OoC
si 1 atm). Vm = 22,4 L
/ mol
DENSITATE ABSOLUTA - rapotul dintre masa molara a
gazului si volumul molar
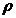 =
= 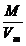
NUMAR DE COORDINARE - numarul ionilor de semn contrar
care inconjoara un ion .
LEGATURA IONICA - se stabileste intre ionii cu
sarcini electrice de semn contrar, intre care se exercita forte de
atractie electrostatica suficient de puternice, pentru a-i
mentine intr-un compus chimic.
LEGATURA COVALENTA - se realizeaza prin punere in comun de
electroni intre atomi de nemetal identici sau diferiti.
LEGATURILE COVALENTE NEPOLARE - se stabilesc intre atomi identici de
nemetale (apartinand aceluiasi element chimic) si sunt
rezultatul punerii in comun de electroni necuplati din stratul de
valenta.
LEGATURILE COVALENTE POLARE - se stabilesc intre atomi diferiti
de nemetale si sunt rezultatul punerii in comun de electroni
necuplati din stratul de valenta.
REACTII IREVERSIBILE - reactiile chimice care , in anumite conditii de lucru, se
desfasoara numai intr-un singur sens (numai cu formare de
produsi de reactie)
REACTII REVERSIBILE - reactiile chimice care , in anumite conditii de lucru, se
desfasoara in ambele sensuri pana cand
concentratiile substantelor ajung la anumite valori, care
caracterizeaza starea de echilibru.
ACID
- substanta care in solutie apoasa are
proprietatea de a ceda protoni (H+)
BAZA
- substanta care in solutie apoasa are
proprietatea de a accepta protoni (H+)
ACIZI
SLABI- acizii care ionizeaza numai partial,
astfel incat in solutie coexista molecule de acid cu ionii
proveniti din ionizare
BAZE SLABE - bazele care nu
ionizeaza complet in solutie apoasa, astefel incat
genereaza o concetratie de ioni HO- mai mica decat a
bazei dizolvate.
ACIZI
TARI - acizii care ionizeaza complet in
solutie apoasa astfel incat se transforma total in anioni
hidratati si pun in libertate ioni hidroniu H3O+
in concentratie egala cu a acidului introdus in solutie.
[H3O+]
= cacid tare
BAZE
TARI - bazele care ionizeaza complet in
solutie apoasa astfel incat se transforma total in cationi
hidratati si pun in libertate ioni hidroxid HO- in concentratie
egala cu a bazei introduse in solutie.
[HO-]
= cbaze tari
pH-ul este numeric egal cu logaritmul zecimal cu semn
schimbat din concentratia ionilor hidroniu, [H3O+] (pH = - lg[H3O+] )
[H3O+]
= 10-pH si [HO-] = 10-pOH
OXIDARE
- procesul chimic in care un atom
cedeaza electroni
REDUCERE
- procesul chimic in care un atom
accepta electroni
AGENT OXIDANT -
specia chimica care accepta electroni, reducandu-se.
AGENT
REDUCATOR - specia chimica care cedeaza
electroni, oxidandu-se
CELULA
ELECTROCHIMICA - dispozitivul in care energia
chimica este transformata in energie
electrica
ANOD
(-)- electrodul la care are loc
procesul de oxidare
CATOD
(+)- electrodul la care are loc
procesul de reducere.
REACTII EXOTERME - reactii
care au loc cu degajarea unei cantitati de caldura
REACTII
ENDOTERME - reactii
care au loc cu absorbtia unei cantitati de caldura
NUMAR DE
OXIDARE - este un numar
care reprezinta sarcina pe care el ar putea sa o aiba teoretic,
intr-un compus, electronii fiind atribuiti atomilor din compus
OXID ACID - oxizii nemetalici care
in reactie cu apa formeaza acizii
corespunzatori
OXID BAZIC - oxizii metalici care in
reactie cu apa formeaza bazele
corespunzatoare
acid +
fenolftaleina= incolor
acid +
turnesol = rosu
baza
+ fenolftaleina = rosu carmin
baza
+ turnesol = albastru
Caldura de reactie - cantitatea de caldura
absorbita sau degajata in reactii chimice
Caldura de combustie- efectul termic asociat unei reactii de ardere
completa a unui mol de substanta la presiune de 1 atm si
temperatura data.
Entalpia de reactie- caldura de reactie determinata la
presiune constanta.
Entalpia de formare standard - caldura degajata sau
absorbita , in reactia de sinteza a unui mol de substanta
din elementele componente, in conditii standard.
Lege lui Hess- intr-o reactie chimica, valoarea efectului
termic depinde numai de starea initiala a reactivilor si de cea
finala a produsilor de reactie si nu depinde de etapele
intermediare.
Reactii lente- au loc cu viteza mica intr-un interval
mare de timp.
Reactii rapide - au loc cu viteza mare intr-un interval mic de
timp.
Catalizatorul- substanta chimica care are rolul de a mari
viteza unei reactii chimice si care se regaseste
neschimbat, calitativ si cantitativ, la sfarsitul reactiei.
Catalizatorul
nu modifica randamentul si efectul termic al unei reactii.
Reactiile chimice au loc si in absenta catalizatorilor , dar cu
viteza mica.
Inhibitori- substante chimice care incetinesc sau
inhiba complet o reactie chimica.

