Enumerate tipurile de retele
cristaline Bravais,
precizand si parametrii celulei elementare
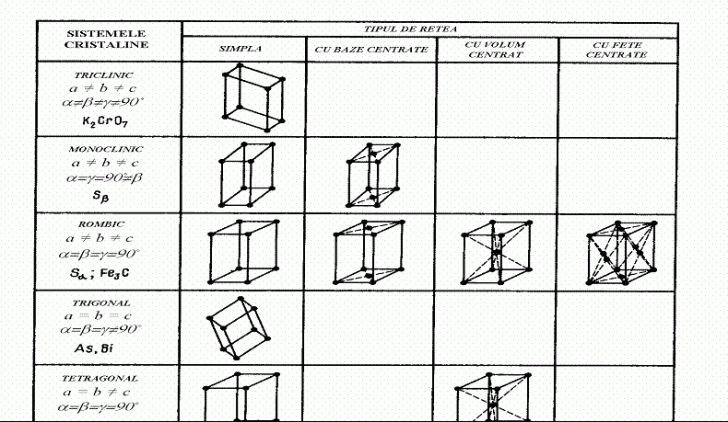
In cadrul cristalografiei sunt
stabilite 14 tipuri de celule elementare, care poarta denumirea de
retele spatiale Bravais.
Drept caracteristici ale celulei
elementare se indica sase marimi: trei laturi ale celulei a, b,
c si cele trei unghiuri delimitate de acestea α, β, γ . Aceste
marimi se numesc parametrii celulei elementare.
Toate cele 14 retele Bravais
sunt distribuite dupa 7 sisteme cristaline, corespunzator orientarii
si marimilor relative ale parametrilor fiecarei retele,
conform figurii 9. Fiecare sistem cristalin include unul sau mai multe tipuri
de retele cristaline spatiale. Pozitia oricarui nod din
reteaua cristalina se stabileste in functie de pozitia
originii celulei elementare prin coordonatele x, y, z.
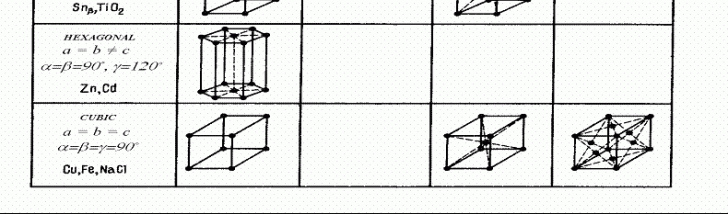
Descrieti reteaua cristalina CVC( sau CFC, CS), precizand
parametrii retelei cristaline, schita celulei elementare, numarul de noduri pe
celula-N
Structura cubica cu volum
centrat -
A2, CVC are mai putini atomi decat structura cubica cu fete
centrate. Atomii in reteaua CVC sunt dispusi in varfurile si in
centrul celulei elementare, conform figurii 14, a. Fiecare atom din aceasta retea are
opt vecini, dispusi la distante egale cu a 3 / 2 (= 0,866 a),
unde a este lungimea laturii
cubului celulei elementare. Deci numarul de coordinatie al acestei
retele este 8. Cea de a doua sfera de coordinatie (vecinii de
ordinul doi) contine sase atomi, dispusi la distanta a.
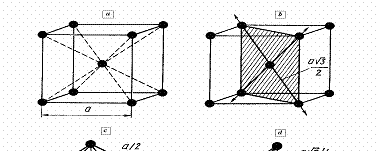
Figura 14 - Reteaua cubica
cu volum centrat: a - celula elementara; b - planele de maxima
densitate in atomi ; c - interstitii octaedrice; d - interstitii
tetraedrice
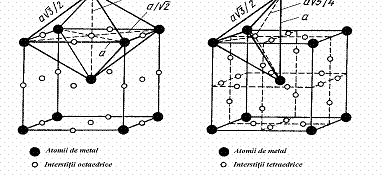
In structura cubic cu volum centrat
exista de asemenea doua tipuri de interstitii. Cele mai mari, de
tip octaedric, sunt dispuse pe fetele celulei elementare (figura 14, d)
si sunt inconjurate de 4 atomi ai retelei CVC dispusi in
varfurile unui tetraedru regulat. Interstitiile mai mici - de tip
tetraedric - sunt inconjurate de 6 atomi ce ocupa varfurile unui octaedru
neregulat (figura 14, c).
Daca structura CVC este
formata din sfere dure compacte, atunci in golurile tetraedrice se vor putea
introduce sfere de raza 0,291 r, iar in golurile octaedrice sfere cu raza
- 0,154 r, raze, ce sunt mai mici decat cele corespunzatoare retelei
CFC.
In reteaua cubica cu volum
centrat nu exista plane de maxima densitate in atomi similare cu cele
din reteaua cubica cu fete centrate. In cazul acesta sunt 12
plane (figura 14, b) cu maxima densitate in atomi. In aceste plane
sunt doua directii de maxima densitate in atomi, de-a lungul
carora atomii sunt tangentiali.
Gradul de compactitate al
retelei cubic cu volum centrat are valoarea de 68%, deci mai mica
decat cea a retelei cubic cu fete centrate (74 %).
Defecte
punctiforme de retea cristalina
Defectele
din cristale se clasifica, dupa cum
urmeaza, in:
defecte punctiforme
(zerodimensionale);
defecte liniare
(unidimensionale);
defecte de
suprafata (bidimensionale);
defecte de volum
(tridimensionale);
Defectele punctiforme sunt acele neregularitati ale retelei
cristaline comparabile dimensional cu
marimea unui atom. In cadrul defectelor punctiforme
intalnim urmatoarele tipuri (figura 17):
vacantele (noduri
ale retelei cristaline fara nici un atom)
atomi interstitiali (atomii
ce se afla interpusi intre nodurile retelei cristaline)
atomi de impuritate de substitutie (atom de impuritate, ce substituie un atom al metalului de baza)
atomi de impuritate interstitial (atom de impuritate dispus in interstitiile
retelei cristaline)
Figura 17 - Schema defectelor punctiforme intr-un cristal: 1
- vacanta; 2 - atom interstitial;
3 - atom de
impuritate de substitutie; 4 - atom de impuritate interstitial;
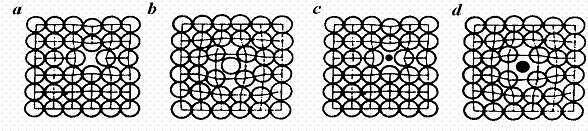
La trecerea unui atom din starea de
echilibru (din nod) in pozitie interstitiala, i-a nastere o
pereche "vacanta - atom interstitial", care se numeste 'defect
Frankel'. Daca atomul dintr-un nod iese
la suprafata cristalului, atunci se formeaza un 'defect
Schottky'.
Defectele punctiforme
reprezinta centri locali de distorsionare a retelei cristaline, cu
dimensiuni de ordinul a cateva diametre atomice. Desi necesita o
anumita cantitate de energie pentru formarea lor, aceste defecte se
afla in echilibru din punct de vedere termodinamic, cu alte cuvinte ele
exista intotdeauna intr-un cristal. Aceasta se explica prin faptul
ca defectele punctiforme cresc entropia sistemului.
Energia de formare a unei
vacante este de ordinul a 1 eV, iar energia de formare a unui atom
interstitial este de ordinul a ~ 3 eV, fapt explicabil prin aceea ca
un atom interstitial duce la o distorsionare mai accentuata a
retelei decat o vacanta.
Concentratia de defecte
punctiforme poate fi marita prin: iradiere cu particule elementare de
energie inalta, prin deformare plastica, sau prin calire de la
temperaturi inalte (racire ultrarapida), ce 'ingheata' concentratia de vacante de la temperaturi
ridicate.
Vacantele pot interactiona
intre ele formand perechi - bivacante - sau chiar aglomerari de
vacante.
Miscarea vacantelor in
cristal joaca un rol important intr-o serie de procese precum difuzia in
aliaje, alunecarea .
Ce este o
dislocatie intr-o retea cristalina?
Defectele
liniare dintr-un cristal se
caracterizeaza prin aceea ca dimensiunea lor transversala nu depaseste
cateva distante interatomice, pe cand lungimea lor poate atinge
dimensiunea intregului cristal.
Aceste defecte liniare se numesc dislocatii care pot fi marginale sau
elicoidale
(vezi figura 18).
Dislocatia marginala
reprezinta limita unui plan atomic incomplet (extraplan).
Dislocatia elicoidala rezulta
prin alunecarea unei regiuni dintr-un cristal fata de alta
regiune. Daca intr-o retea ideala se traseaza un contur (conturul Bürgers) in jurul unui punct arbitrar ales, cu stabilirea unui
anumit numar de parametri de retea in jurul acestui punct, atunci
conturul Bürgers se va inchide. Intr-o retea reala, conform figurii
19, care contine o dislocatie, conturul Bürgers nu se inchide,
diferenta reprezentand-o vectorul Bürgers Pentru
dislocatia marginala, vectorul Bürgers este perpendicular pe linia de
dislocatie, iar pentru dislocatia elicoidala vectorul este
paralel cu linia de dislocatie.
Figura
18 - Schema unei dislocatii marginale (a) si elicoidale (b) dintr-o
retea cristalina
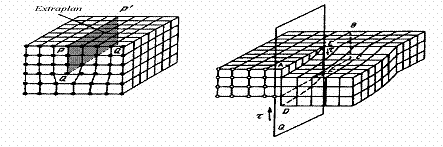
In cristalele reale se pot, de
asemenea, intalni si asa numitele dislocatii mixte, care au
unghiul intre
vectorii b si l arbitar (deci diferit de 0 sau de 90
Sub actiunea fortelor
exteriore, dislocatiile se deplaseaza (aluneca), realizandu-se
deformarea plastica a materialului. Deplasarea dislocatiilor in planul de
alunecare duce la ruperea si la formarea, ulterior, a unor noi
legaturi interatomice pe linia de dislocatie. Drept urmare,
deformarea plastica se poate realiza la tensiuni exterioare mici, mult mai
scazute decat cele necesare pentru deformarea plastica a unui cristal
ideal, care nu are dislocatii si in cadrul caruia este
necesara ruperea legaturilor interatomice pe intregul plan de
alunecare.
Deoarece deformarea plastica in
corpurile cristaline se realizeaza prin miscarea dislocatiilor,
un
metal se poate durifica prin blocarea alunecarii
acestor dislocatii.
Dislocatiile au o
influenta semnificativa nu numai asupra proprietatilor
de rezistenta si plasticitate
a metalelor, ci si asupra proprietatilor
fizice ale acestora, crescand rezistenta electrica, viteza de difuzie .
Ce sunt blocurile in mozaic?
Defectele
de suprafata dintr-o retea
cristalina prezinta dimensiuni mult mai mari pe doua axe de
coordonate, fata de dimensiunea de cateva
distante interatomice corespunzatoare celei de a treia axe de
coordonate. Dintre aceste defecte fac parte:
defectele de impachetare
maclele
limitele de graunte
suprafetele
exterioare ale cristalului.
Grauntii dintr-un
policristal nu sunt monolitici, monocristale perfecte, ci sunt compusi din
subgraunti
(blocuri in mozaic - figura 21), cu
un unghi de dezorientare intre ei foarte mic, de ordinul minutelor. Limitele de
subgraunte (sublimitele) si limitele de graunte din metale se
impart in limite la unghiuri mici (cand unghiul de dezorientare < 5 ) si limite
la unghiuri mari (> 5
Limitele
la unghiuri mici se intalnesc, de regula, intre
subgraunti si sunt formate fie din dislocatii marginale
paralele, fie din dislocatii elicoidale - limita rasucita. Structura
limitelor
la unghiuri mari este mult mai complicata. Figura
21 - Blocuri in mosaic

Limita
dintre graunti reprezinta o
zona de trecere foarte ingusta, cu grosimea de aproximativ 5-10
distante interatomice. Dispunerea dezordonata a
atomilor din aceasta zona se accentueazaprin acumularea de
dislocatii si de incluziuni.
Tensiunile datorate acumularii
de dislocatii la limita de graunte se transmit in grauntii
invecinati, fapt care duce la activarea in acestia a surselor de
formare de noi dislocatii.
Ca urmare a faptului ca limita
de graunte impiedica alunecarea dislocatiilor, reprezentand zone
de acumulari mari de incluziuni, acestea au o influenta
semnificativa asupra proprietatilor mecanice ale materialului
metalic.
Procesul de alunecare plastica
si, ca urmare, limita de curgere depinde de spatiul de alunecare al
dislocatiei pana la bariera, adica
pana la limita de graunte. Limita de curgere depinde de dimensiunea
de graunte
Cu cat este mai fina
granulatia, cu atat este mai mare limita de curgere si
rezistenta materialului. De
asemenea, plasticitatea si tenacitatea materialului vor
fi mai mari, cea de-a doua fiind deosebit de importanta pentru materialele
care lucreaza la temperaturi scazute. Valorile ridicate ale acestor
doua caracteristici sunt asigurate de o compozitie uniforma, de
o granulatie fina uniforma, de lipsa defectelor structurale care
pot provoca fisuri.
6.
Ce influenta au defectele de retea cristalina asupra
proprietatilor unui material metalic?
a.) Defectele punctiforme cresc entropia sistemului. Concentratia
de defecte punctiforme poate fi marita prin iradiere cu particule
elementare de energie inalta, prin deformare plastica, sau prin
calire de la temperaturi inalte (racire ultrarapida), ce 'ingheata' concentratia de vacante de la temperaturi
ridicate.
Vacantele pot interactiona
intre ele formand perechi - bivacante - sau chiar aglomerari de
vacante.
Miscarea vacantelor in
cristal joaca un rol important intr-o serie de procese precum difuzia in
aliaje, alunecarea
b.) Existenta dislocatiilor intr-un cristal
creaza in jurul acestora campuri de tensiuni sub actiunea carora
dislocatiile pot interactiona intre ele. Sub actiunea
fortelor exteriore, dislocatiile se deplaseaza (aluneca),
realizandu-se deformarea plastica a materialului. Deplasarea dislocatiilor
in planul de alunecare duce la ruperea si la formarea, ulterior, a unor
noi legaturi interatomice pe linia de dislocatie. Drept urmare,
deformarea plastica se poate realiza la tensiuni exterioare mici, mult mai
scazute decat cele necesare pentru deformarea plastica a unui cristal
ideal, care nu are dislocatii si in cadrul caruia este
necesara ruperea legaturilor interatomice pe intregul plan de
alunecare. Deoarece deformarea plastica in corpurile cristaline se
realizeaza prin miscarea dislocatiilor, un metal se poate
durifica prin blocarea alunecarii acestor dislocatii.
Dislocatiile au o
influenta semnificativa nu numai asupra proprietatilor
de rezistenta si plasticitate
a metalelor, ci si asupra proprietatilor
fizice ale acestora, crescand rezistenta electrica, viteza de
difuzie .
c.) Defecte de suprafata: -maclele
se formeaza printr-o reorientare simetrica a unor regiuni din
reteaua cristalina. Maclarea presupune rearanjarea pozitiilor
atomilor sub actiunea efectului aplicat, determinand reorientari
cristalografice mai favorabile deformarii plastice in continuare a
materialului metalic
- limita
de graunte impiedica alunecarea dislocatiilor, reprezentand
zone de acumulari mari de incluziuni, acestea au o influenta
semnificativa asupra proprietatilor mecanice ale materialului
metalic. Tensiunile datorate acumularii de dislocatii la limita de
graunte se transmit in grauntii invecinati, fapt care duce
la activarea in acestia a surselor de formare de noi dislocatii.
Procesul de alunecare plastica
si, ca urmare, limita de curgere depinde de spatiul de alunecare al
dislocatiei pana la bariera, adica
pana la limita de graunte. Limita de curgere depinde de dimensiunea
de graunte
Cu cat este mai fina
granulatia, cu atat este mai mare limita de curgere si
rezistenta materialului. De
asemenea, plasticitatea si tenacitatea materialului vor
fi mai mari, cea de-a doua fiind deosebit de importanta pentru materialele
care lucreaza la temperaturi scazute. Valorile ridicate ale acestor
doua caracteristici sunt asigurate de o compozitie uniforma, de
o granulatie fina uniforma, de lipsa defectelor structurale care
pot provoca fisuri.
d.) Defectele de volum (tridimensionale) sunt reprezentate de fisuri macroscopice,
pori, sufluri, formate in diferitele etape ale procesului tehnologic de
elaborare prin turnare sau de prelucrare a semifabricatelor. Este evident, in
acest caz, rolul negativ al acestor defecte.
Tipuri de faze in
sistemele de aliaje
Metalele pure au multe
utilizari in practica insa, cel mai adesea, in special cand sunt
necesare proprietati mecanice imbunatatite, sunt
folosite aliaje sau amestecurile de metale.
Aliajul
este un material metalic
obtinut prin amestecul unui metal cu alte metale sau metaloide. Aceste
amestecuri se realizeaza de cele mai multe ori prin
topire si solidificare. Totalitatea aliajelor alcatuite din
aceiasi componenti, insa in proportii
diferite, formeaza un sistem de aliaje. Exista doua tipuri de
aliaje: aliaje
cu o singura faza - monofazice si aliaje cu
faze multiple - plurifazice.
In materialele metalice pot apare
urmatoarele tipuri de faze solide:
I - metal pur
II - solutie solida
III - compus chimic
7.
Faza de metal pur
Faza metal pur este
alcatuita dintr-o singura specie de atomi, caracterizandu-se
printr-o retea cristalina
specifica. Curbele de racire ale metalului pur
prezinta palier la temperatura de solidificare si la temperaturile
transformarilor polimorfe. Metalul pur se
caracterizeaza prin conductibilitate electrica si termica
ridicata,
plasticitate mare si proprietati de
rezistenta scazute (duritate, limita de curgere,
rezistenta la rupere).
8.
Faza de solutie solida
In stare lichida, majoritatea
aliajelor metalice utilizate in tehnica formeaza topituri omogene,
adica solutii lichide. La trecerea in stare solida, in multe
astfel de aliaje se pastreaza omogenitatea, deci solubilitatea. Faza
solida ce se formeaza ca rezultat al cristalizarii unui asemenea
aliaj se numeste "solutie solida". Este plastica si putin dura.
Faza solutie solida este
formata dintr-un singur tip de cristale, toate avand acelasi tip de
retea cristalina. In plus, solutia solida poate exista
intr-un interval de concentratie a componentilor. Structura
solutiilor solide se formeaza ca urmare a penetrarii in
reteaua metalului de baza a aliajului (solventul) atomilor solubili.
Din punct de vedere al acestui fenomen, se disting doua cazuri diferite:
a) Solutii solide de substitutie
Solutiile solide de
substitutie pot avea solubilitatea limitata sau nelimitata. In
cazul solubilitatii nelimitate, reteaua cristalina a
componentului de baza, pe masura ce creste
concentratia componentului solubil, se transforma treptat in
reteaua cristalina a componentului solubil.
In solutiile solide cu
solubilitate limitata, concentratia elementului solubil este
posibila doar pana la o
anumita limita. Prin cresterea
ulterioara a acestei concentratii, solutia solida se
descompune, formand amestecuri bifazice. Variatia cu temperatura a
solubilitatii componentilor din solutia solida se
poate explica pe baza legilor termodinamicii. Curba de racire cu paliere in
dreptul temperaturii de solidificare in care atomii soloubili substituie atomii
de solvent din reteaua acestuia( daca distantele atomice sunt aproximativ
egale). Exemplu: solutia solida de substitutie Cu-Ni.
b) Solutii solide interstitiale
Solutiile
solide interstitiale se formeaza prin patrunderea atomilor
componentului solubil in interstitiile retelei
cristaline a componentului de baza (solventul). Acest lucru este posibil
daca atomii solubili sunt dimensional mult mai mici decat
atomii solventului, ca de exemplu atomii de H, C, N, B, cu diferente mari
de diametre atomice, de aproximativ 45 - 59%. Reteaua
cristalina a unei solutii solide interstitiale este aceea
corespunzatoare solventului, care este evident totdeauna elementul cu
diametrul mai mare. Prezenta atomilor dizolvati vor determina o
distorsionare a retelei cristaline si o usoara
crestere a parametrului retelei.
Exemplu: solutia solida
interstitiala Feα- C.
Hume
-Rofhery: " trebuiesc indeplinite 4 conditii pentru a exista solubilitate
nelimitata intre 2 sau mai multe elemente chimice:
-
izomorfism( ambele elemente sa cristalizeze in acelasi tip de retea cristalina;
Cu-Ni )
-
diferente minime de dimensiuni atomice
-
caracterul electrochimic sa fie aproximativ egal
-
concentratia electronic sa aiba valori clar definite.
9. Faza de compus chimic
Compusii chimici ce se pot
forma in aliajele metalice sunt foarte variati si prezinta
urmatoarele
caracteristici:- reteaua cristalina a
compusilor chimici este diferita de reteaua componentilor
ce formeaza compusii;
compusul chimic se
caracterizeaza intotdeauna printr-un raport exact al componentilor,
permitand
exprimarea compozitiei printr-o formula simpla de tip AnBm,
AmBnCp, etc (compus binar, ternar, etc). Din acest motiv, li se mai atribuie
denumirea de compusi definiti.
proprietatile compusului
chimic se deosebesc radical de proprietatile fiecarui component
in parte.
temperatura de topire a compusului
chimic este constanta.
formarea compusului chimic este
insotita de un efect termic considerabil.
Regula de formare a compusilor
definiti este cea a valentei imparte compusii chimici in:
- compusi cu valenta normala. Ex : elemetele chimice din grupele principale
Fe3C
- compusi cu valenta variabila. Ex : elemetele chimice din
grupele tranzitionale Cu5Zn8, CuZn
De regula, compusul chimic este
dur si fragil.
10. Care sunt caracteristicile structurale ale compusilor de
tip geometric
Compusii
de tip geometric se formeaza pe baza factorului geometric (diferenta
dintre razele atomice
ale componentilor). Din aceasta grupa fac
parte fazele Laves, fazele Sigma si fazele Hägg (sau compusi
interstitiali). Daca diferenta atomica
este mare, se formeaza compusii interstitiali. Daca
dimensiunile atomice
sunt relativ apropiate, se formeaza fazele Laves
si fazele Sigma.
a.) Compusi de tip substitutional. Au diametrele atomice aproximativ
egale.
Compusi tip Zintl. Raportul diametrelor celor 2 compusi este aproximativ egal
cu 1. Cristalizeaza frecvent in
CVC. Au valentele 1-1. Ex : CuZi
, LiCd
Compusi de tip Sigma se
formeaza intre metalele de tranzitie din grupele V si VI cu metalele
de tranzitie din grupele VII si VIII, daca diferentele
intre diametrele atomice nu sunt mai mari de 10 - 12%. Fazele Sigma sunt dure si fragile si
au conductibilitate electrica mare.
Dintre fazele Sigma se mentioneaza FeCr, FeV,
CoCr, CoMo,
MnCr, Mn2V.
Compusi de tip Laves - are
formula AB2 si se formeaza intre componenti de tip A si B intre
care sunt diferente atomice de pana la 20%. Atomii sunt cel mai compact
distribuiti. Fazele Laves au o retea cristalina de tip hexagonal compacta
(MgZn2 si MgNi2) sau de tip CFC (MgCu2).
Din familia de faze Laves fac parte AgBe2, CaAl2, TiBe2,
TiCr2 .
b.) Compusi de tip interstitial. Faza Hägg reprezinta
compusii formati intre metalele de tranzitie - M, cu raze
atomice mari (Fe, Mn, Cr, Mo, etc.), si nemetale - X cu raze atomice mici
(H, B, C, N).
Diferentele
dimensionale intre atomii constituent sunt foarte mari. Au formule chimice
diferite.
11. Principalul mecanism structural de deformare plastica la
rece
Pentru metale rezistenta la
intindere sau comprimare este mai mare decat cea de forfecare. De
aceea, procesul de deformare plastica reprezinta de
obicei un proces de alunecare a unei
zone de cristal
fata de alta, pe o suprafata
cristalografica sau un plan atomic de alunecare cu maxima densitate
de atomi,
unde rezistenta la forfecare este minima. Alunecarea
se realizeaza ca urmare a miscarii dislocatiilor in
cristal, proces care nu afecteaza arhitectura
cristalografica.
Capacitatea de
deformare plastica a unui material metalic creste odata cu cresterea numarului
de planuri atomice cu densitate atomica mare. Sistemul de cristalizare CFC este
cel mai usor deformabil plastic.
Prin alunecare
nu se modifica integritatea materialului( adica tipul de retea cristalina).
Atomii se deplaseaza cu un numar intreg de distante interatomice.
12.Efectele
deformarii plastice la rece asupra structurii
si
proprietatilor unui material metalic
La baza deformarii plastice
sta deplasarea ireversibila a unor zone din cristal fata de
alte zone.
Se schimba forma si dimensiunile
grauntilor( cristalelor) prin alpatizarea si lungirea lor pe direcita de
deformare plastic. Stuctura devine texturata si neuniforma.
Se scimba orientarea spatial a
grauntilor. Ei se rostesc si tind sa se aseze pe directii favorabile
alunecarii.
Se schimba structura fina( cea de la
nivelul retelei cristaline). Are loc fragmentarea grauntilor in blocuri in
mozaic. Are loc in plus si o crestere a numarului de defecte cristaline,
dislocatii in special, care duc la cresterea tensiunilor interne din cristal si
in final la crestera valorilor de rezistenta mecanica, duritate si scaderea
plasticitatii.
Datorita plasticitatii se
poate efectua prelucrarea metalelor prin deformare. Plasticitatea permite
redistribuirea uniforma a tensiunilor locale in intreg volumul de
material, fapt ce micsoreaza pericolul ruperii.
Alunecarea se realizeaza ca
urmare a miscarii dislocatiilor in cristal, proces care nu
afecteaza arhitectura cristalografica.
Ca si alunecarea, maclarea se realizeaza printr-o
deplasare atomica, dar de data aceasta deplasarea zonei de cristal are loc
intr-o pozitie corespunzatoare imaginii in oglinda a zonei
nedeplasate.
Cu cresterea gradului de deformare,
proprietatile mecanice ce caracterizeaza rezistenta la
deformare
cresc, are loc o durificare prin deformare, iar capacitatea de
deformare plastica scade. Limita de curgere creste mult mai
pronuntat decat rezistanta la rupere, insa, pe masura cresterii
gradului de deformare plastica, valorile celor doua caracteristici se
apropie. Ca urmare a ecruisarii,
proprietatile mecanice se modifica substantial: rezistenta
la rupere creste, iar alungirea relativa scade.
Durificarea prin ecruisare se
explica prin cresterea substantiala a densitatii
de dislocatii ca urmare a
procesului de deformare plastica. Densitatea de
dislocatii dupa deformarea la rece creste cu cateva ordine
de marime fata de densitatea de dislocatii a
unui material recopt.
In acelasi timp, in procesul de
deformare plastica, are loc cresterea defectelor punctiforme -
vacante si atomi interstitiali. Odata cu cresterea
densitatii de dislocatii si in general a defectelor
retelei cristaline, se
ingreuneaza libera circulatie a dislocatiilor. Se
formeaza bariere suplimentare ca urmare a deformarii grauntilor
si a fragmentarii blocurilor in mozaic. Toti acesti factori
produc durificarea materialului prin ecruisare.
In acelasi timp, ca urmare a
deformarii plastice, se modifica si proprietatile
fizico-mecanice ale
materialului metalic. Materialul ecruisat are o densitate mai
mica, are o rezistenta electrica mai mare, are
o conductibilitate termica mai scazuta,
rezistenta la coroziune este mai scazuta. Materialele metalice
cu
retea CFC se durifica, in urma ecruisarii,
intr-un grad mult mai mare decat metalele cu retea CVC.
13.Ce reprezinta ecruisarea unui material metalic?
Ecruisarea.
Dupa inlaturarea sarcinii ce depaseste limita de
curgere, proba ramane deformata. Prin
repetarea
incarcarii probei creste limita de curgere a metalului si
scade capacitatea sa de deformare
plastica,
adica are loc durificarea materialului. Durificarea materialului sub
actiunea deformarii plastice se
numeste ecruisare.
Prin
deformare, grauntii isi schimba forma si orientarea,
formand o structura texturata cu o orientare
preferentiala
a cristalelor. Grauntii cu orientari diferite se rotesc si
se dispun cu axele de maxima densitate
in atomi de-a lungul
directiei de deformare. Astfel, grauntii se deformeaza
si se aplatiseaza alungindu-se
pe directia de
actiune a fortelor P, si formand o structura texturata
.
Orientarea
cristalografica preferentiala a grauntilor de-a lungul
directiei de deformare se numeste textura
materialului. Cu cat
este mai mare gradul de deformare, cu atat un numar mai mare de
graunti vor obtine
o orientare
preferentiala. Formarea texturii faciliteaza aparitia
anizotropiei proprietatilor pe directia
longitudinala
si transversala a orientarii fibroase.
Cu
cresterea gradului de deformare, proprietatile mecanice ce
caracterizeaza rezistenta la deformare
cresc, are loc o
durificare prin deformare, iar capacitatea de deformare plastica scade . Limita
de curgere creste mult mai pronuntat decat rezistanta la rupere,
insa, pe masura cresterii gradului de deformare plastica,
valorile celor doua caracteristici se apropie.
Durificarea
prin ecruisare se explica prin cresterea substantiala a
densitatii de dislocatii ca urmare a
procesului de deformare
plastica. Densitatea de dislocatii dupa deformarea la rece
creste cu cateva ordine
de marime
fata de densitatea de dislocatii a unui material recopt.
In
acelasi timp, in procesul de deformare plastica, are loc
cresterea defectelor punctiforme - vacante si atomi interstitiali.
Odata cu cresterea densitatii de dislocatii si in
general a defectelor retelei cristaline, se
ingreuneaza libera
circulatie a dislocatiilor. Se formeaza bariere suplimentare ca
urmare a deformarii
grauntilor
si a fragmentarii blocurilor in mozaic. Toti acesti factori
produc durificarea materialului prin
ecruisare.
Ca
urmare a deformarii plastice, se modifica si
proprietatile fizico-mecanice ale materialului metalic. Materialul
ecruisat are o densitate mai mica, are o rezistenta
electrica mai mare, are o conductibilitate termica mai
scazuta, rezistenta la coroziune este mai scazuta.
Materialele metalice cu retea CFC se durifica, in urma
ecruisarii, intr-un grad mult mai mare decat metalele cu retea CVC.
14. Ce
este recristalizarea primara? In ce coditii se desfasoara?
De ce este
necesara ca tratament termic?
Procesul de recristalizare decurge in doua
stadii. Primul stadiu il reprezinta cel al "recristalizarii
primare", cel de-al doilea se numeste
"recristalizare cumulativa".
"Recristalizarea
primara" reprezinta procesul de formare de noi graunti
echiaxiali. Noii graunti se
formeaza la limita
blocurilor in mozaic sau a vechilor graunti, adica acolo unde
reteaua este cel mai puternic deformata prin ecruisare. Din punct de
vedere termodinamic, procesul de recristalizare primara este eficient
deoarece la trecerea metalului deformat intr-o stare mult mai stabila are
loc scaderea energiei libere. Ca urmare, in urma recristalizarii
primare ecruisarea metalului dispare, iar proprietatile se apropie de
cele corespunzatoare starii initiale. Densitatea de
dislocatii revine, de asemenea, la valoarea initiala.
Temperatura
de inceput de recristalizare se numeste "pragul de temperatura al
recristalizarii", sau
mai scurt "temperatura
de recristalizare". Aceasta depinde de temperatura de topire, conform legii enuntata
de A.A. Bocivar, astfel: Trecristalizare = a Ttopire, unde a - este un coeficient
ce depinde de compozitia si structura materialului metalic. Cauza
unei asemenea dependente este conditionata de faptul ca
ambele procese (topirea si recristalizarea) sunt legate de schimbarea
dispunerii reciproce a atomilor si pentru derularea acestora este nevoie
de o anumita mobilitate difuziva a atomilor.
Raportul
valorilor mobilitatii difuzive a celor doua procese este
aproximativ constant si ca urmare si
raportul temperaturilor
corespunzatoare celor doua procese este constant. In aliaje,
impuritatile interactioneaza cu dislocatiile limitand
mobilitatea acestora, fapt ce ingreuneaza formarea germenilor noilor
graunti franand astfel recristalizarea. De aceea, temperatura de
recristalizare a aliajelor este mai mare decat in cazul metalelor pure.
Cresterea
ulterioara a temperaturii duce la al 2-lea stadiu al procesului -
"recristalizarea
cumulativa", ce consta
in cresterea noilor graunti formati.
Dimensiunea
grauntilor formati in timpul procesului de recristalizare are o
influenta foarte mare
asupra
proprietatilor materialului metalic. Formarea grauntilor
mari scad proprietatile mecanice.
Daca
se impune inlaturarea totala a ecruisarii, recoacerea metalului
se realizeaza la temperaturi
mult mai mari decat
temperatura de recristalizare, pentru ca viteza de recoacere sa
decurga cu o viteza
eficienta.
Deformarea
plastica se poate realiza "la rece" sau "la cald". "Deformarea
plastica la rece" se
realizeaza la
temperaturi mai scazute decat temperatura de recristalizare si duce
la ecruisarea metalului.
15. Cum definiti ruperea
ductila a unui material metalic?
Ruperea
ductila are loc prin alunecare, sub actiunea tensiunilor
tangentiale. Suprafata de alunecare
este dispusa sub un
unghi de 45 fata de directia principalelor
tensiuni normale.
Ruperea
ductila pura, prin alunecare are loc pentru materiale amorfe precum
argila. Dar, majoritatea materialelor prezinta o rupere atat fragila,
cat si ductila, distinctia pe cele doua tipuri
facandu-se in functie de preponderenta unuia sau altuia.
Caracteristica
principala a unei ruperi ductile sau fragile este capacitatea
energetica a materialului, adica valoarea lucrului mecanic de rupere,
tipul fisurii si al suprafetei de rupere, viteza de propagare a fisurii.
In
cazul ruperii ductile se consuma un lucru mecanic mult mai mare. Pentru
propagarea ruperii ductile este necesar un aport exterior continuu de energie,
consumata cu deformarea plastica a metalului in zona din fata
fisurii ce se propaga. Astfel, lucrul mecanic consumat cu deformarea
plastica este considerabil mai mare decat cel de rupere propriu-zisa.
In
cazul ruperii ductile fisura are un unghi mare de deschidere (fisura
tesita), suprafata de rupere fiind caracterizata de o
puternica deformare plastica.
In
cazul ruperii ductile, suprafata de rupere are un aspect mat si
valurit, fara luciu metalic.
Viteza
de propagare a unei fisuri ductile este mult mai mica si se stabileste
in functie de viteza de crestere a tensiunilor interne.
In
cazul ruperii ductile este necesara cresterea rezistentei
materialului pentru luarea masurilor de prevenire ale ruperii.
16. Cum definiti ruperea fragila a unui material metalic?
Ruperea
fragila pura are loc pentru materiale elastice ideale, cum este de
exemplu diamantul.
Ruperea
fragila are loc prin rupere prin forfecare, cand suprafata de rupere
este perpendiculara la componenta normala a tensiunii. Pentru ruperea
fragila, unghiul de deschidere al fisurii este ascutit (fisura
ascutita), iar deformarea plastica in jurul suprafetei de
rupere lipseste aproape integral. Microfisura are un aspect neted si
stralucitor, dat de suprafetele rupte ale grauntilor
cristalini.
Pentru
a preveni ruperea fragila trebuie crescuta plasticitatea
materialului, la nevoie chiar scazand rezistenta acestuia. Cea mai
periculoasa ramane totusi ruperea fragila.
Sub actiunea tensiunilor normale are loc
deformarea elastica a retelei cristaline, iar dupa atingerea
valorilor maxime are loc
ruperea legaturilor interatomice cu desprinderea unei suprafete
atomice de alta, adica ruperea metalului.
Pentru
ruperea fragila, viteza de propagare a fisurii este foarte mare, de
ordinul a 0,4 din viteza de
propagare a sunetului in
metal. De aici rezulta ca viteza de propagare a unei fisuri fragile
in cazul unui
otel trebuie
sa fie ~ 2 x 103 m/s.
Prin
ruperea fragila se consuma o valoare mult mai mica a lucrului
mecanic pentru procesul propriu-zis de rupere decat in cazul ruperii ductile.
Ruperea fragila, odata initiata, devine un proces ce se dezvolta
de la sine, pe baza eliberarii energiei elastice acumulate in sistem,
motiv pentru care pentru propagarea fisurii nu este necesar un aport
suplimentar de energie. Astfel, pentru ruperea fragila, consumul de
energie pentru formarea unor noi suprafete ca rezultat al deschiderii
fisurii, este mult mai mic decat eliberarea de energie elastica
acumulata anterior.
17. Fazele care se
formeaza in sistemul Fe-cem
Diagrama de stare Fe - cementita (starea
metastabila)
Diagrama
de stare a sistemului fier - cementita este aratata in figura 92.
Linia
ABCD este linia lichidus, iar linia AHJECF - linia solidus. Punctul A
corespunde
temperaturii de topire a
fierului (1536 C),
punctul D - temperaturii de topire a cementitei (1252 C).
Punctele N si G
corespund temperaturilor de transformare polimorfa a fierului.
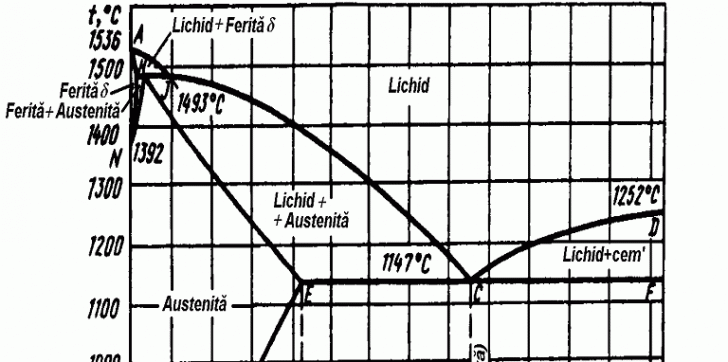
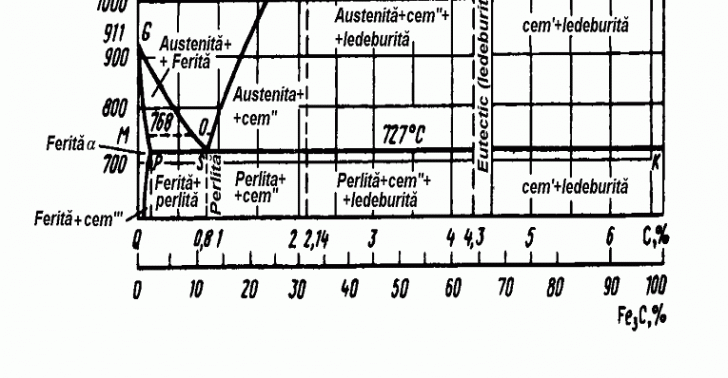
In
sistemul Fe - Fe 3C are loc o transformare eutectica si
una eutectoida. Dupa linia ECF, la 1147 C, are loc transformarea eutectica: LC AE cemF. Eutecticul format
se numeste ledeburita.
Ledeburita
(Led) -
eutecticul sistemului Fe - Fe3C - reprezinta amestecul mecanic
dintre austenita si cementita si contine 4,3 %C.
Dupa
linia PSK, la 727 C,
are loc transformarea eutectoida: AS Fp
cemK , in
urma careia din austenita cu continut de 0,8 %C se formeaza
amestecul mecanic eutectoid de ferita si cementita.
Transformarea
eutectoida este similara cristalizarii eutecticului, dar
eutectoidul nu se formeaza din lichid, ci dintr-o solutie
solida. Eutectoidul se numeste perlita. Perlita (P) -
eutectoidul sistemului Fe - Fe3 C
este amestecul mecanic
de ferita si cementita ce contine 0,8 %C.
Perlita este formata din
lamele de cementita intr-o masa de ferita si are o culoare
cenusiu - sidefie in proba atacata, de unde si denumirea de
perlita. Grauntele de perlita este format din lamele paralele de
cementita si ferita. Cu cat sunt mai mari cristalele de
cementita cu atat sunt mai slabe proprietatile mecanice ale
perlitei.
Austenita, ce intra in
componenta ledeburitei, sufera la 727 C o transformare
eutectoida. De aceea, sub 727 C
ledeburita este formata din amestec mecanic de perlita si
cementita.
Linia
PQ corespunde liniei de solubilitate variabila. Sub aceasta linie
aliajul este suprasaturat in carbon, are loc precipitarea carbonului in exces
care va forma un compus chimic cu fierul, adica cementita. La
racire, cementita se separa continuu, iar concentratia de carbon
in ferita scade conform liniei PQ, ajungand la temperatura camerei la 0,006
%. Cementita ce se separa din ferita se numeste cementita
tertiara - cem'''.
Variatia
dimensionala si de distributie a formatiunilor de
cementita influenteaza puternic proprietatile
aliajelor Fe - C.
La
temperaturi ridicate, din lichid se separa cementita primara - cem',
sub forma de cristale aciculare mari. Cementita secundara - cem'' -
se separa din austenita la temperaturi relativ ridicate si la viteze
mari de difuzie. De aceea cementita secundara se formeaza ca o
retea la limita grauntilor de austenita.
Cementita
tertiara - cem''' - se formeaza din ferita la temperaturi
scazute. Ea se separa de obicei in interiorul grauntilor de
ferita sub forma unor incluziuni disperse, care de altfel si cresc
duritatea feritei.
Aliajele
sistemului Fe - Fe3C se impart din punct de vedere structural in: oteluri
carbon si fonte
albe. Otelurile
carbon contin pana la 2,11 %C si isi incheie procesul de
solidificare prin formarea austenitei. Fontele albe contin mai mult de
2,11 %C si isi incheie solidificarea prin formarea eutecticului-
ledeburita.
Lipsa
ledeburitei din structura
otelurilor face ca plasticitatea acestora sa fie mai mare si
deci sa poata fi prelucrate prin deformare plastica. Pe de
alta parte, prezenta in structura fontelor a ledeburitei usor
fuzibile, face ca proprietatile de turnare ale acestora sa fie
considerabile.
18. Cum variaza
solubilitatea carbonului in fier odata cu cresterea temperaturii?
Fierul
este un
metal gri - argintiu, ce apartine grupei a VIII-a a sistemului periodic,
avand masa
atomica de 55,85,
densitatea de 7,86 g/cm3 si temperatura de topire de 1536 0C.
Fierul pur obtinut in conditii de laborator contine mai
putin de 0,0001 % impuritati, iar fierul de puritate
tehnica in jur de 0,1 -0,15% impuritati.
Fierul,
in stare solida, se poate afla in doua forme polimorfe: CVC (cubic cu
volum centrat) si CFC
(cubic cu fete
centrat). Conform schemei de variatie a energiei libere (figura 90)
rezulta ca in intervalul de
temperaturi 910 C cea mai mica energie libera si cea mai mare
stabilitate o are Fe γ cu retea cristalina
CFC.
Figura 90 - Schema
variatiei energiei libere a modificarilor polimorfe ale fierului cu
structura CVC si CFC.
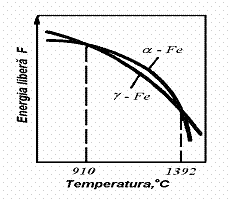
Sub
temperatura de 910 C si deasupra
temperaturii de 1392 C
este stabil Fe cu
retea CVC.
Modificarea
de temperatura inalta a fierului este denumita
uneori Fe δ deoarece este paramagnetica si
nu feromagnetica ca
Fe , desi din punct de
vedere cristalografic nu se deosebesc.
Curba
de racire inregistreaza doua transformari polimorfe si
una magnetica (figura 91).
Transformarea
magnetica de la 768 C
nu este legata de modificari ale retelei cristaline sau de
recristalizari, ci
de modificari ale straturilor electronice interioare si exterioare
ale atomilor care duc la
variatii ale
proprietatilor magnetice.
Figura 91 - Curba de
racire si incalzire a fierului
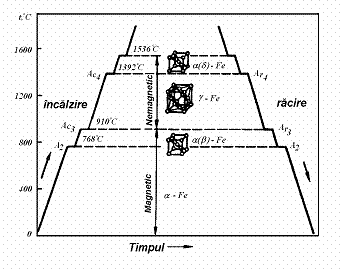
Carbonul
apartine
grupei a IV-a din sistemul periodic al elementelor. Carbonul se intalneste
in natura sub doua forme: diamant si grafit. Masa atomica a
carbonului este 12, densitatea grafitului de 2,25g/cm3 si temperatura de
topire de 3500 C.
Grafitul cristalizeaza in sistem hexagonal, este un material moale si
are o rezistenta scazuta. Rezistenta grafitului
creste odata cu cresterea temperaturii: la 20 C rezistenta Rm =
20 MPa, iar la 2500 C
grafitul este mai rezistent decat toate metalele refractare.
Carbonul
formeaza cu fierul solutii solide interstitiale. Solubilitatea
carbonului in fier depinde de forma sa cristalografica. Diametrul
interstitiilor retelei cristaline CVC este mult mai mic decat diametrul
interstitiilor din reteaua CFC. De aceea Fe este capabil sa
dizolve carbon in cantitati mici, in timp ce solubilitatea carbonului
in Fe este
mult mai mare.
In
sistemul Fe - C se pot intalni urmatoarele faze: faza lichida,
solutia solida pe baza de Fe (ferita),
solutia solida pe baza de Fe (austenita),
compusul chimic Fe3C (cementita) si grafit.
Ferita
(F)
este solutia solida interstitiala de carbon in Fe . La 727 C
solubilitatea carbonului in Fe
are valoarea
maxima, de 0,02 %; la 20 C
carbonul este solubil in Fe in
proportie de 0,006%. Proprietatile feritei sunt apropiate de
cele ale fierului pur.
Austenita
(A)
este solutia solida interstitiala de carbon in Fe . La 1147 C
austenita poate dizolva
2,11 %C, iar la 727 C - 0,8 %C.
Si
in ferita si in austenita se pot dizolva multe elemente de
aliere ce formeaza solutii solide de substitutie si care
modifica puternic proprietatile. In plus, alierea poate modifica
substantial temperature limitelor de existenta a acestor faze.
Cementita
(cem) -
carbura de fier Fe3C contine 6,67 %C. Temperatura de topire a cementitei
este de 1252 C, iar duritatea
acesteia este foarte mare, de 800 HB, putand zgaria cu usurinta
sticla. Cementita este foarte fragila, are o plasticitate aproape
nula, o retea ortorombica cu o impachetare densa a
atomilor.
La incalzire
cementita se dizolva conform urmatoarei reactii: Fe3C 3Fe Cgrafit
19. Ce este perlita in oteluri
Criteriile
de clasificare ale otelurilor aliate sunt: dupa structura in stare de
echilibru, dupa structura
obtinuta
dupa racirea in aer, dupa cantitatea de element de aliere
si dupa destinatie.
Dupa structura obtinuta dupa
racirea in aer
1. oteluri perlitice, cu un continut scazut de
elemente de aliere si stabilitate scazuta a austenitei subracite,
2. oteluri
martensitice, cu un continut mediu de elemente de aliere si
stabilitate ridicata a austenitei,
3. oteluri
austenitice, cu un continut ridicat de elemente de aliere si
structura austenitica la temperatura camerei.
Perlita este formata din
lamele de cementita intr-o masa de ferita si are o culoare
cenusiu - sidefie in proba atacata, de unde si denumirea de
perlita. Grauntele de perlita este format din lamele paralele de
cementita si
ferita. Cu cat sunt mai mari cristalele de cementita cu atat sunt mai
slabe proprietatile
mecanice ale perlitei.
20. Ce este
ledeburita?
Ledeburita (led) este amestecul
mecanic dintre austenite si cementita. Contine 4,3%C.
Dupa structura in stare de echilibru
1. hipoeutectoide,
cu ferita simpla in structura;
2. eutectoide, cu
structura perlitica,
3. hipereutectoide,
cu carburi in exces,
4. oteluri ledeburitice, in structura carora apar carburi primare, care au precipitat
din otelul lichid.
Acest
fenomen se explica prin faptul ca elementele de aliere
deplaseaza la stanga punctele S, E din
diagrama fier-carbon. De
aceea, limita dintre otelurile enumerate apare la concentratii mai
mici de carbon
fasa de
valorile din diagrama Fe-Fe3C.
Daca se pune in
discutie si faptul ca elementele de aliere micsoreaza
sau maresc domeniul , in
afara de grupele
enumerate mai sus se mai considera si urmatoarele doua:
5. oteluri
austenitice
6. oteluri
feritice
Otelurile carbon
simple pot fi numai din primele trei clase, iar cele aliate din toate cele
sase clase.
Ledeburita
(Led) -
eutecticul sistemului Fe - Fe3C - reprezinta amestecul mecanic
dintre
austenita si
cementita si contine 4,3 %C.
Dupa
linia PSK, la 727 C,
are loc transformarea eutectoida: AS Fp
cemK , in
urma careia din
austenita cu
continut de 0,8 %C se formeaza amestecul mecanic eutectoid de
ferita si cementita.
Transformarea
eutectoida este similara cristalizarii eutecticului, dar
eutectoidul nu se formeaza din lichid, ci dintr-o solutie
solida. Eutectoidul se numeste perlita. Perlita (P) -
eutectoidul sistemului Fe - Fe 3C -
este amestecul mecanic
de ferita si cementita ce contine 0,8 %C.
Lipsa
ledeburitei din structura
otelurilor face ca plasticitatea acestora sa fie mai mare si
deci sa
poata fi prelucrate
prin deformare plastica. Pe de alta parte, prezenta in structura
fontelor a ledeburitei
usor fuzibile, face
ca proprietatile de turnare ale acestora sa fie considerabile.












