STRUCTURA MATERIEI
Materia in univers se
gaseste sub doua forme de existenta:
substanta - care are o structura discontinua, discreta,
formata din microparticule din a caror asociere rezulta
corpurile, si se prezinta sub diferite stari de agregare:
gazoasa, lichida, solida si plasma;
camp - cu o structura continua prin
intermediul careia particulele de substanta interactioneaza
intre ele. Dupa natura lui campul poate fi: gravitational, electric,
magnetic, nuclear, biologic etc.
Materia vie este forma superioara de organizare a
materiei, fiind constituita din substanta cu structura
specifica, si camp biologic. Se caracterizeaza printr-o mare
heterogenitate si complexitate, precum si prin capacitatea de
a-si mentine structura, de a se reinnoi si adapta in
functie de conditiile mediului inconjurator.
1. Structura moleculara
Prin asocierea atomilor se
formeaza grupari stabile numite molecule, care pastreaza
proprietatile si compozitia procentuala a
substantei. Dimensiunea moleculelor este de ordinul 10-10 m in
cazul moleculelor mici, care sunt constituite dintr-un numar restrans de
atomi, si 10-7 - 10-6 m in cazul macromoleculelor care pot cuprinde peste 104
atomi. Organismele vii contin molecule mari (de exemplu, macromolecula de ADN are 108 - 109
atomi).
Structura si stabilitatea
moleculelor sunt determinate de interactiunile fizice ce se manifesta
intre particulele constituiente ale atomilor, precum si intre atomii
moleculei. Efectul imediat al interactiunilor dintre atomi sau grupuri de
atomi este formarea legaturilor chimice si dispunerea
spatiala a acestora.
In general, fortele interatomice
(intramoleculare) sunt de natura electrica, deoarece atomii sunt
formati din nuclee pozitive si electroni negativi, ceea ce
determina aparitia interactiunilor repulsive, respectiv
atractive. Expresia acestor forte electrostatice este data de legea lui
Coulomb:
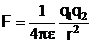 (1)
(1)
unde q1,
q2 sunt sarcinile electrice, r distanta dintre particule, iar e este
permitivitatea mediului.
1.1. Stabilitatea moleculelor
Se considera un ansamblu de doi
atomi aflati la distanta r unul de altul, cand fortele dintre
acestia pot fi predominant de atractie sau de repulsie, sau in
ansamblul lor sa se compenseze reciproc. In figura 1. este
reprezentata variatia cu distanta a energiei potentiale
datorata fortelor intramoleculare.
Energia potentiala
datorata fortelor de atractie este negativa, iar cea
datorata fortelor de respingere este pozitiva. Energia
potentiala totala este rezultanta celor doua energii (linia
punctata).
Cand distanta dintre cei doi
atomi este mare, practic fortele interatomice sunt nule, iar energia
ansamblului este data de suma energiei fiecarui atom. Cu
scaderea distantei incep sa se manifeste fortele de
atractie si de respingere, si cum variatia acestora este
diferita, la o anumita distanta, r0, cele
doua devin egale in modul. Aceasta configuratie corespunde
energiei potentiale minime a ansamblului de atomi, respectiv starii
stabile in care cei doi atomi formeaza o molecula.
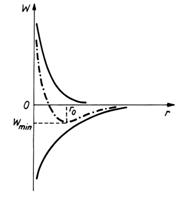
Fig.1. Energia potentiala datorata fortelor
intramoleculare.
Cand distanta dintre cei doi
atomi este mare, practic fortele interatomice sunt nule, iar energia
ansamblului este data de suma energiei fiecarui atom. Cu
scaderea distantei incep sa se manifeste fortele de
atractie si de respingere, si cum variatia acestora este
diferita, la o anumita distanta, r0, cele
doua devin egale in modul. Aceasta configuratie corespunde
energiei potentiale minime a ansamblului de atomi, respectiv starii
stabile in care cei doi atomi formeaza o molecula.
Daca molecula primeste o
energie mai mare decat energia potentiala minima Wmin,
egala cu energia gropii de potential, ea se desface in atomii
constituenti care se deplaseaza separat cu viteze determinate de
surplusul de energie. Energia minima necesara desfacerii moleculei se
numeste energie de
legatura Wleg, deci:
Wleg = - Wmin (2)
In concluzie, stabilitatea moleculei
se datoreaza fortelor interatomice (intramoleculare) si
corespunde energiei potentiale minime.
1. Dipoli electrici
O proprietate importanta a
moleculelor este distributia spatiala a sarcinilor electrice,
care explica unele interactiuni moleculare si comportarea
moleculelor in campurile de forte externe.
Moleculele, care din punct de vedere
electric sunt neutre, pot avea o structura spatiala
simetrica sau una asimetrica, in care centrul de greutate al
sarcinilor pozitive (nucleele) nu coincide cu centrul de greutate al sarcinilor
negative (electronii), ele fiind despartite spatial (Fig.). O
astfel de molecula se comporta la interactiunea cu un camp
exterior ca un dipol electric permanent, fiind caracterizat de un moment
dipolar permanent (m
m = q d (3)
unde q este
sarcina iar d distanta dintre centrele de greutate ale sarcinilor
electrice. Exemple de molecule ce se comporta ca un dipol permanent sunt
apa, amoniacul gazos, cetonele, esterii, aminele primare, urea etc.
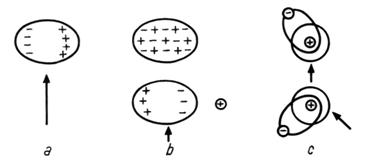
Fig. Dipoli electrici:
(a) permanent, (b) indus, (c) instantaneu.
Unele molecule cu o structura
simetrica pot deveni dipoli in prezenta unui camp electric exterior,
care separa centrele sarcinilor, inducand un moment dipolar:
m a E (4)
unde a reprezinta polarizabilitatea moleculei -
capacitatea de formare a norului electronic, iar E este intensitatea campului
electric extern. Acest tip de molecula este un dipol indus.
Exita
unele molecule unde repartitia asimetrica a sarcinilor electrice
rezulta datorita miscarii norului electronic,
obtinandu-se un dipol instantaneu, a carui orientare variaza in
timp, avand un moment dipolar doar intr-un interval de timp foarte scurt.
Majoritatea
moleculelor de natura biologica sunt molecule de tip dipol.
Legaturi intramoleculare si
intermoleculare
Studiile privind structura materiei
au condus la concluzia ca, in conditii normale, sub forma de
atomi liberi stabili exista numai gazele rare si metalele in stare de
vapori. Atomii celorlalte elemente se combina intre ei, dar mai ales cu
atomii altor elemente. Prin asocierea atomilor se degaja energie,
obtinandu-se molecule sau grupari moleculare de energie mai mica,dar
mai stabile decat daca ar ramane in stare libera.
Modul cum se formeaza o
molecula din atomi individuali se reflecta in legatura
chimica intramoleculara. Exista trei tipuri de legaturi: ionica,
covalenta, metalica.
Moleculele,
la randul lor, pot sa interactioneze intre ele, formand legaturi
intermoleculare si rezultand macromolecule. Aceste legaturi sunt: legatura
van der Waals si legatura (puntea) de hidrogen.
Din punct
de vedere energetic, legaturile intramoleculare sunt mai puternice, astfel legatura
ionica si cea covalenta au energia de legatura de
ordinul 10 - 102 kcal/mol. In schimb, legaturile
intermoleculare sunt mai slabe, dar au
rol esential in mentinerea structurii materiei vii si a
dinamicii ei.
Deci, la
baza oricarei legaturi stau interactiunile fizice, exprimate prin
diferite tipuri de forte, lucru valabil si pentru legaturile ce
formeaza moleculele biologice.
1.
Legatura van der Waals
Majoritatea substantelor organice si unele
combinatii anorganice ale nemetalelor formeaza asociatii
moleculare datorita existentei unor interactiuni fizice slabe
intre molecule sau grupari moleculare, care determina deformarea
orbitalilor atomici sau moleculari. Fortele van der Waals apar
datorita acestor deformari si se manifesta fie intre
molecule, fie intre parti ale unor molecule mari. In general, sunt
forte de natura electrica mai slabe, intensitatea
energetica este mai mica decat in cazul legaturilor ionice
si covalente, fiind de ordinul 1-2 kcal/mol.Forte van der Waals sunt proportionale
cu 1/ r4.
Legatura de hidrogen
Legatura de
hidrogen sau puntea de hidrogen este de natura electrostatica, fiind
o forma speciala a interactiunii dipol-dipol, dar mai
puternica decat legatura van der Waals, avand o energie de
legatura cuprinsa intre 4-7 kcal/mol.
Acest tip de legatura
se formeaza intre atomul H legat covalent de un atom puternic
electronegativ ca O sau N si un al doilea atom tot cu electronegativitate
ridicata. Este specifica apei, careia nu ii confera o
structura rigida, ci mai degraba o structura in echilibru
dinamic in care aceste punti de hidrogen se rup si se formeaza
permanent. Astfel se pot explica agregatele moleculare si
proprietatile speciale ale apei.
Puntile de
hidrogen au un rol important in stabilirea structurilor spatiale ale
biopolimerilor si in formarea dublei elice intre doua lanturi
complementare de ADN.
3.
Interactiunea hidrofoba
Dupa
interactiunea cu molecula de apa, unele substante imersate se
incadreaza in doua tipuri sau grupari moleculare:
hidrofile - care
interactioneaza cu apa. La dizolvarea lor se degaja o cantitate
mare de energie (DG < 0). Din categoria acestor substante fac parte
electrolitii si diferite grupari polare ale unor molecule, chiar
daca gruparea este legata de un rest molecular cu caracter apolar.
hidrofobe - care nu interactioneaza
cu apa. Energia eliberata la dizolvare nu este suficienta pentru
desfacerea structurii supramoleculare a apei. Astfel de substante sunt:
hidrocarburile saturate, catenele hidrocarburice din acizii grasi etc.
Caracterul hidrofob al unor substante este evaluat
prin variatia energiei libere Gibbs, in cazul dizolvarii lor intr-un
solvent apolar, respectiv polar, care este pozitiva (DG > Daca moleculele au o parte hidrofoba si una
hidrofila, cand sunt introduse in apa, isi orienteaza partile
hidrofile spre apa iar cele hidrofobe se grupeaza.
In concluzie, interactiunea hidrofoba
reprezinta tendinta moleculelor sau a agregatelor moleculare apolare
de a se grupa atunci cand sunt imersate in apa. Acest fapt se
constata des in cazul macromoleculelor biologice. Astfel,
interactiunea hidrofoba contribuie la formarea structurii
spatiale a proteinelor, la stabilirea dublei elice a ADN-ului si
chiar la structura supramoleculara a materiei vii.
Referitor la structura organismelor vii se pot face
urmatoarele observatii:
materia
organica din biosisteme este alcatuita, in principal, dintr-o
varietate foarte mare de biopolimeri, care au la baza structurala un
numar destul de restrans de monomeri.
componentii
macromoleculari au proprietati si functii specifice,
determinate de compozitia lor chimica, dar si de structura lor
spatiala.
interactiunile
moleculare din organismele vii au un grad ridicat de specificitate, determinat
de configuratia spatiala.
componentii
macromoleculari alcatuiesc complexe supramoleculare din care se
asambleaza organitele celulare, celulele, organele, tesuturile etc
pana la intregul organism.
toate procesele
si interactiunile ce au loc la diferite nivele de organizare ale
sistemelor vii se supun legilor fizicii si chimiei.



