TRANSPORTUL DE SUBSTANTA PRIN MEMBRANA CELULARA
1. Membrana celulara
Una din
caracteristicile importante ale biosistemelor este existenta unor limite
distincte, ce le separa de mediul inconjurator. Aceste limite,
reprezentate de membranele biologice, se intalnesc pana la nivel
subcelular.
Celula alcatuita din citoplasma
si organite celulare este inconjurata de membrana celulara
(membrana plasmatica), avand o grosime cuprinsa intre 50 - 100
Å. Prin urmare, membrana celulara este limita de separare intre mediul
intracelular si mediul extracelular reprezentat de lichidul
interstitial.
Lichidul
interstitial si citoplasma sunt sisteme disperse, in care mediul de
dispersie este apa, iar fazele dispersate sunt electrolitii (Na+,
K+, Cl-, Ca2+, Mg2+ etc), micromoleculele
si macromoleculele, in concentratii diferite. Per ansamblu, cele
doua lichide sunt izotonice, avand aceeasi osmolaritate ( 300 mosmol/l).
Compozitia,
structura si functiile membranei celulare au fost studiate
experimental prin difractie de raze X, microscopie electronica
si printr-o serie de metode termodinamice si electrochimice.
1.1.
Structura supramoleculara a membranei celulare
Prin metode de
analize fizico-chimice moderne s-a stabilit ca in compozitia membranelor
celulare se gasesc in principal lipide si proteine, la care se
adauga carbohidrati, ioni si apa
Modul de asamblare si configuratia
spatiala a componentelor membranare au determinat conceperea unor
modele de membrane celulare, care au satisfacut intr-o masura
mai mare sau mai mica proprietatile complexe ale membranei.
Astazi, pe baza datelor experimentale si a
cerintelor termodinamicii sistemelor macromoleculare, este acceptat pentru
structura supramoleculara a membranei celulare modelul de mozaic
fluid lipo-proteic, elaborat de Singer si Nicolson in 1972. Acest
model considera ca membrana celulara este formata dintr-un
strat bilipidic in care sunt inserate proteinele (Fig. 1).
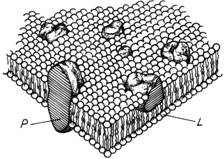
Fig.1. Modelul de membrana de mozaic fluid
lipo-proteic;
L - strat bilipidic; P - proteine membranare
Aranjarea structurala a membranei celulare este
determinata de interactiunile dintre componentele membranare si
mediul apos adiacent, ce pot fi de mai multe tipuri: hidrofobe, hidrofile,
punti de hidrogen, interactiuni electrostatice, in general
interactiuni necovalente. Dintre acestea, cele mai importante sunt
interactiunile hidrofile si hidrofobe, care asigura
conditia realizarii unei energii libere minime pentru sistemul
membrana-mediu apos.
Conform acestor considerente termodinamice,
rezulta ca reziduurile proteice nepolare ale aminoacizilor hidrofobi
impreuna cu lanturile de acizi grasi ale lipidelor se
orienteaza spre interiorul mozaicului fluid, pe cand cele polare
impreuna cu reziduurile polare ale zaharidelor se indreapta spre
mediul ionic apos intra- si/sau extracelular.
In general, proteinele, in functie de
caracterul lor hidrofob sau hidrofil, se pot lega de matricea stratului
bilipidic in diferite pozitii. Dupa modul de legare proteinele se
clasifica in:
proteine
intrinseci sau integrale ( in proportie de 70%) - care traverseaza o data sau de mai multe ori membrana pe
toata grosimea ei.
Partile
intramembranare sunt structuri hidrofobe, in dublu helix, legate intre ele in
mediul apos prin zone hidrofile
neelicoidale.
Proteinele intrinseci sunt implicate in
procesele de transport.
proteine extrinseci sau periferice
(in proprtie de 30%) - care se gasesc pe suprafata membranei sau
pot patrunde in ea pe o anumita grosime.
Proteinele
extrinseci pot interactiona cu suprafata bistratului lipidic prin legaturi
electrostatice. In general, la ele
predomina caracterul hidrofil, motiv pentru care sunt expuse atat spre
mediul extracelular, cat si spre cel intracelular, dar pot fi legate
si prin interactiuni hidrofobe, fara a patrunde prea
mult in stratul bilipidic. De asemenea, acestea pot interactiona cu alte
proteine membranare, formand complexe proteice. Proteinele extrinseci au un rol
important in transmiterea informatiilor spre interiorul celulei.
Date experimentale
au aratat ca interactiunile dintre lipide si proteine nu
sunt foarte puternice, cu toate ca ele au un rol important intr-o serie de
functii membranare. Deci, lipidele si proteinele se pot misca
relativ independent in planul membranar.
Aceasta
afirmatie este sustinuta de cel putin doua argumente.
Pe de o parte, faptul ca cele mai multe dintre lipide se gasesc sub
forma de bistrat, si numai cele de la extremitati, asa
numitele lipide de granita,
interactioneaza puternic cu proteinele membranare. Pe de alta
parte, la temperatura la care se desfasoara procesele vitale,
membrana celulara este fluida, prin urmare macromoleculele dispun de
mai multe grade de libertate.
Lipidele pot avea
miscari de translatie in stratul in care se afla,
miscari de rotatie in jurul propriei axe sau pot fi basculate
dintr-un strat lipidic in celalalt.
Proteinele pot efectua miscari
de translatie laterala prin bistrat si de rotatie in jurul
unei axe perpendiculare pe bistratul lipidic. Spre deosebire de lipide, care se
pot misca liber in bistrat, miscarea proteinelor este influentata
de interactiunile cu alte proteine. Aceste interactiuni sunt
importante in stabilirea proprietatilor si functiilor
membranelor. Astfel, pot determina legarea specifica a unei proteine
extrinseci de partea hidrofila a unei proteine intrinseci sau asocierea
mai multor proteine intrinseci pentru a forma un complex proteic specific
(agregat specific) in interiorul membranei, ca in cazul pompelor ionice.
Experimental s-a
constatat ca cele doua fete ale membranelor celulare difera
in compozitie, structura si functie, aceasta asimetrie
se datoreaza in special proteinelor. De exemplu, prin microscopie
electronica s-a observat dispunerea carbohidratilor din
compozitia glicoproteinelor numai pe fata externa a membranei.
Absenta lor pe fata interna demonstreaza ca
tranzitiile rotationale din exterior spre interior sunt nefavorabile
din punct de vedere energetic.
2. Transportul prin membrana
celulara
O celula vie, fiind un sistem termodinamic
deschis, are in permanenta schimburi de substanta cu mediul
extern. Aceste schimburi se realizeaza in ambele sensuri prin intermediul
unor mecanisme de transport prin membrana celulara.
Mecanismele de transport sunt diferite, fiind impuse
de natura substantei transferate, de tipul celulei si de aportul ei
energetic in schimbul de materie.
Transportul unor particule de dimensiuni mari (macromolecule, agregate
macromoleculare) se realizeaza prin distrugerea locala a
integritatii membranei celulare, ca de exemplu in cazul fenomenelor
de:
fagocitoza - care
reprezinta inglobarea unor particule solide de dimensiuni relativ mari,
prin emiterea de prelungiri protoplasmatice (pseudopode), si
pinocitoza - care este inglobarea de picaturi
microscopice de lichid extracelular, ce contine coloizi si
macromolecule, prin formarea unei vezicule sau a unui canal in membrana
prin care picatura trece in citoplasma.
In ambele fenomene, dupa transport, membrana se reface datorita
plasticitatii sale deosebite.
In cazul particulelor de
dimensiuni mici (micromolecule, atomi, ioni, molecule de apa, etc)
transferul de substanta are loc cu pastrarea
integritatii membranei celulare prin:
transport pasiv - care se realizeaza datorita
gradientilor de concentratie, de presiune, de potential
electric, in sensul lor, fara consum de energie. Depinde de structura
si proprietatile fizico-chimice ale membranei celulare si
are loc prin procese de difuzie si osmoza.
transport activ - ce are loc impotriva gradientilor
de concentratie, de potential electric sau presiune osmotica
si necesita consum de energie metabolica, care se obtine
din reactiile biochimice exergonice. Se realizeaza cu ajutorul
moleculelor transportoare, care au proprietati enzimatice.
In acest capitol se trateaza transferul de
substanta prin mecanisme de transport pasiv si activ.
2.1. Transportul pasiv
Transportul pasiv
este un proces de difuzie al moleculelor si ionilor prin membrana
celulara. Se realizeaza fara consum de energie
metabolica, in sensul gradientilor electrochimici sau de presiune.
Membrana
celulara avand o structura de bistrat lipidic, o particula
pentru a trece de pe o fata pe cealalta a membranei, trebuie
sa traverseze zone hidrofile si hidrofobe. Din acest motiv,
mecanismele de transport sunt diferite pentru particule hidrofile (ioni si
molecule polare) si particule hidrofobe (molecule nepolare), respectiv
pentru particule hidrosolubile si liposolubile. In functie de natura
particulelor transportul pasiv poate avea loc prin:
difuzie simpla prin stratul
bilipidic,
difuzie prin canale,
difuzie facilitata,
osmoza (in general pentru moleculele
de apa).
Transportul pasiv
are tendinta de a aduce sistemul celula-mediu extern in stare de
echilibru. Procesul inceteaza cand energia potentiala
totala are aceeasi valoare in cele doua compartimente extra-
si intracelular.
2.1.1. Difuzia simpla
Substantele ce traverseaza membrana
celulara prin difuzie trebuie sa fie solubile in lipidele care
alcatuiesc dublul strat membranar.
In general, solubilitatea unei substante este diferita in mediul apos
si in membrana lipidica fluida.
Se
numeste coeficient de partitie
solvent-apa (b raportul dintre solubilitatea intr-un solvent (in
acest caz membrana lipidica fluida) si solubilitatea in
apa.
In
cele doua compartimente extracelular si intracelular separate de
membrana se gasesc medii apoase: lichidul interstitial,
respectiv citoplasma, de concentratii diferite. La interfata
solutie-membrana apare cate un salt de concentratie, determinat
de coeficientul de partitie b 1. (Fig. 2.). Intre concentratia
membranei (Cm) si concentratia solutiei apoase ( C )
exista relatia:
Cm
= b C (1)
Tinand cont
de relatia (21) de definitie a coeficientului de permeabilitate (vezi
Legile lui Fick), permeabilitatea prin
membrana celulara devine:
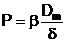 (2)
(2)
unde Dm - coeficientul de difuzie al membranei, iar d - grosimea membranei.
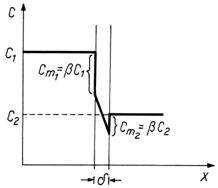
Fig. 2. Saltul
de concentratie la interfetele membranei
datorat coeficientului de partitie.
Se
poate constata ca permeabilitatea membranei celulare depinde de
caracteristicile particulei transferate (b) si de proprietatile
bistratului lipidic (Dm). Astfel, pentru ionii din mediul apos de
dimensiuni mici (r = 1 )
coeficientul de partitie este de ordinul b 10-60, deci permeabilitatea
membranei, tinand cont de relatia (2), este extrem de mica.
Macroionii nu pot difuza prin membrana, deoarece au dimensiuni mari
si sarcina electrica.
Moleculele
hidrofobe (nepolare) pot traversa membrana daca dimensiunile lor sunt mici
si se pot "dizolva" in matricea lipidica a membranei, cum sunt
alcoolii, acizii grasi, unele medicamente (exemplu penicilina etc).
In
concluzie, membrana celulara este o bariera selectiva pentru
ionii anorganici, macroionii organici, macromoleculele polare sau hidrofobe.
Prin difuzie simpla doar moleculele mici nepolare pot traversa membrana.
2.1.2.
Difuzia prin canale
Difuzia ionilor (Na+,
K+, Cl-, Ca2+, Mg2+ etc) prin
membrana are loc prin intermediul unor structuri proteice specializate, ce
strabat membrana pe toata grosimea ei, numite canale. In general, canalele permit trecerea ionilor in ambele
sensuri, directia lor de deplasare fiind determinata de gradientul
electrochimic.
Canalul ionic trebuie
considerat o structura cu proprietati de selectivitate si
functii complexe. Canalele ionice au caracteristici asemanatoare
cu cele ale enzimelor, cum ar fi: energie redusa de transport,
specificitate pentru un anumit ion, posibilitate de saturare la
concentratii mari, posibilitate de inhibare. Ele mediaza transportul pasiv al ionilor.
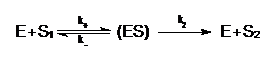 Transportul ionilor prin
canale poate fi descris formal printr-o cinetica
de tip Michaelis-Menten, specifica reactiilor enzimatice. Astfel,
canalul ionic poate fi considerat enzima E, care formeaza un complex (ES)
cu ionul ce trebuie transferat, el reprezentand substratul S:
Transportul ionilor prin
canale poate fi descris formal printr-o cinetica
de tip Michaelis-Menten, specifica reactiilor enzimatice. Astfel,
canalul ionic poate fi considerat enzima E, care formeaza un complex (ES)
cu ionul ce trebuie transferat, el reprezentand substratul S:
(3)
unde S1 si S2
reprezinta concentratia ionului in compartimentul extracelular,
respectiv intracelular.
Factorii
care influenteaza selectivitatea canalului ionic sunt urmatorii:
bariera energetica de legare a
ionului de canal, exprimata prin constanta de viteza k+;
bariera energetica de translocare a
ionului de pe o fata pe alta a membranei, exprimata prin
constanta de viteza k2 ;
concentratia de saturare a
canalului.
Eficacitatea de
transport a canalelor este foarte mare, astfel printr-un singur canal pot trece
106 - 108 ioni/s.
Canalele pentru
cationi sunt mult mai frecvente decat
cele pentru anioni. Astfel, canalele ionice pentru Na+, K+,
si Ca2+ sunt proteine cu masa de cca. 300.000 Da, existand
intre ele o similitudine: reduc bariera energetica cauzata de
interiorul nepolar al stratului bilipidic (de cca. 60 kcal/mol) prin realizarea
la nivelul stratului membranar a unei cai polare apoase. Deci, mediaza
difuzia cationilor (Fig. 3).
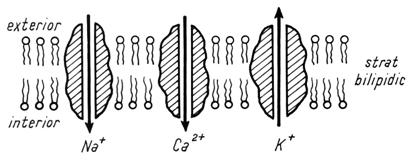
Fig.3. Canale ionice transmembranare.
Fluxul ionilor
Na+ si K+ prin membrana celulara se
realizeaza conform gradientului electrochimic: un influx pentru Na+
si un eflux pentru K+. Acesti doi ioni joaca rolul
cel mai important in stabilirea potentialului de repaus al membranei
si in transportul substantelor nutritive, respectiv al
produsilor de catabolism. Daca in anumite situatii
permeabilitatea membranei pentru acesti ioni se schimba, ei pot fi
utili ca traductori de semnale.
Concentratia
ionilor Ca2+ in mediul intracelular este mult mai mica decat in
cel extracelular, aceasta disproportie permitand celulei
utilizarea Ca2+ ca mesager in declansarea unor functii
fiziologice. Are un rol important in memtinerea contractilitatii
cardiace, in procesele de cuplare stimul-raspuns, in mentinerea
integritatii celulare.
Deschiderea sau
inchiderea canalului ionic se realizeaza printr-o modificare
conformationala a proteinei canal si se poate face:
electric, prin modificarea
potentialului de membrana (exemplu canalele de Na+ si
K+ din membrana axonala);
chimic, prin moleculele ce se leaga
specific la proteina canal (exemplu: canalul ionic de Na+ si Ca2+
din membrana celulei fotoreceptoare controlat de guanozinmonofosfatul ciclic
GMPc ,sau canalul de acetilcolina);
prin alte mecanisme (exemplu canale
sensibile la variatiile de presiune).
Selectivitatea
canalelor se realizeaza prin diferite mecanisme, de regula cunoscute.
Exceptie face canalul de Na+, al carui mod de
selectivitate nu este complet elucidat.
S-au descoperit
doua posibilitati de transport pasiv ionic, la care, spre
deosebire de canalele ionice selective, exista coordonari intre
diferiti ioni. Astfel, s-a
constatat ca pentru concentratii mici de ioni de calciu (maxim 1mmol/l in
mediu intracelular) exista un
canal de eflux de K+ deschis, numit canal de K+ activat
de Ca2+. De asemenea, exista un canal membranar numit
schimbator de Na+-Ca2+, care transporta
acesti ioni fara consum de energie (Fig.4.).
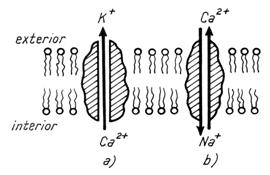
Fig.8.4. Mecanisme de transport ionic pasiv
a) canal de K+ activat deCa2+
b) schimbator Na+-Ca2+
In concluzie,
particulele incarcate (ioni) sunt transportati prin
membrana prin difuzie cu ajutorul
canalelor ionice, care din punct de vedere electric au o rezistenta
mica, respectiv o conductanta constanta, de ordinul 10-12
S (Siemens).
2.1.3.
Difuzia facilitata
Moleculele hidrofile mari, cum sunt majoritatea
factorilor nutritivi si anumiti ioni, nu pot trece nici matricea
lipidica si nici prin canalele ionice, nefiind liposolubile.
Transferul acestora de pe o fata pe cealalta a membranei poate
avea loc printr-un transport mediat de o molecula transportoare, proces
cunoscut sub numele de difuzie
facilitata.
Transportul de
substanta prin difuzie facilitata, desi are loc in sensul
gradientului electrochimic, se desfasoara cu viteze mai mari
decat valorile date de legile difuziei simple. De regula, molecula
transportoare este o proteina specifica cu rol enzimatic. Difuzia
facilitata poate fi descrisa tot pe baza cineticii Michaelis-Menten,
avand caracteristici comune cu cataliza enzimatica, cum ar fi:
fiecare proteina are un loc
specific de legare a substratului (molecula ce trebuie translocata);
viteza transportului este maxima
cand toate locurile de legare ale proteinei sunt ocupate;
difuzia depinde de pH;
exista o inhibitie
competitiva cu compusi similari si necompetitiva prin alte
substante.
Proteina transportoare se poate afla in doua stari
conformationale diferite, avand un loc de legare pe una din fetele
membranei.
Mecanismul transportului facilitat consta in crearea unei stari
legate intre proteina transportare P si molecula de transferat M, deci
formarea unui complex proteina-molecula. Modificarea
conformationala are drept rezultat transferul complexului pe
cealalta fata a membranei si eliberarea moleculei M (Fig.5.).
Viteza de reactie este proportionala cu concentratia
substratului, asadar transportul se desfasoara in sensul
gradientului chimic.
Acest tip de difuzie facilitata se
cunoaste si sub denumirea de mecanism ping-pong. Apare la transportul
glucozei, glicerolului, neelectrolitilor, ureei, aminoacizilor.

Fig. 5. Difuzia
facilitata: mecanism ping-pong. M - molecula transferata,
P1,P2 - proteina in starea conformationala 1,
respectiv 2.
Eficacitatea transportului mediat de o molecula
transportoare este mult mai mica decat a celei prin canale. De exemplu,
transportul de glucoza prin membrana eritrocitara mediaza
transferul a cca. 300 molecule/s.
Un caz particular al difuziei facilitate il
constituie transportul ionilor prin formarea in jurul lor a unor structuri
hidrofobe, care le permit difuzia prin stratul bilipidic. Se numeste ionofor o substanta, care
inclusa in membrana celulara, permite translocarea ionilor de pe o
fata pe cealalta.
Ionoforii mobili sau carausii sunt proteine, de regula
peptide ciclice, care au o zona polara capabila sa capteze
un ion. Mecanismul de transport (Fig.6.) poate fi imaginat ca un lant de
reactii:
S(1) + C(1) SC(1) SC(2) S(2) + C(2) (4)
unde: S - substratul (ionul de transportat)
C - proteina
caraus.
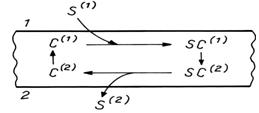
Fig. 6. Mecanism
de transport cu ionofori mobili.
Fluxul de ioni este pasiv,
transportul avand loc in sensul gradientului electrochimic.
Daca se
considera afinitatea substratului (ionului) fata de
proteina aceeasi pe ambele fete ale membranei si N un numar
cunoscut de proteine din membrana, in prima aproximatie,
lantul de reactii este determinat de miscarea proteinei de pe o
parte pe alta a membranei. Atunci, numarul de ioni transportati este:
dN/dt = - k N
(x1 - x2) (5)
unde: k - constanta de reactie
x1, x2
- fractiile de saturare ale proteinelor pe cele doua fete.
Se poate constata ca
transportul inceteaza cand substratul are aceeasi concentratie
in ambele compartimente despartite de membrana sau cand
fractiile de saturare ale proteinelor pe cele doua fete sunt
egale.
Ionoforii mobili au o
specificitate pentru un anumit ion, de exemplu: valomicina pentru K+,
gramicidina pentru Na+.
In ce priveste
transportul apei, respectiv al protonilor, se realizeaza atat prin difuzie
simpla, cat si prin pori aposi (canale). Din datele
experimentale s-a constatat ca permeabilitatea membranelor pentru apa
este mult mai mare decat ceea ce ar corespunde celor prezentate mai sus.
Mecanismele de transport al apei sunt mai complexe, un rol important avand
gradientul de presiune osmotica.
In concluzie, membrana
celulara poate fi traversata prin transport pasiv de molecule mici
hidrofobe prin difuzie simpla, de ioni prin canale sau difuzie
facilitata si de molecule hidrofobe mari prin difuzie facilitata.
Permeabilitatea membranei pentru o specie moleculara sau ionica
caracterizeaza capacitatea particulei respective de a traversa in mod
pasiv membrana, indiferent de mecanismul de transport.
2.2.
Transportul activ
Transportul
activ are loc impotriva gradientilor de concentratie, de
potential electric sau de presiune osmotica, necesitand consum de
energie metabolica. Din acest motiv, procesul este cuplat cu reactii
biochimice exergonice, donoare de energie libera.
2.2.1. Transportul activ primar
Transportul activ primar este determinat de
existenta unei distributii asimetrice a ionilor in cele doua compartimente extra- si intracelular
despartite de membrana celulara.
Substanta este
transferata de pe o fata pe cealalta a membranei celulare prin
intermediul unor molecule transportoare cu proprietati enzimatice.
Transportul activ este de
doua tipuri:
primar - realizat prin pompe ionice, fiind cuplat cu o
reactie producatoare de energie metabolica;
secundar - care este cuplat cu transportul simultan
al unei alte substante in sensul gradientilor.
Transportul activ este o caracteristica
fundamentala a materiei vii si permite adaptarea la conditiile
de mediu.
Se realizeaza prin intermediul unei proteine
transportoare cu rol enzimatic, care leaga ionul pe o parte a membranei
si suferind modificari conformationale il "pompeaza" pe
cealalta parte. Acest mecanism a primit denumirea generica de pompa ionica.
Reactia de transfer,
endergonica, este cuplata cu o reactie exergonica, de
obicei hidroliza ATP:
ATP + H2O ADP + Pi cu DG = -7,3 kcal/mol (6)
unde ATP - adenozintrifosfat, ADP - adenozindifosfat, Pi -
fosfat anorganic.
In functie de ionii
specifici translocati, in organismele vii exista mai multe tipuri de
pompe ionice.
a)
Pompa Na+/ K+.
Pompa ionica Na+/ K+
transporta ionul Na+ din mediul intracelular (i) spre mediul
extracelular (e) si ionul K+ din exterior spre interiorul
celulei, concentratiile celor doi ioni in mediile respective fiind [Na+]i
<< [Na+]e si [K+]i >> [K+]e. Deci, transferul ionilor se face in sens
invers gradientului electrochimic, necesitand consum de energie
metabolica.
Proteina transportoare cu rol enzimatic este ATP-aza specifica, ce are doua stari conformationale distincte: X
cu locuri de legare pe fata interna si Y cu locuri de legare pe
fata externa a membranei.
Mecanismul de functionare al pompei Na+/ K+ este
ilustrat in figura
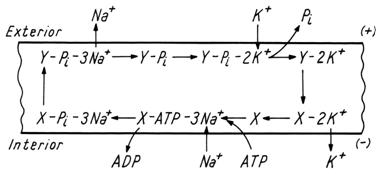
Fig.
Mecanismul pompei Na+/ K+.
Forma conformationala X leaga pe fata interna a
membranei ATP si ioni de sodiu, formand complexul X-ATP-3Na+. Legarea sodiului
determina hidroliza ATP, ceea ce duce la fosforilarea enzimei si
eliberarea de ADP. Enzima se transforma in forma Y, astfel ionii Na+
sunt transferati pe fata externa unde sunt eliberati.
Aceasta forma leaga ionii de potasiu formand complexul Y-Pi-2K+.
Legarea K+ determina defosforilarea enzimei si trecerea ei
in forma X, iar ionii K+ sunt translocati pe fata
interna a membranei. Astfel se inchide un ciclu in care sunt
transportati 3 ioni de sodiu spre lichidul interstitial si 2
ioni de potasiu spre mediul celular.
Pompa Na+/ K+ poate fi
inhibata de catre glicozidele cardiotonice (digitala si oubaina)
si de oligomicina, care impiedica eliberarea ionului Na+
din complexul enzimatic. De asemenea, ATP-aza Na+/ K+
specifica poate lega in locul fosfatului (Pi) vanadatul, care
care nu mai disociaza, blocand astfel pompa.
Stoechiometria pompei Na+/ K+ poate fi exprimata
prin reactia:
3(Na+)i + 2(K+)e +
ATP 3(Na+)e + 2(K+)i + ADP + Pi (7)
Se
constata ca la fiecare ciclu de functionare al pompei are loc un
transfer net de sarcina pozitiva (1Na+) spre exterior,
ceea ce determina polarizarea menbranei: pozitiv spre exterior si
negativ in interior.
In conditii fiziologice normale, tinand cont de numarul de
cicluri efectuate in unitatea de timp ( 175 cicluri/s) curentul
transmembranar creat de pompa este de ordinul 10-15 A.
Cunoscandu-se rezistenta membranei celulare de 1011 -1012
W, diferenta de potential este de ordinul mV sau chiar mai
mica are o contributie foarte mica la potentialul de repaus
al membranei.
2.2.2. Transportul activ secundar
Transportul activ
secundar reprezinta transportul unei substante impotriva gradientului
de concentratie, cuplat cu transportul altei substante in sensul
gradientului de concentratie, asigurat de un transport activ primar. Cele
doua substante sunt translocate de pe o fata pe alta a
membranei celulare de aceeasi proteina transportoare.
Prin
transportul activ secundar pot fi transferati aminoacizii, acizii mono- si dicarboxilici, acizii
biliari, glucidele, precum si diversi ioni de fosfat, sulfat,
bicarbonat, calciu.
Transportul
activ secundar este intalnit in tesuturile epiteliale, cum ar fi
tesutul intestinal si renal.
Transportul
activ secundar are un consum de energie metabolica mai redus decat
transportul activ pasiv, deoarece utilizeaza energia furnizata de
gradientul electrochimic mentinut de pompa ionica.
Din
punct de vedere al sensurilor fluxurilor de substanta, transportul
activ secundar este de doua tipuri: antiport si simport.
a)
Antiport (contratransport)
Antiportul transporta o substanta in
sensul gradientului ei electrochimic, mentinut prin transport activ primar
si o alta substanta in sens contrar gradientului ei. Acest
transport activ secundar este cunoscut si sub denumirea de contratransport.
Mecanismul de functionare al pompei antiport
este asemanator cu cel al pompei ionice, dar cu consum energetic
redus. Astfel, proteina transportoare (T), ce se poate transforma
conformational, leaga pe fata (1) a membranei o substanta
(S) pe care o transloca pe fata (2) a membranei, unde leaga o
alta substanta (P) transferand-o pe fata (1) a membranei
(Fig. 8).
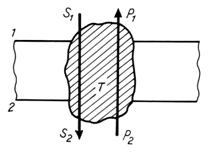
Fig. 8. Pompa
antiport - mecanism.
Viteza de transport depinde de concentratiile
celor doua substante pe fetele membranei unde sunt legate de
proteina, mai exact de produsul acestor concentratii.
In cazul unor coeficienti stoechiometrici ai
reactiei enzimatice egali cu unitatea (s=p=1), la echilibru, vitezele de
transport pe cele doua fete sunt egale:
S1 P2 = S2 P1 (8)
respectiv raportul concentratiilor este:
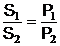 (9)
(9)
Generalizand, daca sunt transportati
s moli de substanta (S) si p moli de substanta (P),
raportul concentratiilor devine:
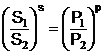
 (10)
(10)
Astfel, se constata ca raportul
concentratiilor substantelor transportate depinde de stoechiometria
reactiei enzimatice.
Un exemplu de
contratransport este antiportul Na+/Ca2+, care
asigura o concentratie scazuta de ioni de calciu in
interiorul celulelor tesutului muscular cardiac
b) Simport (cotransport)
Simportul asigura transportul a doua
substante in acelasi sens, din acest motiv este denumit si cotransport. Proteina transportoare
leaga pe aceeasi fata a membranei ambele substante,
una dintre ele fiind transferata in sensul gradientului de
concentratie, mentinut tot de transportul primar activ, si
cealalta in sens contrar gradientului (Fig. 9).
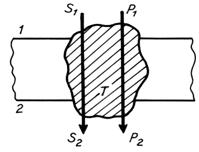
Fig. 9. Simport
- mecanism.
Viteza de transport este proportionala cu produsul dintre
concentratiile celor doua substante pe aceeasi
fata a membranei.
La echilibru, pentru o stoechiometrie de 1/1, vitezele de transport sunt
egale S1 P1 = S2 P2 , iar raportul concentratiilor este:
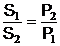 (11)
(11)
Pentru o stoechiometrie a reactiei enzimatice de s/p, raportul
concentratiilor este:
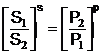 (12)
(12)
Exemplu de cotransport este simportul Na+/glucoza
care se gaseste in tesutul intestinal si cel renal.
In continuare este prezentat simportul Na+/glucoza utilizat
in elaborarea urinei. Concentratia de glucoza din urina pimara
este comparabila cu cea din sange. Ea este reasorbita total la
nivelul tubului urinar impreuna cu ionii de natriu, care sunt transportati
in sensul gradientului de concentratie, mentinut de pompa Na+/K+.
In tubul urinar se gasesc doua pompe simport Na+/glucoza:
una in regiunea proximala cu o stoechiometrie de 1/1 si cealalta
in zona distala cu o stoechiometrie de 1/2. Ele asigura
absorbtia totala a glucozei in patul vascular (Fig. 10.).
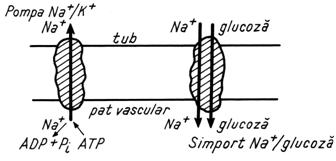
Fig. 10. Simportul Na+/glucoza la nivelul tubului urinar.
Glucoza este o molecula neutra, ionul Na+
transfera o sarcina pozitiva, astfel apare un potential
electrochimic, deci simportul Na+/glucoza este electrogenic.




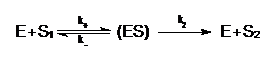






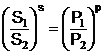

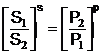 (12)
(12)