TIPURI DE STRUCTURI CRISTALINE CARACTERISTICE PIGMENTILOR OXIDICI
1.Pigmenti
oxidici cu structura corindon-hematitului
Structura corindon-hematitului prezentata
in figura 1, este formata din ioni de O2-, aranjati
hexagonal compact, compensati electrostatic de ionii de Al3+,
care ocupa simetric doua treimi din golurile octaedrice ale
retelei.Fiecare ion de Al3+ este inconjurat de 6 ioni de O2-
si fiecare ion de O2- de 4 ioni de Al3+.
Legaturile dintre atomi in aceste cristale au caracter partial
covalent.
Dintre pigmentii oxidici care
prezinta o astfel de structura cristalina se pot mentiona:
Cr2O3, (Al,Cr)2O3, Mn2O3,Fe2O3,etc.
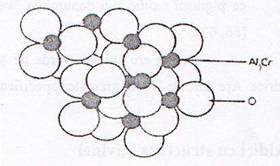
Fig.1. Structura corindon hematitului
2.Pigmenti oxidici cu structura
granatilor
Granatii sunt ortosilicati dublii cu formula generala : 3R"O∙R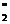 ∙3SiO2,in care R"=Ca, Mg, Fe, Mn,
Y, iar R'"= Fe, Al, Cr, Ti.
∙3SiO2,in care R"=Ca, Mg, Fe, Mn,
Y, iar R'"= Fe, Al, Cr, Ti.
Granatii fac parte din
categoria nesosilicatilor, al caror cation se prezinta in
coordinatie octaedrica si cubica.(fig. 2) [45].
Uvarovitul sau granatul
calci-cromic, Ca3Cr2[SiO4]3 sau
3CaO∙Cr2O3∙3SiO2, este utilizat ca
pigment oxidic sub denumirea "verde Victoria"[20,21].Acesta se prezinta in
cristale dodecaedrice.
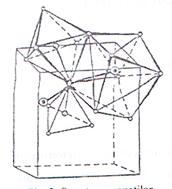
Fig.2.
Structura granatilor
3.Pigmenti oxidici cu structura olivinei
Sub denumirea de olivine sunt
cuprinsi cativa silicati ortorombici care reprezinta
solutii solide intre: Mg2SiO4(forsterit), Fe2SiO4
(fayalit), si Mn2SiO4 (tefroit).Olivina este un
compus izomorf intre forsterit si fayalit, formula chimica a acesteia
fiind (Mg,Fe)2SiO4.Structural, olivina este
considerata nesosilicat[46].
Structura cristalelor de
olivina este prezentata in
figura 3 [45].
Tetraedrii[SiO4],
apar izolati, legandu-se intre ei prin ionii de Mg si de Fe. Ionii de
oxigen formeaza in retea structuri cu aspect hexagonal.
Dintre pigmentii oxidici cu
structura olivinei se amintesc Co2SiO4 de culoare
rosie-violacee si Ni2SiO4 de culoare verde[22,23].
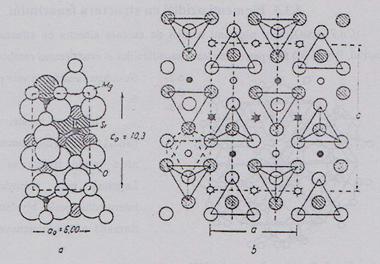
Fig.3.Structura
cristalelor de olivina
a)Proiectie cotata reprezentata prin
atomi; b)Distributia tetraedrilor[SiO4] in retea;
4.Pigmenti oxidici cu
structura periclazului
(Co,Ni)O sunt pigmenti oxidici de
culoare cenusie cu structura periclazului.
Acestia
prezinta o retea cubica cu fete centrate, ionii de Co2+,Ni2+
si O2- ocupand alternativ nodurile retelei(fig.4).
Intre ionii din retea se
exercita forte de legatura electrostatice care plecand de
la fiecare ion se raspandesc in toate directiile.
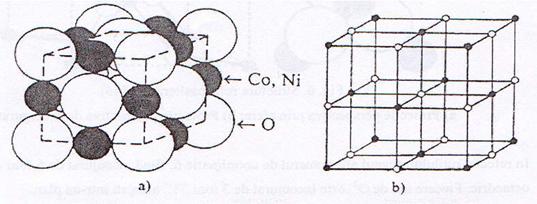
Fig.4.Structura periclazului
a)Proiectie perspectiva prin sfere; b)Proiectie
perspectiva de configuratie.
5.Pigmenti oxidici cu structura fenacitului
(Co,Zn)2SiO4
sunt pigmenti oxidici de culoare albastra, cu structura fenacitului[24].Fenacitul,
Be2[SiO4] face parte din clasa nesosilicatilor
si cristalizeaza romboedric-trigonal.
Structura fenacitului este
prezentata in figura 5. In aceasta structura, tetraedrii [SiO4]
nu au varfuri comune, ci sunt situati ca niste insule izolate in
edificiul cristalin. Legatura intre tetraedrii se face prin intermediul
ionilor bivalenti cu coordinatie 6, formand retele tridimensionale.
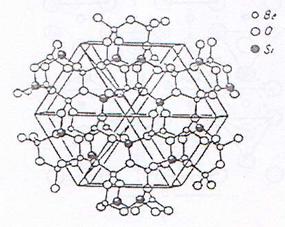
Fig.5. Structura fenacitului
6.Pigmenti
oxidici cu structura rutil-casiteritului
Rutilul cristalizeaza in sistem
tetragonal si este izotop cu casiteritul.
Structura rutil-casiteritului
prezentata in figura 6 este caracteristica unui mare numar de
pigmenti oxidici[18,25].
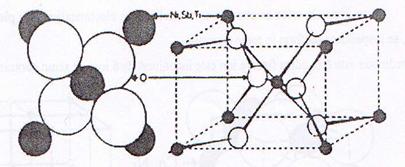
Fig.6.Structura
rutil-casiteritului.
a)Proiectie
perspectiva prin sfere; b)Proiectie perspectiva de
configuratie.
In reteaua rutilului,
titanul are numarul de coordinatie 6, fiind inconjurat de 6 ioni de O2-
aranjati octaedric. Fiecare ion de O2- este inconjurat de 3
ioni de Ti4+ aranjati intr-un plan.
7.Pigmenti oxidici cu
structura spinelica
In literatura sunt
indicati numerosi pigmenti oxidici [18] ce cristalizeaza
izomorf cu mineralul MgAl2O4 numit spinel.
Compozitia chimica a
compusilor cu structura spinelica [48-52] poate fi prezentata
prin formula AB2O4, unde A si B sunt cationi
metalici diferiti sau identici.Sarcina totala pozitiva pe un
cation A si doi cationi B trebuie sa fie de opt
unitati.Aceasta permite combinatii de valente: 2-3, 4-2
si 6-1(rar), prima cifra reprezentand valenta cationilor A iar a
doua cifra, valenta cationilor B.
Celula elementara a retelei
de tip spinel cuprinde opt unitati AB2O4 si
prezinta simetrie cubica. In celula elementara a spinelului
prezentata in figura 7 se gasesc 64 interstitii tetraedrice
si 32 octaedrice, din care numai 8 respectiv 16 sunt ocupate.
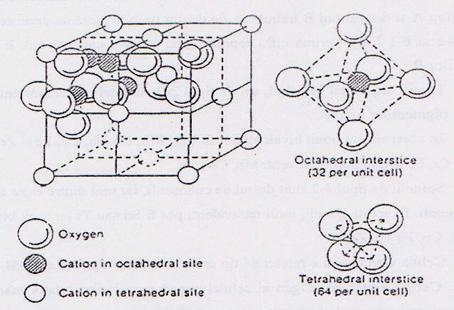
Fig.7.Celula
elementara a structurii spinelice
8.Pigmenti cu structura
zirconului
Silicatul de zirconiu sau zirconul
corespunde formulei ZrSiO4 sau ZrO2∙SiO2.
Zirconul cristalizeaza in sistemul tetragonal,avand parametri de
retea: a0 si
c0 5,94 Å [45] (figura 8).
In structura zirconului,
gruparile ionice [SiO4]4- sunt izolate,
fara nici un oxigen comun. In grupul ionic [SiO4], atomii
de oxigen sunt asezati in varfurile unui tetraedru regulat,iar
siliciul ocupa centrul tetraedrului.Legatura dintre tetraedri[SiO4]4-
se realizeaza prin intermediul cationilor Zr4+ [53].
In literatura sunt
indicati o serie de pigmenti oxidici cu structura zirconului[4,26-29],
larg utilizati in colorarea glazurilor si emailurilor datorita
stabilitatii lor la temperaturi inalte, in contact cu topiturile.
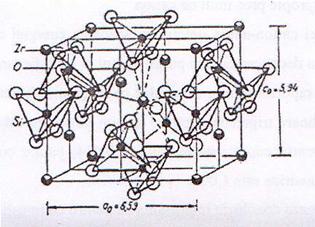
Fig.8.Celula
elementara a silicatului de zirconiu
9.Pigmenti oxidici cu
structura de sillenit
Structura sillenit este atribuita
unui grup de compusi formati de Bi2O3 cu
alti oxizi metalici si se caracterizeaza printr-o retea
cristalina cu celula elementara cubica centrata intern, a
carui parametru reticular a0 este cuprins intre 10,10 si
10,25Å.
Faza cu structura cubica centrata intern este semnalata
in diagramele de faze ale sistemelor Bi2O3-MeO2(Me4+=Si4+,
Ge4+, Ti4+) (figura 9)[56,57].
In literatura sunt prezentate date
referitoare la posibilitatea obtinerii unor pigmenti oxidici cu
structura sillenitului [19].
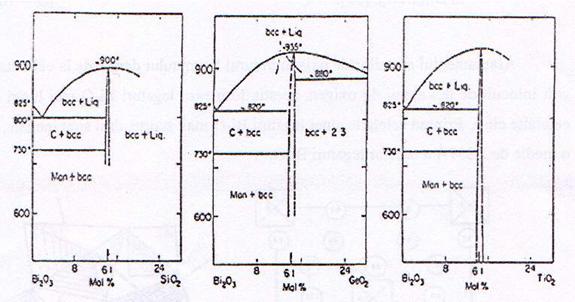
Fig.9.Diagramele de faze ale sistemelor Bi2O3-MeO2
10.Pigmenti oxidici cu
structura de perowskit
Structura perowskitului CaTiO3
se caracterizeaza prin coordinarile diferite ale diversilor
cationi.Structura este cubica.Ionul de Ca2+ situat in centrul
cubului este inconjurat de 12 ioni de oxigen asezati in mijlocul
laturilor unui cub, iar ionii de Ti4+ asezati in varfurile
cubului sunt inconjurati octadric de ionii de oxigen.
Aceasta structura se intalneste la BaTiO3, CaZrO3,
CaSnO3, YAlO3, LaGaO3,precum si la KMgF3,
KZnF3, CsCdCl3.
Structura relativ complexa a
perowskitilor se preteaza la o serie de substitutii izomorfe in
urma carora in reteaua cristalina pot fi inclusi
diversi ioni cromofori.
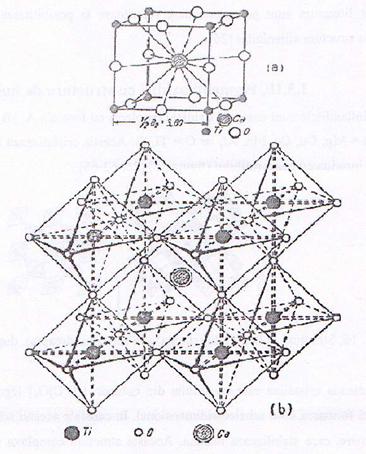
Fig 10.
Structura perowskitului:
a)
paralelipipedul elementar;
b)modul de coordonare a diferitilor ioni intre ei.
11.Pigmenti oxidici cu structura de hollandit
Hollanditele sunt compusi oxidici
complecsi cu formula A1-2B1-2C6-7O16
in care: A=Ba, K, Rb; B=Mg,Cu,Co,Mn,Al, iar C= Ti,Si.Acestia
cristalizeaza in sistem tetragonal avand structura inrudita cu cea a
rutilului (figura11) [19,62-65].
Reteaua cristalina este
constituita din octaedri[(B,C)O6] legati intre ei prin
muchii si colturi, cu formarea unui schelet tridimensional.In
canalele acestui schelet se gasesc cationii A, cu raza mare, care
stabilizeaza reteaua. Aceasta structura complexa se
preteaza foarte bine la elaborarea unor compozitii variate care pot
sta la baza unei game largi de pigmenti oxidici.
In literatura se arata
ca hollanditele in care C =Ti, pot sta la baza obtinerii unor
pigmenti stabili fata de emailuri si glazuri[19,30].
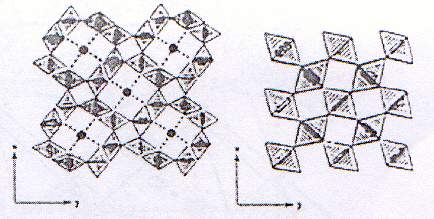
Fig.11.Structura hollanditului(stanga) si a rutilului(dreapta),
dupa planele (001)












