EVALUAREA COMPORTARII LA COROZIUNE
PRIN METODE ELECTROCHIMICE A MATERIALELOR UTILIZATE INTR-O CNE CANDU
I. Introducere
Centralele
nuclearo-electrice produc electricitate prin fisiunea uraniului si nu prin
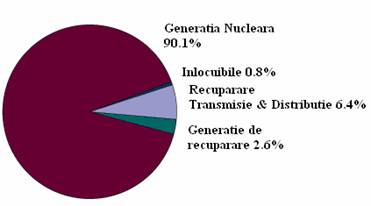
metoda clasica de ardere a combustibililor fosili. In consecinta, centralele
nuclearo-electrice nu polueaza mediul cu oxizi de azot, oxizi de sulf, praf sau
alte gaze cu efect de sera, ca monoxidul de
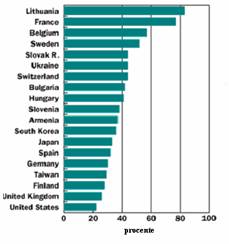
carbon (Fig.1). Astazi, peste 400 de NPP-uri
opereaza in aproximativ 25 de tari pe
intreg globul, asigurand circa 17% din necesarul de electricitate al
tarilor de pe glob (Fig 2.). In acest scop, multe natiuni contruiesc in
continuare centrale nucleare pentru acoperirea necesarului energetic datorat
cresterii permanente a populatiei si
dezvoltarii economice.
In decursul exploatarii centralelor nuclearo-electrice
s-a constatat ca, si in conditiile normale de functionare ale circuitelor de
transfer a caldurii, pot apare efecte nedorite datorate in special coroziunii,
eroziunii, hidrurarii si depunerii de diversi produsi de coroziune pe
suprafetele de transfer termic.
In general, operatiile de intretinere ale unei centrale
nuclearo-electrice (CNE) sunt deosebit de complexe si dificile, datorita
naturii specifice a acesteia. Astfel, opririle neplanificate ale instalatiilor
nucleare datorate degradarii lor prin coroziune, reprezinta aproximativ 50% din
cheltuieli in ultimii 10 ani, acestea functionand in medie cu circa 5% mai
putin .
Avand in vedere o serie de cerinte cum ar fi:
cresterea duratei de
functionare in conditii de securitate a componentelor structurale;
diminuarea costurilor
necesare de readucere a instalatiei in conditii de functionare normala dupa
opriri cauzate de inlocuirea unor componente corodate;
reducerea nivelului de
radiatii in sistemele CNE;
evitarea diminuarii puterii
instalatiei;
diminuarea riscului pierderii
increderii publicului in cei care opereaza instalatiile nucleare, este necesar
sa se cunoasca si sa se inteleaga fenomenele de degradare a componentelor
structurale dintr-o CNE.
Analiza si diagnosticarea proceselor de coroziune care
conduc la degradarea componentelor metalice aferente unei centrale
nuclearo-electrice precum si identificarea solutiilor pentru diminuarea /
prevenirea acestor procese sunt deosebit de importante, deoarece oprirea
instalatiilor pentru repararea sau inlocuirea unor componente presupune costuri
ridicate, mareste riscul expunerii la radiatii a personalului operator si riscul
contaminarii radiochimice.
In prezenta lucrare vor fi
prezentate atat unele metode utilizate in cadrul LADICON pentru analiza
componentelor corodate din instalatiile nucleare cat si metode de testare
utilizate pentru evaluarea coroziunii materialelor structurale in conditii si
medii similare cu cele in care au functionat componentele corodate.
II. Principalele activitati ale laboratorului de analiza
si diagnoza componente metalice corodate in instalatii nucleare LADICON
Notiunea
de coroziune include toate procesele chimice si electrochimice care au drept
rezultat degradarea spontana si continua a suprafetelor metalelor si aliajelor.
Majoritatea metalelor se gasesc
in natura sub forma de combinatii, cele mai frecvente fiind sub forma de oxizi
sau saruri ale acestora. In cazul respectivelor metale, starea metalica este,
deci, instabila din punct de vedere termodinamic, in prezenta agentilor chimici
si electrochimici, ele avand tendinta de a se combina, refacand, astfel, unii
dintre compusii din care au provenit. In seria tensiunilor electrochimice,
aceste metale care sunt situate inaintea hidrogenului, au, deci, potentiale mai
electronegative.
In tehnologie tocmai aceste
metale sunt folosite cu precadere, din care cauza pierderile de metale sunt
dintre cele mai mari. Un numar restrans de metale, metale nobile, se gasesc in
natura si in stare libera. Ele se situeaza dupa hidrogen in seria tensiunilor
electrochimice si sufera mai greu procesul de degradare prin coroziune.
Coroziunea este un proces
complex fiind determinat de mai multi factori. In functie de mecanismele care actioneaza,
coroziunea poate fi chimica si electrochimica.
Coroziunea chimica are loc in mediu uscat, atunci cand
metalele sau aliajele sunt atacate chimic de unele gaze dintre care enumeram:
oxigenul, clorul, bioxidul de sulf, bioxidul de carbon, hidrogenul sulfurat,
acidul clorhidric fumans, etc. Acest tip de coroziune este prezenta mai cu
seama in unele instalatii din industria chimica, fiind favorizata de temperaturile
mai ridicate.
De cele mai multe ori, coroziunea chimica capata un
aspect electrochimic (coroziune electrochimica), deoarece instalatiile,
utilajele, masinile, statiile de transformare, conductele aeriene si subterane
de gaze si apa, etc. in contact cu agentii atmosferici (oxigenul sau umezeala
din aer), devin, de fapt, sisteme electrochimice, formate dintr-un metal sau
aliaj in contact cu un electrolit. Aceste sisteme dau nastere la pile electrice
locale.
In mod uzual, pierderile cele mai insemnate de metal se
datoreaza coroziunii fierului si aliajelor feroase. Astfel, o bara de fier
lasata timp indelungat in contact cu agentii atmosferici, colecteaza in imperfectiunile
retelei metalice apa avand un pH slab acid. Aceste imperfectiuni, care vor
functiona ca anozi locali ai unor micropile electrice locale, sub influenta
moleculelor dipolare ale apei, vor favoriza transformarea fierului in oxid sau
oxihidroxid, conform urmatorului proces anodic:
M + nH2O = M(OH)n + nH+
+ ne- (2.1) formarea de
oxid sau hidroxid si
M + nH2O = Mnn- + 2nH+
+ ne- (2.2) producerea de anioni.
Electronii rezultati din acest proces
anodic raman pe bara de fier si sunt orientati spre partile marginale ale cavitatilor,
incarcand astfel suprafata metalica din aceste zone cu sarcini negative. Aceste
suprafete incarcate negativ, vor functiona ca si catozi ai pilelor electrice
locale, pe ele avand loc urmatoarele procese:
 Ionii
de Fe rezultati, vor forma cu ionii OH- hidroxidul feros, care, in prezenta
oxigenului atmosferic, se va transforma in oxid feric hidratat, cu aspect
poros, sfaramicios, de culoare rosu inchis, care poarta denumirea de rugina.
Ionii
de Fe rezultati, vor forma cu ionii OH- hidroxidul feros, care, in prezenta
oxigenului atmosferic, se va transforma in oxid feric hidratat, cu aspect
poros, sfaramicios, de culoare rosu inchis, care poarta denumirea de rugina.
 In
urma reactiei redox care are loc, rezulta, deci, rugina. Desi stratul de
rugina izoleaza suprafata metalica de mediul exterior, procesul de coroziune va
continua in profunzime.
In
urma reactiei redox care are loc, rezulta, deci, rugina. Desi stratul de
rugina izoleaza suprafata metalica de mediul exterior, procesul de coroziune va
continua in profunzime.
Experimentele de coroziune executate in cadrul LADICON in afara
reactorului abordeaza coroziunea generalizata si localizata a diferitelor componente
si materiale structurale prin diverse metode procedurate, in conformitate cu
standardele sau normele actuale si anume:
teste
de durata (indelungate) la parametrii care simuleaza conditiile de operare din
circuitele CNE (autoclavizari in conditii statice si dinamice);
teste accelerate - care se refera la teste chimice accelerate,
la evaluari de viteze de coroziune prin metode electrochimice, etc.
II.1. Activitatea de
cercetare
Pentru a urmari
efectele chimiei apei asupra coroziunii si generarii de compusi
superficiali radioactivi pe materialele structurale utilizate in miezul
reactorului si pentru a demonstra influenta transportului activitatii in
circuite, la CNE - Cernavoda exista un sistem de 4 autoclave plasat intr-un
"by-pass" al circuitului primar. Autoclavele Y1 si Y4 aflate la iesirea din
reactor, servesc la determinarea coroziunii probelor expuse in ele la 310oC, dupa iesirea
agentului termic din canalul combustibil, in timp ce in autoclavele Y2 si Y3
asamblate la intrarea in reactor, se evalueaza comportarea la coroziune a
probelor la 265oC, in conditiile circuitului secundar, dupa
iesirea agentului termic din Generatorul de Abur.
Folosind dispozitive cu
geometrie adecvata, pe langa coroziunea generalizata se mai
poate studia coroziunea fisuranta sub sarcina, coroziunea
galvanica, coroziunea in crevasa, ca si coroziunea diferitelor zone
afectate termic.
II.2.
Activitatea de analiza si diagnoza
Avand in vedere ca
activitatea de analiza si diagnoza componente metalice corodate provenite din
instalatii nucleare este deosebit de importanta pentru mentinerea securitatii
nucleare a instalatiilor din CNE, ea trebuie realizata in conformitate si
cu legislatia Comisiei Nationale pentru Controlul Activitatilor Nucleare -CNCAN,
referitor la urmatoarele metode de analiza si evaluare:
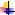 Analiza gravimetrica a
cupoanelor expuse la coroziune;
Analiza gravimetrica a
cupoanelor expuse la coroziune;
 Analiza prin
microscopie metalografica a cupoanelor corodate in autoclavele Y1-Y4 plasate in "by-pass"-ul circuitului primar
ca si a esantioanelor prelevate din componentele
metalice corodate in instalatiile nucleare din CNE;
Analiza prin
microscopie metalografica a cupoanelor corodate in autoclavele Y1-Y4 plasate in "by-pass"-ul circuitului primar
ca si a esantioanelor prelevate din componentele
metalice corodate in instalatiile nucleare din CNE;
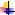 Evaluarea comportarii
la coroziune a materialelor structurale prin metode electrochimice.
Evaluarea comportarii
la coroziune a materialelor structurale prin metode electrochimice.
Se stie ca majoritatea
componentelor metalice si, in special cele executate din otel carbon, se
corodeaza in mediul apos aflat la temperaturi si presiuni ridicate, in
conditii similare celor existente in circuitele primar si secundar ale CNE
CANDU. De aici rezulta importanta executiei testelor de coroziune in acele
conditii care sa simuleze cat mai fidel pe cele din circuitele primar si
respectiv secundar, in vederea prognozarii directiilor de avansare a coroziunii
si a mecanismelor diferitelor procese de coroziune. Modalitatea
cea mai sigura si reproductibila de determinare a vitezei de coroziune a unui
aliaj consta in expunerea acestuia in mediul in care opereaza in mod normal, la
parametrii normali de exploatare, urmata de determinarea coroziunii acestuia in
acel mediu specific. In majoritatea cazurilor, aceste experimente dureaza mult
timp si implicit sunt foarte costisitoare. De aceea, un procedeu de obtinere
mai rapida a datelor referitoare la viteza de coroziune a unui metal (aliaj) expus
intr-un mediu specific este fie folosirea unor echipamente in care sa fie
simulati cat mai multi parametri de operare, fie utilizarea unor teste chimice
accelerate executate in medii mult mai agresive,
perioade mai scurte de timp.
III. Investigarea comportarii la coroziune in
solutii apoase
utilizand autoclavizari
la temperatura si presiune ridicata
Testarea
la coroziune prin autoclavizare implica expunerea cupoanelor, prelevate din
diferite materiale structurale, in mediu apos sau de vapori, la temperaturi si
presiuni ridicate, pentru perioade de timp limitate. Parametrii de lucru si
mediul de testare trebuie sa fie similare conditiilor de operare ale
componentelor corodate aflate in studiu.
Echipamentele statice folosite in testarea la coroziune
sunt urmatoarele:
 autoclave
Prolabo - 1litru: temperatura maxima 400oC (eroare masurare 5oC) si presiunea maxima 20 MPa
(eroare masurare 0,5 MPa);
autoclave
Prolabo - 1litru: temperatura maxima 400oC (eroare masurare 5oC) si presiunea maxima 20 MPa
(eroare masurare 0,5 MPa);
 autoclave
Baskerville - 5litri: temperatura maxima 400oC (eroare masurare 5oC) si presiunea maxima 20 MPa
(eroare masurare 0,5 MPa)(Fig. 3.);
autoclave
Baskerville - 5litri: temperatura maxima 400oC (eroare masurare 5oC) si presiunea maxima 20 MPa
(eroare masurare 0,5 MPa)(Fig. 3.);
 autoclava
Baskerville de 13litri: temperatura maxima 400oC (eroare masurare 5oC) si presiunea maxima 20 MPa (eroare masurare
0,5 MPa);
autoclava
Baskerville de 13litri: temperatura maxima 400oC (eroare masurare 5oC) si presiunea maxima 20 MPa (eroare masurare
0,5 MPa);
 instalatie
de decontaminare(descalare) in regim dinamic;
instalatie
de decontaminare(descalare) in regim dinamic;
 autoclava
electrochimica de 1 litru, care permite
efectuarea masuratorilor electrochimice (potentiale de coroziune in circuit
deschis, cronoamperometrie, voltametrie) la parametrii specifici circuitelor
unei centrale nucleare (temp.max.= 3000C, presiune 100atm). (Fig.4.)
autoclava
electrochimica de 1 litru, care permite
efectuarea masuratorilor electrochimice (potentiale de coroziune in circuit
deschis, cronoamperometrie, voltametrie) la parametrii specifici circuitelor
unei centrale nucleare (temp.max.= 3000C, presiune 100atm). (Fig.4.)
Cu ajutorul softului de coroziune incorporat
in autoclava electrochimica, pot fi determinate potentialele si curentii de
coroziune aferenti probelor expuse in mediile apoase specifice, la temperaturi
si presiuni ridicate. Acesti parametri electrochimici
masurati vor furniza informatii privitoare la susceptibilitatea la coroziune a
materialelor respective din centrala nucleara.
III.1. Metoda de analiza
gravimetrica a cupoanelor
Gravimetria este o metoda de analiza
cantitativa bazata pe cantarirea masei unui cupon de coroziune
inainte si dupa expunerea o perioada de timp bine determinata in
medii diferite. Pe baza cantaririlor initiale si a celor inregistrate, de
exemplu, dupa diferite perioade de autoclavizare, se determina variatia in greutate
DG in mg care se raporteaza la suprafata calculata in dm2, pe
baza determinarii dimensiunilor cupoanelor efectuate inainte de expunerea la
coroziune.
In felul acesta se determina variatia in greutate pe
suprafata , DG/S (mg/dm2), care raportata la
timpul de expunere exprimat in zile, conduce la viteza de coroziune in mg/dm2zi.
Tot pe baza determinarilor gravimetrice,
se poate estima si grosimea compusilor superficiali, cu conditia
cunoasterii tipului compusului si a densitatii acestuia.
III.2. Metode electrochimice
Controlul coroziunii are o importanta
deosebita in prevenirea/ asigurarea sigurantei oamenilor si
instalatiilor. Degradarile care conduc la avarii, la deteriorarea
vaselor de presiune, a tancurilor care contin materiale toxice sau
radioactive, pot avea ca efect final nu numai avarierea instalatiilor, ci
si ranirea sau chiar moartea a sute de persoane. Daca
securitatea instalatiei si/ sau a oamenilor nu poate fi asigurata
prin selectarea judicioasa a unor materiale sau prin folosirea unor metode
adecvate de control a coroziunii, atunci proiectul instalatiei respective trebuie
abandonat.
Coroziunea este un proces care decurge, deobicei, prin
reactii chimice si electrochimice, care au loc la interfata
material/ mediu. Coroziunea chimica este o reactie eterogena
care are loc la interfata metal/ mediu, metalul fiind unul dintre
reactanti.
In majoritatea mediilor apoase
aflate la temperaturi si presiuni ridicate, indiferent de pH-ul lor,
procesele care au loc sunt de natura electrochimica,
ele constand in doua sau mai multe reactii partiale, care
implica un transfer de electroni sau sarcini. Pentru ca o reactie
electrochimica sa aiba loc, este necesara prezenta
unui anod, a unui catod, a electrolitului si inchiderea circuitului
electric prin electrolit. De exemplu, in cazul unui proces electrochimic care
are loc la interfata metal/ mediu acid, au loc urmatoarele
reactii:
M Mn+ + ne- (3.1) reactia
de oxidare anodica concomitent cu
2H+ + 2e- 2H H2 (3.2) reactia de reducere catodica.
Dupa cum se observa din ecuatiile
reactiilor de mai sus, coroziunea are loc la anod, unde metalul sau
aliajul este oxidat, fapt care cauzeaza dizolvarea totala sau
partiala a anodului. Cand
in sistemele corodabile metal/ mediu, semireactiile anodice si
catodice sunt mutual dependente, se formeaza o celula galvanica
spontana. Celula in care electronii sunt dirijati prin intermediul
unei surse de energie externa in directie contrara aceleia in
care s-ar fi deplasat in cazul unei celule spontane, constituie o celula electrolitica. Intre metal si mediu se stabileste o
diferenta de potential care este dependenta de
compozitia electrolitului si de taria lui ionica, de
temperatura mediului, de natura metalului sau aliajului si de alti
factori mai putin importanti.
In conditii standard (1atm, 25oC), in
conditiile existentei echilibrului intre concentratia ionilor
metalici din solutie a caror activitate este egala cu 1,
densitatea neta de curent care trece prin solutie este egala cu
0. In conditiile in care curentii anodici si catodici sunt egali
in valoare absoluta si opusi ca semn, exista relatia:
ian = icat = io (3.3) in care: io
este densitatea curentului de schimb.
Potentialul electrodului este masurat in raport
cu un electrod standard de referinta, cum este de exemplu cel de
calomel standard (SCE), Cu/ CuSO4, Ag/ AgCl, etc.
Din considerente termodinamice,
potentialul unei reactii electrochimice este o masura a energiei libere Gibbs: DG = -nFE (3.4)
unde: n este numarul de electroni
participanti la reactie, F
este constanta lui Faraday (96500C/ mol) si E este potentialul electrodului. Potentialul celulei
electrochimice va depinde de concentratia reactantilor si a
produsilor rezultati din reactiile partiale respective
si de pH-ul solutiei. Potentialul poate fi corelat cu energia
libera Gibbs folosind ecuatia lui
Nernst: DE = DEo + 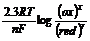 (3.5)
(3.5)
in care: DEo este
potentialul electrodului standard, (ox)
este activitatea unei specii oxidate, (red)
este activitatea speciilor reduse, iar x si
r sunt coeficientii
stoechiometrici implicati in reactiile din semicelula
respectiva.
Coroziunea va avea loc
atunci cand directia spontana a reactiei este oxidarea
metalului, adica atunci cand DG < 0. Aplicarea
principiilor termodinamicii la fenomenele de coroziune a fost
particularizata prin folosirea diagramelor
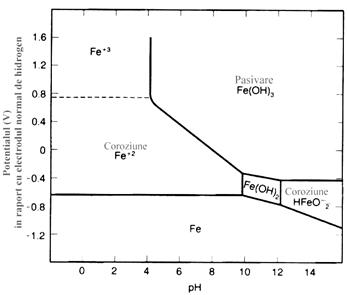
Pourbaix potential-pH. Asemenea
diagrame au fost construite pe baza calculelor facute utilizand
ecuatia lui Nernst si datele de solubilitate referitoare la
diferiti compusi. Ca exemplu, pe diagrama potential-pH aferenta
sistemului Fe-H2O (Fig.6 [12]) sunt evidentiate zonele de
potential functie de pH, in care fierul fie este imun, fie este
probabil sa se pasiveze, ca si regiunile in care coroziunea poate
avea loc.
Sistemul electrochimic Princeton Model 2273(Fig.7 si 8)
utilizat in cadrul LADICON pentru executarea masurilor electrochimice,
cuprinde: un potentiostat / galvanostat, celula electrochimica propriu-zisa (Fig.
8.) si un computer Windows XP(pentru prelucrarea datelor)(Fig.7.).
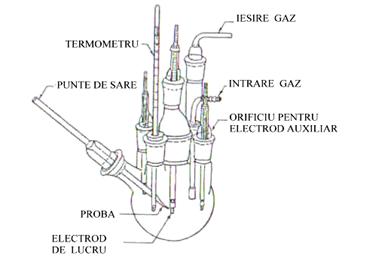
In celula electrochimica se introduce solutia
de testare, in care se imerseaza cei
trei electrozi: electrodul de lucru - proba de testat, electrozii auxiliari -
din grafit si electrodul de referinta (calomel) (SCE)(Fig.8). Pentru realizarea
masuratorilor electrochimice la temperaturi mai mari decat temperatura camerei,
solutia din celula electrochimica poate fi incalzita cu ajutorul unui
incalzitor electric.
Tipurile
de masuratori electrochimice efectuate se incadreaza in
urmatoarele categorii:
a) variatia potentialului de
coroziune in circuit deschis (Ecor) functie de timp,
determinata pe diverse sisteme (ex: otel carbon/ solutii [13])(Fig.9);
b) efectuarea de
masuratori potentiodinamice utilizand metoda polarizarii
lineare(PD) pe probe neacoperite, filmate sau decrustate, teste executate in
diverse solutii [inerte chimic, continand diverse concentratii
de contaminanti (de exemplu Cl-), de decrustare neinhibate sau
continand diverse concentratii din diferiti inhibitori, etc] in
scopul determinarii vitezelor de coroziune prin cele doua metode -
pante Tafel si a rezistentei de polarizare (Rp) - si
a suprapunerii grafice a picurilor din domeniul catodic[14].
Masuratoarea
potentiodinamica(PD)(Fig.10) necesitand inregistrarea variatiei
intensitatii curentului din celula pe parcursul baleierii
potentialului, este caracterizata prin urmatorii parametri:
- domeniul de
potential baleiat: [( (+1000)]mV
vs.(SCE);
- diverse viteze de
baleiaj ; in mod uzual se foloseste viteza de 0,2 mV/sec in
cazul probelor filmate si respectiv 1mV/sec in cazul probelor
neacoperite;
- temperatura solutiei, care poate fi temperatura
camerei sau alte temperaturi de interes, maxima fiind temperatura de 5)0C.
Metoda
potentiodinamica poate servi si la aprecierea eficientei
unui inhibitor, in care caz se va lua in calcul fie variatia vitezelor de
coroziune, fie variatia rezistentelor de polarizare(Rp) a unei
probe testate in solutie in absenta si respectiv in
prezenta inhibitorului, conform relatiei (3.4):
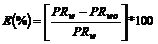 (3.4) in care:
(3.4) in care:
PRw-rezistenta
de polarizare masurata in prezenta inhibitorului dupa timpul t;
PRwo-rezistenta
de polarizare(Rp) masurata in absenta inhibitorului dupa
acelasi timp.
c) masuratori executate prin
metoda galvanostatica (sub un curent constant), cand se determina
variatia potentialului in timp;
d) masuratori executate prin
metoda potentiostatica (sub un potential constant), cand se determina
variatia intensitatii curentului in timp;
e) masuratori executate prin
metoda polarizarii ciclice (PC) pe probe expuse in solutii
contaminate, in scopul determinarii susceptibilitatii materialului
respectiv la pitting [14]. Pentru aflarea parametrilor specifici coroziunii
pitting si anume: potentialul de initiere al pittingului in
cazul probelor neacoperite (Ei) si respectiv cel de rupere al
filmului (Ebd ) in cazul celor acoperite cu diversi
compusi ca si a potentialului de repasivare a piturilor (Erp)
sau respectiv a potentialului de protectie(Eprot), este
folosita metoda polarizarii ciclice(Fig.
11).
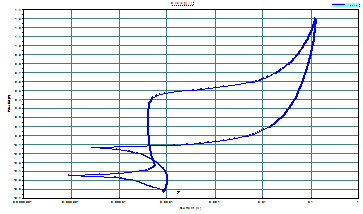
Figure 11. Curba tipica de polarizare ciclica
O metoda moderna de evaluare a
performantelor filmelor superficiale depuse pe suprafatele metalelor,
care are avantajul de a nu accelera reactiile electrochimice de la
interfata metal/solutie este metoda spectroscopiei impedantei
electrochimice (EIS), metoda larg
folosita in cercetarile de coroziune, intrucat ea prezinta urmatoarele
avantaje:
foloseste semnale foarte mici de tensiune/ curent, care
nu perturba proprietatile electrozilor;
pot fi studiate procesele de coroziune si masurate
vitezele de coroziune in lichide cu conductivitate foarte coborata, in care
metodele traditionale nu pot fi folosite;
facand o singura masuratoare, pot fi obtinute cel putin
doua caracteristici electrice ale filmelor superficiale: capacitatea stratului
dublu electric si rezistenta de polarizare.
III. 3.Metoda de analiza metalografica
Analiza metalografica consta in examinarea macroscopica si
microscopica a materialelor metalice (Fig. 12).
Analiza microscopica,
este o metoda de lucru indispensabila in studiul microstructurii materialelor,
care permite efectuarea urmatoarelor analize: determinarea microscopica a
incluziunilor nemetalice in metale si aliaje, studiul modificarii
grauntilor cristalini, determinarea morfologiei cristalitelor si a
distributiei lor dupa marime, etc.
Microscopul OLYMPUS GX 71 (Fig.12.) este un
instrument optic de vizualizare, la mariri cuprinse intre x12,5 - x2000,
care permite evidentierea morfologiei straturilor de oxizi si a depunerilor
de produsi de coroziune prezente pe suprafetele probelor. Pentru
achizitie, prelucrare si arhivare imagine, microscopul este dotat cu un PC
si un soft de lucru (program: analySIS). Se pot face examinari in camp
luminos (BF=bright field), camp intunecat (DF=dark field) si lumina
polarizata (LP) si DIC.
Aceasta analiza
poate evalua microstructura (structura fina) unui material metalic, poate furniza
informatii referitoare la fazele care alcatuiesc materialul metalic, grauntii
cristalini, distributia fazelor si grauntilor, natura acestora, marimea
cristalelor, morfologia hidrurilor, aspectul si grosimea filmelor
superficiale, etc (Fig.13). De asemenea, ea poate evidentia morfologia
suprafetelor corodate, aspectul in sectiune al filmelor superficiale si poate
determina grosimea, uniformitatea si continuitatea filmelor superficiale.
IV. Concluzii:
 Activitatea in cadrul LADICON este impartita in doua
directii: cercetari privind chimia apei si coroziunea in circuitele primar
si secundar al unei CNE CANDU si analiza si diagnoza comportarii la
coroziune a componentelor metalice corodate din instalatii nucleare.
Activitatea in cadrul LADICON este impartita in doua
directii: cercetari privind chimia apei si coroziunea in circuitele primar
si secundar al unei CNE CANDU si analiza si diagnoza comportarii la
coroziune a componentelor metalice corodate din instalatii nucleare.
 In experimentele de coroziune este studiata
coroziunea generalizata si respectiv localizata prin teste de durata
(autoclavizari statice si dinamice ) si teste accelerate. Evaluarea
comportarii la coroziune a probelor testate se face folosind metoda gravimetrica
si tehnici de analiza a suprafetelor.
In experimentele de coroziune este studiata
coroziunea generalizata si respectiv localizata prin teste de durata
(autoclavizari statice si dinamice ) si teste accelerate. Evaluarea
comportarii la coroziune a probelor testate se face folosind metoda gravimetrica
si tehnici de analiza a suprafetelor.
 Metoda
spectroscopiei de impedanta electrochimica (EIS) se utilizeaza in studiul
proceselor de coroziune si in analiza proprietatilor de aderenta si
porozitate, in special, a filmelor superficiale rezultate in urma coroziunii
probelor.
Metoda
spectroscopiei de impedanta electrochimica (EIS) se utilizeaza in studiul
proceselor de coroziune si in analiza proprietatilor de aderenta si
porozitate, in special, a filmelor superficiale rezultate in urma coroziunii
probelor.
 Metoda
gravimetrica permite determinarea vitezelor de coroziune, a cantitatilor de produsi
de coroziune eliberati si respectiv a vitezelor de eliberare a
acestora sau a metalului prin coroziune, ca si cantitatile de produsi de
coroziune total formati, aderenti si eliberati in mediul coroziv.
Metoda
gravimetrica permite determinarea vitezelor de coroziune, a cantitatilor de produsi
de coroziune eliberati si respectiv a vitezelor de eliberare a
acestora sau a metalului prin coroziune, ca si cantitatile de produsi de
coroziune total formati, aderenti si eliberati in mediul coroziv.
 Analiza
metalografica este o metoda de cercetare fizica care consta in examinarea
macroscopica si microscopica a materialelor.
Analiza
metalografica este o metoda de cercetare fizica care consta in examinarea
macroscopica si microscopica a materialelor.
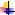 Pentru investigarea si
evaluarea comportarii la coroziune a materialelor structurale, in vederea
solutionarii cauzelor de degradare coroziva, pot fi folosite si metode
electrochimice, ca: polarizarea potentiodinamica, polarizarea ciclica si
variatia potentialului de coroziune in timp, spectroscopia impedantei electrochimice, etc.
Pentru investigarea si
evaluarea comportarii la coroziune a materialelor structurale, in vederea
solutionarii cauzelor de degradare coroziva, pot fi folosite si metode
electrochimice, ca: polarizarea potentiodinamica, polarizarea ciclica si
variatia potentialului de coroziune in timp, spectroscopia impedantei electrochimice, etc.
Bibliografie:
I. Pirvan s.a, "Studiul cerintelor din reglementari si
descrierea metodelor de analiza si caracterizare la coroziune generalizata si
localizata a componentelor metalice corodate" R.I. 7721/ 2006
M.Fulger "
Manualul Calitatii MC LADICON, Ed5, act 0 /2009
Li-TH-06 - Instructiuni de lucru la autoclava
Baskerville de 5l;
Li-TH-08 - Instructiuni de operare pentru autoclavele
Prolabo de 1l.
LI-TH-203 - Operarea autoclavei electrochimice,
ASTM E 3/2007: Standard Methods of Preparation
of Metallographic Specimens
ASTM E 7/2003: Standard Definitions of Terms
Relating to Metallographic
Scully J.R., "Corrosion Tests and Standards:
Application and Interpretation" Ed.R.Baboian (1995);
"Handbook on Corrosion Testing and Evaluation"
Ed.Ailor W.H. (1971);
Scully J.R., "Corrosion Tests and Standards: Application and Interpretation"
Ed.R.Baboian (1995);
"Handbook on Corrosion Testing and Evaluation"
Ed.Ailor W.H. (1971).
Pourbaix M., "Atlas of
Electrochemical Equilibria in Aqueous Solutions", 1951.
Procedura SCN LI-TH-190 "Determinarea comportarii la coroziune a
materialelor structurale prin metoda polarizarii lineare" Ed.3 Act.0 (2008).
Procedura SCN LI-TH-191 "Determinarea comportarii la
coroziune a materialelor structurale prin metoda polarizarii ciclice" Ed.3
Act.0 (2008).