Teste
la chimie Clasa VIII
Proba
teoretica
I.
Exista un
singur raspuns corect la testele grila care va fi completat in tabelul din foaia de concurs.
1. 2 moli amestec echimolar de Cu si un oxid al
lui cu 20% O reactioneaza cu un numar
de moli de 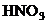 egal cu:
egal cu:
A. 4,67; B.
14; C. 7; D. 1,33; E. 2,67.
(3 puncte)
2. Prin descompunerea termica a unui azotat masa
probei solide scade cu 36,47% iar din reactie rezulta un amestec
gazos in raportul molar 2:1 si in raportul de masa 23:8. Metalul din
azotat este:
A. nobil, Au; B.
seminobil, Cu; C. seminobil, Ag; D.alcalin pamintos, Ca; E. alcalin, K.
(4 puncte)
3. Forma alotropica a apei este:
A. apa oxigenata; B. Apa grea; C. Apa
supergrea; D. Apa minerala; E. nu exista.
(1 punct)
4. La descompunerea termica a unui amestec de
azotati de argint si sodiu raportul molar al celor doua gaze
obtinute, scrise in ordinea descrescatoare a maselor lor moleculare,
este:
A. 2; B. 1;
C. 0; D. 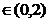 ; E. oricit in
functie de raportul molar al celor 2 azotati.
; E. oricit in
functie de raportul molar al celor 2 azotati.
(3 puncte)
5. Este corecta afirmatia:
A. Cu poate reactiona cu o solutie de 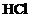 in absenta
aerului.
in absenta
aerului.
B. La dizolvarea unui cristalohidrat in apa,
moleculele de apa de cristalizare ramin atasate de moleculele de
solvat.
C. Pentru nici un element din Tabelul periodic al
elementelor doi izotopi nu pot sa aiba numere de masa in raportul
de 1:3.
D. Pentru a obtine o solutie de 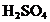 intotdeauna se
adauga apa distilata peste acid sulfuric concentrat.
intotdeauna se
adauga apa distilata peste acid sulfuric concentrat.
E. Pentru un amestec din urmatoarele gaze 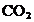 ,
, 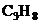 si
si 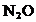 procentele de
masa si de moli sunt egale.
procentele de
masa si de moli sunt egale.
(2 puncte)
6. In schema: 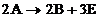
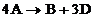
unde in A raportul de mase
dintre atomii X, Y si Z este 1,95:1,775:2,4, 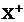 si
si 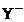 sunt izoelectronici cu
elemental cu numarul atomic 18 iar Z formeaza doua forme
alotropice (dintre care una este chiar E):
sunt izoelectronici cu
elemental cu numarul atomic 18 iar Z formeaza doua forme
alotropice (dintre care una este chiar E):
A. B este un precipitat alb brinzos.
B. A, B si D provin din acizi oxigenati ai
elementului Y.
C. B reactioneaza cu 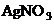 formind un precipitat
galben.
formind un precipitat
galben.
D. XY este o sare solubila in apa
diferita de B.
E. In D exista 46,21% oxigen.
(4 puncte)
7. Este corecta afirmatia:
A. In apa pura (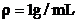 ) exista 55,55 moli de
) exista 55,55 moli de 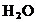 intr-un litru de
apa.
intr-un litru de
apa.
B. Precipitatul format intre o solutie
apoasa de azotat de plumb si o solutie apoasa de
iodura de potasiu este solubil in apa.
C. In reactia dintre acidul clorhidric si
permanganatul de potasiu se formeaza un gaz diatomic incolor.
D. La introducerea unei placute de Zn intr-o
solutie de 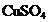 masa
placutei creste cu 1 g/ion-g
masa
placutei creste cu 1 g/ion-g 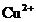 depus ca atom de Cu.
depus ca atom de Cu.
E. In reactia Fe cu 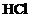 se formeaza
clorura ferica.
se formeaza
clorura ferica.
(1 punct)
8. Din lista de mai jos 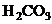 reactioneaza
cu:
reactioneaza
cu:
A. 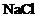 ; B.
; B. 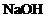 ; C.
; C. 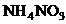 ; D.
; D.  ; E. Fe.
; E. Fe.
(1 punct)
9. La dizolvarea a 10 g 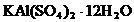 in 90 g
in 90 g 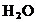 rezulta o
solutie:
rezulta o
solutie:
A. colorata; B.
De concentratie 10%; C. De
concentratie >10%; D. De
concentratie <10%; E. un
precipitat de 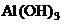 .
.
(1 punct)
10. Se da schema de mai jos (s=stare solida,
aq=solutie):
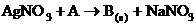
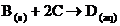
A. Substanta C este 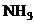 . B.
Substanta A este
. B.
Substanta A este 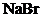 . C.
Substanta C este
. C.
Substanta C este 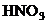 . D.
Substanta A reactioneaza cu apa si de aceea nu poate fi
folosita in scop alimentar. E.
A doua reactie este de substitutie.
. D.
Substanta A reactioneaza cu apa si de aceea nu poate fi
folosita in scop alimentar. E.
A doua reactie este de substitutie.
(2 puncte)
II.
Un amestec de 'm' g Ag si Cu
reactioneaza complet cu acidul azotic formind un amestec de
saruri care, dupa separare, are masa '2m'.
a.
Scrieti ecuatiile reactiilor chimice
implicate. (2
puncte)
b.
Calculati compozitia procentuala
masica a amestecului initial. (8 puncte)
c.
Calculati raportul molar dintre Ag si Cu
in amestecul initial. (4 puncte)
III.
Se prepara o solutie de acid sulfuric
oleum cu 20% 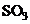 liber din 100 g
solutie de
liber din 100 g
solutie de 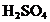 91% prin adaugare
de
91% prin adaugare
de 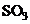 .
.
a.
Cite grame de 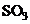 trebuie adaugate?
(8 puncte)
trebuie adaugate?
(8 puncte)
b.
Ce masa de apa trebuie adaugata
la solutia de acid sulfuric oleum obtinuta pentru a o readuce la
concentratia initiala? (7 puncte)
IV.
Masele moleculare a doua halogenuri diferite
ale aceluiasi metal difera prin 14 si au ca suma 606.
Diferenta dintre masele atomice ale halogenilor este 47.
a.
Care sunt cele doua halogenuri? (8 puncte)
b.
Scrieti reactiile cu 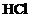 ale celor trei oxizi
ai metalului respectiv. (4 puncte)
ale celor trei oxizi
ai metalului respectiv. (4 puncte)
Nota:
1.
Toate subiectele sunt obligatorii
2.
Timp de lucru 3 ore.
3.
Mase atomice: 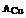 =64,
=64, 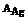 =108,
=108, 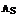 =32,
=32, 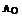 =16,
=16, 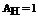 ,
, 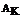 =39,
=39, 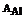 =27,
=27, 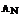 =14,
=14, 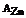 =65,
=65, 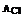 =35,5,
=35,5, 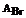 =80,
=80, 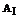 =127,
=127, 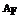 =19,
=19, 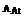 =210,
=210, 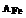 =56,
=56, 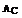 =12,
=12, 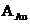 =197,
=197, 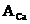 =40.
=40.
SUCCES!
BAREM
Subiectul I Testul
grila 22 puncte
|
Numar intrebare
|
Raspuns corect
|
Punctaj
acordat
|
|
1
|
A
|
3
|
|
2
|
C
|
4
|
|
3
|
E
|
1
|
|
4
|
D
|
3
|
|
5
|
E
|
2
|
|
6
|
E
|
4
|
|
7
|
A
|
1
|
|
8
|
B
|
1
|
|
9
|
D
|
1
|
|
10
|
A
|
2
|
Subiectul
II (
14 puncte)
a) 3Ag +
4HNO3 = 3AgNO3 + NO↑ + 2H2O (1 punct)
3Cu + 8HNO3 = 3Cu(NO3)2
+ 2NO↑ + 4H2O (1
punct)
b)
8
puncte
% Ag = 68,7
% Cu = 31,3
c)
4
puncte
Ag : Cu = 1,3
Subiectul
III ( 15 puncte)
a) 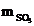 = 75 g ( 8 puncte)
= 75 g ( 8 puncte)
b) 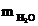 = 25,96 g ( 7 puncte)
= 25,96 g ( 7 puncte)
Subiectul
IV (
12 puncte)
a) - Determinarea halogenilor: I, Br ( 2 puncte)
- Determinarea metalului: Fe ( 2 puncte)
- Determinarea valentelor : 2,3 ( 2 puncte)
- Determinarea formulelor : FeI2 si FeBr3 ( 2 puncte)
b)FeO + 2HCl = FeCl2 + H2O ( 1 punct)
Fe2O3
+ 6HCl = 2FeCl3 + 3 H2O
( 1 punct)
Fe3O4
+ 8 HCl = FeCl2 + 2 FeCl3 + 4H2O ( 2 puncte)
TOTAL : 63 PUNCTE
OFICIU: 7 PUNCTE
70 PUNCTE