STARILE
FIZICE ALE MATERIEI
1. Clasificarea
substantelor dupa starile de agregare
La
nivel macroscopic materia se prezinta in trei stari net diferite,
numite stari de agregare: gazoasa, lichida si solida,
fiecare cu proprietatile ei specifice. Din punct de vedere
fenomenologic, cele trei stari de agregare pot fi caracterizate astfel:
starea gazoasa - nu are nici forma si nici volum propriu;
starea lichida - nu are forma proprie, insa are volum propriu;
starea solida - are si forma si volum propriu.
Substantele aflate in stare solida, in
functie de aranjarea spatiala a particulelor componente, in
conditii normale de temperatura si presiune, se clasifica
in:
solide cristaline - in
care particulele componente sunt aranjate ordonat si periodic in
spatiu in nodurile unei retele numita retea cristalina;
solide amorfe - in
care particulele componente nu mai sunt dispuse ordonat, de aceea starea
amorfa este o stare intermediara intre starea cristalina si
cea lichida.
Existenta starilor de agregare ale materiei poate
fi explicata daca se tine cont de miscarea, interactiunea si structura particulelor ce
alcatuiesc corpurile. Particulele se gasesc intr-o stare de miscare numita
agitatie termica, care este dependenta de temperatura
si are un caracter haotic. Aceasta miscare confera
particulelor energie cinetica, insa in acelasi timp particulele
interactioneaza intre ele ceea ce determina aparitia
energiei potentiala. Interactiunea dintre particule este
exprimata prin fortele intermoleculare, care pot fi de tip electric,
van der Waals, etc., toate impreuna fiind numite forte de coeziune. Intre fortele de coeziune din cele
trei stari de agregare exista urmatoarea relatie:
Fgaz < Flichid < Fsolid (1)
2. Transformari de faza
Aprecierea
asupra starii de agregare a materiei se face in conditii normale de
temperatura si presiune (T= 293 K, p = 1 atm), insa o
substanta poate exista in toate cele trei stari de agregare, in
functie de conditiile de temperatura si presiune la care
este supusa. Trecerea dintr-o stare de
agregare in alta se numeste transformare
de faza.
In figura 1. este prezentata diagrama de stare si
procesele care apar cand au loc transformarile de faza.
Punctul
triplu (PT) - reprezinta punctul in care coexista toate cele trei
stari de agregare, in echilibru dinamic fiind caracterizat de o anumita temperatura si presiune,
specifice substantei respective.
Punctul
critic (PC) - este punctul peste a carui temperatura gazul nu mai
poate fi lichefiat, indiferent cat de mult ar creste presiunea.
Un sistem material poate fi
constituit din mai multe componente, fie in aceeasi stare de agregare, fie
in stari diferite. Daca mediul este continuu, fara zone
separate, sistemul este monofazic. Cand in sistem exista zone de discontinuetate,
sistemul este polifazic, iar suprafata de separatie dintre doua
zone se numeste interfata.
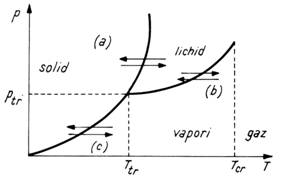
Fig. 1. Diagrama de stare; PT - punct triplu, PC
- punct critic, (a) topire si solidificare; (b) vaporizare si
condensare; (c) sublimare si desublimare.
Stari de agregare in organismele vii
Din
punct de vedere al starii de agregare materia vie este heterogena,
fiind un sistem polifazic. Totusi, ca urmare a adaptarii organismelor
vii la diferitele conditii de mediu, se poate decela existenta
substantei in cele trei stari de agregare.
Gazele in sistemele vii se gasesc sub trei forme:
nedizolvate in
alveolele pulmonare, sinisuri osoase, in tubul digestiv etc;
dizolvate in
diversele lichide: plasma, lichid cefalorahidian etc;
combinate cu
unele biomolecule, cum este hemoglobina.
Starea lichida este prezenta
in organism sub diferite forme:
lichide circulante: sange, plasma, lichid cefalorahidian;
mediu lichid:
citoplasma, lichidul interstitial;
lichide de
secretie;
lichide de excretie: urina, transpiratia;
structuri fluide: mediile refringente din ochi, membrana celilara.
Lichidele biologice nu sunt
niciodata lichide pure, ele sunt sisteme de dispersie complexe de cele
trei tipuri: solutii, coloizi sau suspensii. Solventul tuturor lichidelor
biologice este apa, ce se gaseste in cantitate mare in organismele
vii si poseda proprietati speciale, care vor fi studiate in
capitolul urmator.
Starea solida in organismele vii se gaseste
sub forma de:
structuri
microscopice: macromolecule, organite citoplasmatice, organite nucleare,
citoschelet, dispozitive contractile, structuri solide extracelulare, cum ar fi
substanta fundamentala din tesutul conjunctiv, cartilaginos
si osos, scheletul celulozic la plante;
solide cristaline si amorfe: oase, dinti, par;
structuri complexe care din punct de vedere macroscopic se
comporta ca solide: muschi, organe, peretii vaselor sangvine.
In organismele vii nu exista
intotdeauna o delimitare precisa intre starile de agregare ale
substantei din cauza existentei starilor de intermediare si
mixte. De exemplu, sangele este un fluid cu o alcatuire complexa, ce
contine elemente figurate (leucocite, hematii, trombocite) cu proprietati de solide
plastice si elastice si in care sunt dizolvate gaze ca oxigen, bioxid
de carbon, azot etc.
4. Cristale lichide
Cristalele lichide sunt o clasa
speciala de substante care din punct de vedere al
mobilitatii se comporta ca lichidele, insa au
proprietati asemanatoare cristalelor, de exemplu, optic,
ele sunt birefringente. Starea de cristal lichid poate fi obtinuta prin
topirea, prin racirea materialului topit sau prin actiunea unui
solvent (in cazul substantelor liotrope).
In cazul substantelor de interes
biologic, cristalele lichide sunt substante organice la care
tranzitia solid - lichid se face prin intermediul unor stari stabile
in care substanta este anizotropa, dar fluida. Aceste faze
intermediare se numesc mezofaze, faze
mezomorfe sau fluide condensate cu
anizotropie spontana.
Orientarea spatiala a
moleculelor sau a agregatelor moleculare este o caracteristica impotanta
care confera substantei proprietati de cristal lichid.
Pentru a se forma faze mezomorfe stabile, moleculele trebuie sa
indeplineasca urmatoarele conditii:
sa fie alungite si sa aiba parti
asezate in acelasi plan (exemplu ciclul benzoic);
axa lunga a moleculei sa contina legaturi
duble sau triple care sa-I ofere rigiditate;
trunchiul rigid al moleculei sa contina dipoli electrici
permanenti, puternici, dar si grupari care se pot polariza
usor;
la extremitatile moleculei trebuie sa existe
grupari dipolare slabe.
In cazul materiei vii se cunosc trei
tipuri de structuri moleculare care pot indeplini aceste cerinte, si
anume:
molecule
organice mici, de exemplu esterii colesterorului (observatie: colesterolul
insasi nu este cristal lichid);
agregate moleculare
elicoidale lungi, sub forma de baghete (exemple ADN-ul si anumite
virusuri);
structuri
asociate care sunt amestecuri de amfoliti cu solventi polari, cum ar
fi apa, obtinandu-se la o anumita concentratie o orientare a
gruparilor hidrofile si
hidrofobe (exemplu membrana celulara).
Cristalele lichide, in functie de
conditiile de formare a fazei mezomorfe, se pot clasifica in:
a)
termotrope - care se obtin intr-un anumit domeniu de temperatura (Fig. 2).
Dupa orientarea spatiala a moleculelor, acestea se impart in:
nemantice - in care toate
moleculele se aranjeaza cu axa lunga dupa o directie
preferentiala. Aceste cristale au o transparenta de 100%, insa nu au activitate
optica.
colesterice - sunt formate din straturi in care
moleculele sunt orientate cu axa lunga paralel. Straturile sunt rotite
continuu spre stanga sau spre dreapta cu un anumit unghi, ce difera de la
un strat la altul, obtinandu-se astfel o structura de tip elicoidal. Aceste cristale sunt optic active.
smectice - care au o
structura stratificata, grosimea unui strat fiind egala cu axa
lunga a moleculelor (exemplu mielina).
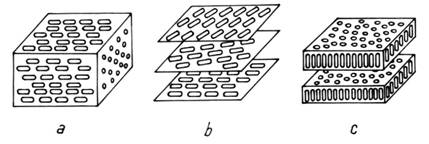
Fig. 2. Cristale
lichide termotrope. (a) nemantice, (b) colesterice, (c)
smectice.
b)
liotrope - se obtin intr-un anumit domeniu de concentratie.
Lichidele biologice, fiind formate dintr-o parte hidrofila si
din doua
parti hidrofobe, au un caracter amfoter. Astfel, intr-un anumit
domeniu de concentratie al mediului apos, care este puternic polar, ele
formeaza structuri micelare sferice, cilindrice, prismatice sau structuri
lamelare (fig. ).
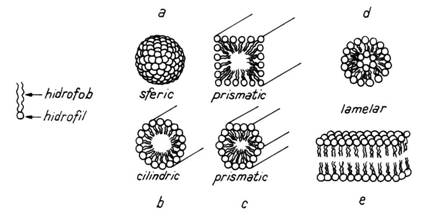
Fig. Cristale lichide liotrope.
Micelele
sunt complexe moleculare, rezultate in urma interactiunilor de tip van der
Waals ale unor compusi moleculari, care pot fi constituiti din
molecule mici sau macromolecule. Stabilitatea acestor agregate moleculare este
asigurata de legaturile hidrofile si interactiunile
hidrofobe.
Acest
tip de structura moleculara se regaseste in membranele
celulare, care au caracteristicile unor
cristale lichide.




